Traumatologie
Coordonné par E. Bui Quoc
C. Burillon
La traumatologie oculaire de l’enfant est beaucoup plus fréquente que l’on imagine, facilitée par la maladresse de l’enfant, son imprudence, et l’agression volontaire ou non de l’entourage. Le segment antérieur (SA) est principalement touché, et le pronostic visuel est marqué par le risque majeur d’amblyopie qui doit rester la principale préoccupation dans notre prise en charge.
De nombreux éléments spécifiques à la pédiatrie doivent être connus afin de mieux cerner certaines étiologies et d’améliorer notre conduite face à cette urgence traumatologique, qu’elle soit bénigne ou sévère :
l’heure du traumatisme et la cause pourront parfois être difficiles à déterminer du fait de l’impossibilité pour l’enfant de raconter ce qu’il lui est arrivé, s’il est trop petit ou en raison de la volonté de cacher cet accident, s’il est un peu plus grand et se sent fautif;
l’examen initial n’est pas toujours possible, l’acuité visuelle pas toujours déterminée, et seul un examen sous anesthésie générale permettra d’affiner le diagnostic des lésions et d’adapter la décision thérapeutique et le geste chirurgical s’il est nécessaire;
les parents doivent être écoutés. Des explications franches sur les différentes étapes de la prise en charge, à l’attention des parents mais aussi de l’enfant, permettent d’obtenir leur adhésion au projet thérapeutique et une diminution conséquente de leur anxiété. Cet entretien permet d’évaluer également la relation parent-enfant, afin de ne pas passer à côté de la possibilité de sévices ou d’automutilation.
L’incidence globale des traumatismes oculaires de l’enfant varie selon la notion de gravité, la période de recueil des données et le pays d’où proviennent les statistiques. Les traumatismes oculaires sévères, qui sont ceux que l’on peut recenser facilement car nécessitant le plus souvent une hospitalisation, touchent entre 8 et 15/100 000 enfants/an [1, 2, 3] dans des études britanniques et américaines, et 14,6/100 000 enfants en Jamaïque dans une belle étude de Mowat [4] en 2012.
Une étude au Népal, datant de 2000, retrouve un chiffre de 300/100 000 enfants/an [5], mais en incluant les cas ne nécessitant pas d’hospitalisation. Or ces derniers cas représentent heureusement 95 % des traumatismes oculaires de l’enfant, suggérant que le nombre total de traumatismes oculaires de l’enfant est bien supérieur, entre 200 et 300/100000/an.
Si l’on s’en tient aux études les plus récentes [1, 2], 45 % des enfants vus aux urgences de nos services consultent pour un traumatisme oculaire.
Le sexe est le plus souvent masculin dans toutes les études, mais cette prépondérance est plus élevée dans certains pays – Israël (sex-ratio homme/femme : 4:1), Afrique du Sud (2,3:1), Écosse (2,3:1) – que dans d’autres – Cameroun (1,8:1), États-Unis (1,7:1), France (1,6:1) [2]. Cette prépondérance a eu tendance à diminuer cependant au cours de ces dernières années.
L’âge moyen se situe autour de 7 ans [2], étant entendu que l’incidence est très faible en dessous de 2 ans [6, 7], qu’elle stagne entre 2 et 12 ans, puis qu’il y a un pic de fréquence entre 12 et 15 ans.
La plupart du temps [1, 2, 8], le traumatisme a lieu, en fréquence, au domicile (55 à 65 % ) à l’école (14 à 18 % ), puis dans la rue. L’âge est corrélé au lieu de la blessure, puisque seuls les enfants scolarisés (4–15 ans) peuvent être des victimes à l’école et, généralement, les plus grands (> 12 ans), des victimes de traumatismes dans la rue. Il est ainsi évident que la surveillance des parents est fréquemment mise en défaut.
Les agents responsables sont également corrélés à l’âge [6, 7 ]. Les produits chimiques représentent 30 % des causes d’accidents oculaires chez les petits enfants de moins de 3 ans, mais seulement 5 % après 8 ans. Inversement, les traumatismes en rapport aux activités sportives (football, squash, badminton, jeu de fléchettes) sont nuls en dessous de 2 ans et atteignent 30 % des causes après 10 ans. Les jouets (volontiers jetés à la tête de la sœur, du frère ou camarade) sont impliqués entre 5 à 10 % , les fournitures de bureau ne dépassent pas 10 % des causes avec un pic vers 5–8 ans. Les pistolets (en jouet ou non), paintballs [9], armes à feu et feux d’artifice sont volontiers responsables de traumatismes sévères – perforants ou brÛlures – et touchent les enfants au-delà de 8 ans, en général, sans dépasser 10 % des causes [6, 7]. Enfin, les projectiles lancés, en pierre ou métal, des boules de neige, concernent les enfants au-delà de 5 ans, avec une fréquence qui peut aller de 7 à 21 % .
Les lésions oculaires par airbag se sont développées avec l’augmentation de la sécurité de nos véhicules. L’explosion accidentelle ou l’ouverture occasionnée par un choc peut créer un traumatisme contusif sévère (hyphéma, éclatement du globe) si l’enfant est en face de l’airbag. Bien sÛr, l’existence de ces airbags a diminué considérablement le niveau de mortalité et morbidité des accidents de voiture. Mais il faut positionner les sièges de nourrissons de telle façon qu’ils tournent le dos au tableau de bord et les sièges d’enfant plus grands toujours à l’arrière du véhicule [10 ].
Les blessures infligées représentent un problème aussi important que les accidents. Les coups de poing ou plaies par couteau ou autres objets tranchants, volontairement, à l’occasion de bagarre sont rares (5,66 % ), mais très graves en ce qui concerne les perforations oculaires.
Les traumatismes par automutilation [11 ], chez certains enfants porteurs de retards mentaux, en particulier les syndromes de Lesch-Nyhan et de Gilles de la Tourette, consistent en des chocs répétés dans les yeux (doigt qui appuie fortement sur le globe et parfois autour) ou des blessures par aiguille : ces lésions sont responsables de cataracte, de décollement de rétine (DR) dont le pronostic est sombre. L’œdipisme ou self-enucleation peut exister chez des adolescents schizophrènes [12 ] et nécessite une force toute particulière dans les doigts, à moins qu’ils n’utilisent (plus rarement) des ciseaux ou couteaux. Enfin, les enfants secoués (avant 6 mois souvent) ou battus (syndrome de Silverman) peuvent présenter des lésions oculaires dont le diagnostic étiologique n’est pas toujours facile à faire [13 ]. Les hémorragies rétinovitréennes sont souvent associées à des hémorragies intracérébrales, voire des zones d’atrophie cérébrale. Des fractures et plaies, brÛlures de cigarette, pourront nous orienter vers une maltraitance et nous permettre de séparer l’enfant de ses parents. Si le pronostic visuel est mauvais, le pronostic vital de ces enfants est engagé dans 13 à 30 % des cas. Les corrections punitives ou sévices se voient principalement dans certains pays où la répression physique est considérée comme un moyen d’éducation, avec parfois jusqu’à un quart des enfants qui présentent un traumatisme oculaire en raison de cette cause [14 ].
Dans une étude française de 2015 [2 ], l’étiologie principale du traumatisme oculaire de l’enfant était le coup d’ongle donné involontairement (12,45 % ) suivi de corps étranger (10,95 % ), de jouet (10,19 % ) et de produit chimique ménager (10,19 % ). Les causes sportives (7,55 % ) dépassaient les causes par bagarre (5,66 % ) et par fournitures de bureau (4,90 % ). Il est intéressant de noter que sur 265 enfants examinés pour traumatisme oculaire sur 6 mois, deux enfants s’automutilaient (0,75 % ). Cette cause n’est donc pas rare et mérite que nous soyons très vigilants dans nos interrogatoires.
Il est essentiel de se renseigner sur les pathologies préexistantes de l’enfant qui pourraient favoriser ou aggraver le traumatisme, comme un trouble de la coagulation, une fragilité sclérocornéenne (maladie d’Ehlers-Danlos par exemple), une chirurgie du globe comme la chirurgie de la cataracte ou greffe de cornée. En cas de globe ouvert, la vaccination antitétanique devra être à jour, d’où l’intérêt de disposer du carnet de santé de l’enfant.
L’inspection permet de parler à l’enfant, de le rassurer et, en même temps, de poser des questions à l’enfant et à ses accompagnateurs, généralement les parents. Les circonstances de survenue sont détaillées si possible : existence ou non d’un corps étranger (CE) responsable du traumatisme; heure du traumatisme; date de la dernière prise alimentaire. Les signes fonctionnels sont précisés (douleur, baisse de vision, céphalées, douleurs abdominales, osseuses, etc.). L’examen ophtalmologique n’est conduit qu’après l’élimination de lésions générales qui pourraient mettre en jeu le pronostic vital.
L’examen des pupilles, avec évaluation de la symétrie et du réflexe photomoteur direct et consensuel, est généralement analysable. Une évaluation des annexes et de la surface conjonctivale est faite avec un éclairage doux.
L’acuité visuelle a une valeur médico-légale mais demande la coopération de l’enfant. Elle peut se limiter à la perception ou non de la lumière, des doigts.
L’examen à la lampe à fente (LAF) se fait si possible, sans forcer sur l’ouverture des paupières surtout si l’on suspecte une plaie. Une goutte de collyre anesthésiant est systématiquement instillée pour soulager la douleur cornéenne. Une goutte de fluorescéine est également instillée dans la foulée pour mieux déterminer les lésions cornéennes. Le fond d’œil (FO) est réalisé avec douceur, en ophtalmoscopie directe ou indirecte selon les habitudes de l’ophtalmologiste.
L’échographie oculaire B n’est réalisée qu’en cas de globe fermé. Un scanner, ou imagerie par résonance magnétique (IRM), sera demandé en cas d’atteintes maxillofaciales ou neurologiques associées. En cas de suspicion de CE métallique intra-oculaire, l’IRM est contre-indiquée.
La tomographie par cohérence optique (optical coherence tomography [OCT]) du SA permet d’obtenir de belles images sans contact oculaire dans le cas où il n’y a pas de trouble trop important des milieux.
Selon le contexte, afin de ne pas traumatiser encore plus l’enfant et de ne pas aggraver les lésions, un examen sous anesthésie générale peut être proposé, en prévenant les parents de la prise en charge chirurgicale qui en découlera si cela s’avère nécessaire (plaie).
Nous suivrons la classification internationale de Birmingham qui permet de classer les différents types de traumatismes à globe ouvert et fermé. Cette classification appelée BETT (Birmingham Eye Trauma Terminology System) est adoptée par les sociétés savantes internationales [15 ].
Largement majoritaires dans la traumatologie oculaire de l’enfant, entre 75 et 99 % des cas, ces traumatismes, souvent des contusions, ne présentent aucune spécificité chez l’enfant par rapport à l’adulte. Le SA est touché comme le segment postérieur (SP).
Un coup d’ongle, un ballon ou une balle, un coup de poing et les traumatismes par branchage, par jet d’objets (jouets le plus souvent) sont le plus fréquemment responsables de ces lésions.
Les hémorragies palpébrales, les œdèmes et les plaies superficielles palpébrales sont fréquents en cas de ballon reçu sur le globe oculaire.
Il ne faudra pas s’arrêter là dans l’examen, car souvent l’ouverture des paupières met en évidence une hémorragie sous-conjonctivale, parfois impressionnante, car elle distend les espaces et peut empêcher une fermeture correcte des paupières. Il n’y a pas de traitement particulier, la disparition de l’hémorragie se fera en 2 à 3 semaines, comme pour un hématome, et seul un traitement lubrifiant sera conseillé.
Un hyphéma témoigne du retentissement important du coup dans le SA, puisque l’hémorragie provient de l’iris ou du corps ciliaire distendus par l’expansion équatoriale induite par la compression antéropostérieure du globe. Dans ce cas, il est parfois nécessaire d’hospitaliser l’enfant pour un repos strict, en position semi-assise, avec un apport de boisson conséquent permettant la résorption de cet hyphéma via la filtration trabéculaire. Une hypertonie peut survenir de manière immédiate (un tiers des cas) ou retardée; elle est observée dans 48,6 % des hyphémas, quelle que soit la période [16 ], conséquence d’un dommage trabéculaire qui peut devenir irréversible : déchirures angulaires (fig. 25-1), récession angulaire dans 60 % des cas, synéchies antérieures périphériques, fibrose trabéculaire. Cet hyphéma peut saigner de nouveau, quelques jours après le traumatisme initial, se surajoutant au sang sombre de la chambre antérieure. Il aura alors plus de difficulté à s’évacuer spontanément. Dans 14,3 % des hyphémas, un lavage chirurgical peut être indiqué, à l’aide d’un système bimanuel d’infusion-aspiration, en cas d’hypertonie non gérable par un traitement médical, de persistance d’un hyphéma de plus de 50 % du volume de la chambre antérieur après 1 semaine d’évolution, plus rarement lors d’hématocornée débutante [16 ].
Une iridodialyse ou une cyclodialyse peuvent également être évidentes avec une extension circonférentielle qu’il faudra préciser, ou visible uniquement en gonioscopie si limitée. L’OCT ou l’ultrasound biomicroscopy (UBM) permettent alors d’en apprécier la gravité. Une hypotonie peut accompagner la cyclodialyse, par hypoxie des corps ciliaires et augmentation de la résorption uvéo-sclérale de l’humeur aqueuse via l’espace sous-choroïdien. Dans toutes ces lésions iridociliaires, la prescription d’un cycloplégique est indispensable dans un premier temps.
Moins grave mais responsable d’une déformation pupillaire, voire d’une mydriase réflectique, la rupture du sphincter irien n’est pas rare dans ces traumatismes. Attention à ne pas la confondre à une anomalie du jeu pupillaire qui devra justifier une imagerie orbitaire et cérébrale.
Un œdème cornéen peut apparaître en raison d’une lésion de l’endothélium par déchirure de la membrane de Descemet lors de la distension excessive secondaire au raccourcissement antéropostérieur induit par le coup direct. Les lignes de rupture apparaissent sous la forme de lignes épaissies au niveau descemétique, facilement visibles en rétro-illumination, entourées d’œdème stromal. Une baisse de vision apparaît avec photophobie et perception de halos colorés. Ce traumatisme est connu lors d’un accouchement avec l’aide de forceps qui compriment le globe oculaire, avec apparition de vergetures endothéliodescemétiques bien visibles quelques mois ou années après la naissance (fig. 25-2). Un OCT de SA visualise la lésion et son importance [17 ]. Dans tous les cas, l’œdème initial disparaît progressivement grâce à la colonisation de la brèche par les cellules endothéliales avoisinantes. Seul un comptage endothélial secondaire permettra d’évaluer le pronostic de ce nouvel endothélio-descemet et de prédire la nécessité d’une greffe endothéliale dans l’avenir.
La cataracte contusive est le plus souvent corticale postérieure ou sous-capsulaire postérieure, en rosace. L’apparition est volontiers retardée, entre un mois et plusieurs années après la contusion. Une zonulolyse partielle peut coexister, responsable d’une subluxation modérée ou franche avec l’existence d’un phacodonesis ou d’un iridodonesis. L’irrégularité de la profondeur de la chambre antérieure est un bon signe ainsi que la présence de vitré en chambre antérieure. La gonioscopie permet de faire le bon diagnostic et de préparer le geste chirurgical. La luxation antérieure du cristallin est rare, dans la chambre antérieure avec hypertonie par blocage pupillaire. La luxation postérieure totale est plus fréquente, souvent sans douleur, mais avec une baisse d’acuité visuelle en rapport avec l’aphaquie. Le retentissement dans le SP (vitré et rétine) doit être évalué avant la décision chirurgicale. La prise en charge chirurgicale pour enlever le cristallin est délicate, par voie antérieure ou postérieure, avec une implantation pas toujours possible dans le sac capsulaire, parfois possible dans le sulcus, et avec parfois un implant clippé à l’iris; l’implantation n’est pas réalisable si l’état oculaire n’est pas parfait : une correction par lentille de contact sera alors la plus sage des solutions.

Fig. 25-1 Lésions angulaires post-contusives.
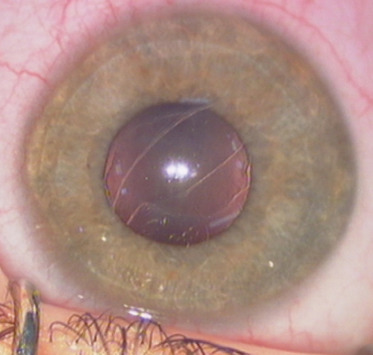
Fig. 25-2 Vergetures endothéliodescemétiques post-traumatiques.
La plaie conjonctivale nécessite une exploration de la sclère afin d’éliminer toute perforation sclérale. Elle sera suturée par des points de Vicryl® 7/0 si elle dépasse 10 mm. La plaie cornéenne lamellaire est souvent très douloureuse et ne peut s’explorer que sous anesthésie générale chez l’enfant. Il faut nettoyer la partie postérieure du scalp cornéen et décider de le maintenir avec quelques points de monofilament 10/0 s’il est trop épais, ou s’il se rétracte, source de cicatrices vicieuses et d’astigmatisme irrégulier induit. Parfois, la pose d’une lentille cornéenne souple laissée pendant quelques jours, sous couverture antibiotique, dispense de la nécessité d’une suture. Les simples érosions cornéennes sont traitées par collyres et pommades antibiotiques et cicatrisants.
Les CE cornéens superficiels chez l’enfant sont rarement métalliques mais plutôt d’origine végétale. La cornée peut être criblée lors d’explosion. Le tableau est toujours bruyant avec douleur, photophobie, larmoiement et spasme palpébral, et calmé par l’instillation d’un collyre anesthésique. L’ablation de tous les CE doit être réalisée sous anesthésie générale le plus souvent. Les tentatives d’ablation sont parfois laborieuses et il faut éviter de pousser le CE dans la profondeur de l’épaisseur cornéenne voire dans la chambre antérieure, maladroitement. En cas de CE stromal profond, le CE est abordé en réalisant un volet cornéen à base limbique, permettant un abord d’emblée profond et tunnelisé. Dans le cas particulier des poils de chenille processionnaire, il faut être patient et ne pas s’obstiner à enlever tous ces poils cassants et transparents. Ils migrent généralement dans la chambre antérieure et sont détruits au prix d’une réaction inflammatoire. Une corticothérapie locale est indiquée rapidement et permet également de diminuer l’œdème palpébral volontiers associé.
Le SA de l’œil est le plus souvent concerné par ce traumatisme; 43 % des traumatismes perforants de l’œil apparaissent chez des enfants de moins de 18 ans [18 ].
Les agents responsables sont un objet tranchant ou contondant (lame de couteau, ciseaux, flèche, extrémité pointue d’un jouet, etc.) ou un CE entrant en contact avec œil à pleine vitesse (métal, plomb), qui va être responsable de lacérations pénétrantes pouvant s’associer à un orifice de sortie dans les lacérations perforantes. C’est le cas des CE intra-oculaires qui ressortent dans l’orbite parfois. La rupture du globe est secondaire à l’augmentation de la pression intra-oculaire (PIO) liée au traumatisme et a lieu au niveau de points de faiblesse du globe oculaire : cicatrices anciennes – de chirurgie de cataracte, de greffe, (fig. 25-3), etc. – ou zones saines limbique ou sclérale en arrière des muscles droits. La rupture est souvent plus grave que la lacération.
Contrairement aux érosions cornéennes, les plaies du globe sont rarement douloureuses.
Il s’agit d’une urgence chirurgicale avec risque infectieux majeur justifiant la mise immédiate sous antibioprophylaxie intraveineuse à large spectre. Ici encore, le bilan des lésions est souvent fait sous anesthésie générale. Un Seidel peut confirmer préalablement l’ouverture ainsi qu’une chambre antérieure plate, une hypotonie majeure et une correctopie. Une hernie d’iris peut obstruer la plaie. Les berges de la plaie doivent être parfaitement nettoyées – avant de les suturer par des points séparés, de façon étanche, en évitant une invasion épithéliale secondaire –, et le moins astigmatogène possible. Les tissus extériorisés sont le plus souvent réintégrés, sauf s’ils sont nécrosés.
S’il existe des CE intra-oculaires, mis en évidence par l’examen clinique et le scanner, il est nécessaire de les retirer mais pas toujours lors de la première chirurgie de parage des plaies. Un CE angulaire nécessite une reprise lorsqu’il n’y a plus d’hyphéma. L’OCT ou l’UBM permettent de mieux le localiser et l’abord limbique sous un volet scléral est souvent la technique la moins délétère. Le CE intracristallinien nécessite d’aborder également la chirurgie cristallinienne et il faudra apprécier auparavant l’état des capsules et de la zonule cristalliniennes.
La particularité de la cataracte des traumatismes à globe ouvert est la possibilité d’effraction des capsules par l’objet pénétrant. La présence de masses dans la chambre antérieure peut déclencher une réaction inflammatoire (cataracte phacolytique) avec hypertonie oculaire nécessitant parfois une chirurgie rapide. Sinon, la prise en charge est volontairement retardée, après la cicatrisation correcte de la plaie cornéosclérale. L’implant intra-oculaire est alors positionné en fonction des résidus capsulaires et iriens, sauf s’il n’y a plus de tissu de maintien. L’implant Artisan® permet depuis plus de 15 ans de corriger l’aphaquie de ces enfants avec un bon résultat sur l’acuité visuelle et un comptage endothélial qui reste stable après 10 ans [19 , 20 ].
Les endophtalmies ne présentent pas de spécificité chez l’enfant en dehors des retards de diagnostic. Le pronostic visuel peut être mauvais du fait d’une flore plus virulente (comme le Bacillus cereus ou comme un champignon) notamment si le traumatisme a lieu en milieu rural. L’antibioprophylaxie générale ne se discute plus et tout patient suspect d’infection bénéficie immédiatement de prélèvements vitréens (culture et polymerase chain reaction [PCR]), suivis d’injections intravitréennes d’antibiotiques et d’antifongiques.
Malgré toutes ces complications potentielles, la moitié des enfants récupèrent une acuité visuelle supérieure à 5/10 dans ces traumatismes perforants du SA [21 ]. Les facteurs de mauvais pronostic sont le jeune âge (< 5 ans), l’acuité visuelle basse et la présence immédiate d’une cataracte [18 ].

Fig. 25-3 Rupture cornéenne sur cicatrice de greffe de cornée antérieure.
Les métalloses sont maintenant exceptionnelles car les CE intra-oculaires sont systématiquement enlevés. La sidérose, indiquant la présence d’ions ferreux dans l’œil, se traduit par des anomalies à l’électrorétinogramme (ERG) très rapidement. La chalcose est liée à la libération de particules de cuivre ionisées : un anneau de Kayser-Fleischer peut permettre de faire le diagnostic, après élimination d’une maladie de Wilson. Les altérations ERG sont plus tardives et les ablations tardives des CE intra-oculaires sont alors difficiles et ne permettent pas un retour en arrière des lésions.
La phtise oculaire est la complication d’un traumatisme très délabrant, avec parfois plusieurs chirurgies oculaires sans succès. L’œil est alors hypotone, avec une cornée parfois excavée. Cet œil non fonctionnel, au-delà de toute ressource thérapeutique, peut devenir douloureux. Pour cette raison, il faut expliquer aux parents et à l’enfant l’intérêt d’une chirurgie radicale (éviscération ou énucléation) en signalant le risque d’ophtalmie sympathique sur l’œil sain et en insistant sur l’amélioration esthétique grâce aux équipements prothétiques : des photographies de patients avec prothèse seront alors les bienvenues pour rassurer et persuader de la nécessité de cette chirurgie qui inquiète toujours.
L’ophtalmie sympathique peut apparaître sur l’œil sain, lorsque l’œil traumatisé est inflammatoire, souvent non voyant et en phtyse. Une uvéite granulomateuse apparaît sournoisement et oblige à un traitement intensif par corticoïdes, localement, au niveau des deux yeux. Seule une éviscération correcte, ou une énucléation, de l’œil traumatisé et perdu fonctionnellement, permet en amont, de prévenir cette complication rare mais grave.
Différents glaucomes peuvent apparaître après les traumatismes du SA. Outre les hypertonies oculaires immédiates déjà vues, une hypertonie oculaire séquellaire peut persister, traduisant les séquelles trabéculaires du traumatisme initial. Déchirure angulaire (récession), déchirure irienne, goniosynéchies, surcharges par cellules hématiques ou par protéines inflammatoires, débris de cristallin et présence de vitré sont autant de raisons pour développer une fibrose cicatricielle de l’angle iridocornéen qui rendra le traitement chirurgical difficile et souvent inefficace. La prévention de ces glaucomes passe par l’utilisation d’anti-inflammatoires très rapidement et la réalisation de chirurgie favorisant l’ouverture et le nettoyage angulaire.
Les opacités cornéennes séquellaires d’une plaie mal suturée ou à berges irrégulières (fig. 25-4) nécessitent la réalisation secondairement d’une greffe de cornée, avec parfois une chirurgie du cristallin associée. Chez l’enfant, il ne faut pas attendre trop longtemps après le traumatisme perforant pour supprimer cette cause majeure d’amblyopie organique.
L’amblyopie est la complication la plus spécifique de ces traumatismes du SA chez l’enfant. Elle nécessite une prise en charge la plus rapide possible et prolongée jusqu’à l’obtention du résultat optimal. Les parents doivent immédiatement être avertis de cette complication, qui apparaît même sur un œil ne présentant plus aucune séquelle, quelque mois après le traumatisme, chez un enfant de moins de 6 ans.
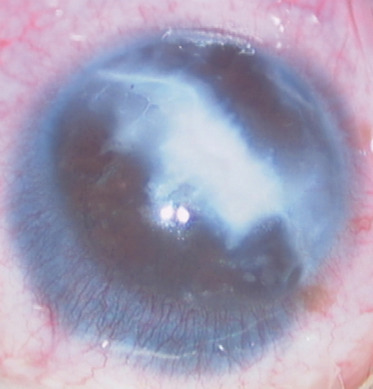
Fig. 25-4 Cicatrice opaque et vicieuse de plaie de cornée.
La meilleure prévention reste l’éducation des enfants et de leurs parents, qui doit commencer à l’école, en insistant sur les dangers domestiques. Des campagnes publiques de prévention des accidents auxquels sont exposés les enfants devraient avoir lieu. La protection des yeux lors de sports ou activités à risque oculaire doit devenir systématique et obligatoire. Certains jouets devraient être interdits (jeux de fléchette à bout métallique effilé, pétards, pistolets à grenaille, etc.) et d’autres soumis de façon plus drastique aux normes de sécurité. Enfin, les enfants ne devraient pas avoir accès aux armes et devraient être éloignés de situation à risque, comme le jardinage avec tondeuse à gazon usagée (lame en acier rouillée se délitant en morceaux), le bricolage (avec utilisation de clous, marteau, perceuse, etc.) et la chasse. Cependant, il sera toujours difficile de lutter contre l’absence de surveillance, voire la négligence des parents.
Un certificat descriptif des lésions doit être remis aux parents lors d’accidents scolaires ou de rixe, ou lors d’un traumatisme commis par un tiers sur l’enfant. Il doit rapporter les données objectives ainsi que les dires de l’enfant et des parents sans se les approprier. L’éventualité des complications et des séquelles doit être mentionnée sur ce certificat.
Enfin, toute suspicion de sévices doit nous inciter à hospitaliser l’enfant et faire intervenir un pédopsychiatre en même temps qu’un bilan lésionnel général est réalisé.
[1] Abbott J, Shah P. The epidemiology and etiology of pediatric ocular trauma. Surv Ophthalmol 2013 : 58 : 476-85.
[2] Mayouego Kouam J, Epee E, Azria S, et al. Aspects épidémiologiques cliniques et thérapeutiques des traumatismes oculaires de l’enfant dans un service d’urgences ophtalmologiques en Ile-de-France. J Fr Ophtalmol 2015 ; 38 : 743-51.
[3] Brophy M, Sinclair SA, Hosteltler SG, Xiang H. Pediatric eye injury-related hospitalizations in the United States. Pediatrics 2006 ; 117 : e1263-7.
[4] Mowatt L, Mac Donald A, Ferron-Boothe D. Paediatric ocular trauma admission to the University Hospital of the West Indies 2000–2005. West Indian Med J 2012 ; 61 : 599-640.
[5] Khatry SK. The epidemiology of ocular trauma in rural Nepal. Br J Ophthalmol 2004 ; 129 : 639-42.
[6] May DR, Kuhn FP, Morris RE, et al. The epidemiology of serious eye injuries from the United States Eye Injury Registry. Graefes Arch Clin Exp Ophthalmol 2000 ; 238 : 153-7.
[7] Moren Cross J, Griffin R, Owsley C, et al. Pediatric eye injuries related to consumer products in the United States. J AAPOS 2008 ; 12 : 626-8.
[8] Serrano JC, Chalela P, Arias JD. Epidemiology of childhood ocular trauma in a northeaster, Colombian region. Arch Ophthalmol 2003 ; 121 : 1439-45.
[9] Hargrave S, Weakley D, Wilson C. Complications of ocular paintball injuries in children. J Pediatr Ophthalmol Strabismus 2000 ; 37 : 338-43.
[10] Pearlman JA, Au Eong KG, Kuhn F, et al. Airbags and eye injuries : epidemiology, spectrum of injury, and analysis of risk factors. Surv Ophthalmol 2001 ; 46 : 234-42.
[11] Patton N. Self-inflicted eye injuries : a review. Eye 2004 ; 18 : 867-72.
[12] Lareg MM, Nielssen OB. Self-enucleation : forget Freud and Oedipus, it’s all about untreated psychosis. Br J Ophthalmol 2012 ; 96 : 1056-7.
[13] Kivlin JD, Simons KB, Lazoritz S, et al. Shaken baby syndrome. Ophthalmology 2000 ; 107 : 1246-54.
[14] Calzada JI, Kerr NC. Traumatic hyphemas in children secondary to corporal punishment with a belt. Am J Ophthalmol 2003 ; 135 : 719-20.
[15] Burillon C, Cornut PL, Janin-Manificat H. Traumatisme du segment antérieur de l’oeil. Encycl Méd Chir (Elsevier, Paris). Ophtalmologie, 21-700-A-10. 2008.
[16] Maia Rocha C, Nogueira Martins E, Melo LAS, Simeren Bueno de Moraes N. Outpatient management of traumatic hyphema in children : prospective evaluation. J AAPOS 2004 ; 8 : 357-61.
[17] Levecq L, Francart D, Van Hollebeke I. Ruptures de la membrane de Descemet après utilisation de forceps : aspects cliniques et en tomographie à cohérence optique. J Fr Ophtalmol 2014 ; 37 : 173-5.
[18] Gupta A, Rahman I, Leatherbarrow B. Open globe injuries in children : factors predictive of a poor final visual acuity. Eye 2009 ; 23 : 621-5.
[19] Sminia ML, Odenthal MT, Wenniger-Prick LJ. Traumatic pediatric cataract : a decade of follow-up after Artisan aphakia intraocular lens implantation. J AAPOS 2007 ; 11 : 555-8.
[20] Sminia ML, Odenthal MT, Gortzak-Moorstein N. Implantation of the Artisan iris reconstruction intraocular lens in 5 children with aphakia and partial aniridia caused by perforating ocular trauma. J AAPOS 2008 ; 12 : 268-72.
[21] Beby F, Kodjikian L, Roche O, et al. Traumatismes oculaires perforants de l’enfant. J Fr Ophtalmol 2006 ; 29 : 20-3.
P. Dureau, F. Metge-Galatoire, G. Caputo
Parmi les traumatismes pouvant toucher l’œil de l’enfant, ceux qui intéressent le segment postérieur (SP) sont les plus pourvoyeurs de mauvais résultat visuel en raison des lésions rétiniennes souvent irréversibles. Plusieurs caractéristiques sont communes à ces yeux en développement :
la brièveté de la pars plana avant l’âge de 3-4 ans, qui oblige à un positionnement plus antérieur des orifices de sclérotomie en cas de vitrectomie;
le caractère cohérent, non liquéfié du vitré et la hyaloïde postérieure non décollée. Ces caractéristiques impliquent une résorption plus lente des hémorragies intravitréennes, des tractions vitréorétiniennes plus importantes et une chirurgie plus difficile;
le fréquent retard au diagnostic et à la prise en charge, entraînant une prolifération vitréorétinienne.
Comme dans toutes les affections ophtalmopédiatriques, l’amblyopie conditionne souvent le pronostic visuel, même en cas de bon résultat anatomique.
II existe une surreprésentation des enfants dans les traumatismes oculaires [1], vraisemblablement multifactorielle : moindre conscience du danger, jeux, petite taille mettant l’œil à la hauteur de nombreux agents vulnérants, etc. Comme dans tous les traumatismes, les garçons sont le plus fréquemment touchés.
Les circonstances du traumatisme, importantes à connaître pour avoir une idée des lésions potentielles, sont les accidents domestiques, les jeux, les sports. Un cas particulier est celui des traumatismes auto-infligés (automutilation) chez des enfants souffrant d’un retard ou d’une maladie mentale.
Les traumatismes à globe ouvert représentent environ la moitié des cas des traumatismes oculaires de l’enfant, et probablement plus en cas d’atteinte du SP.
Il faut distinguer les traumatismes à globe fermé (contusions) de ceux à globe ouvert. La classification des traumatismes oculaires à globe ouvert habituellement utilisée pour décrire ce groupe hétérogène de lésions est celle de Birmingham [2]. Elle distingue :
les traumatismes pénétrants (une porte d’entrée, c’est-à-dire une plaie);
les traumatismes perforants (une porte d’entrée et une porte de sortie);
les traumatismes avec CE intra-oculaire;
les éclatements du globe.
Cette classification a une valeur pronostique.
Comme chez l’adulte, le principe de la prise en charge en urgence est de fermer la plaie et de traiter les lésions associées secondairement.
L’interrogatoire de l’enfant et des parents permet généralement (mais pas toujours) de préciser les circonstances de l’accident et l’agent vulnérant, donnant une idée des lésions à rechercher.
Quand l’âge de l’enfant et les lésions le permettent, l’examen doit être le plus complet possible (valeur médico-légale) : mesure de l’acuité visuelle, oculomotricité intrinsèque et extrinsèque, examen du SA, FO. Un scanner orbitaire peut révéler les lésions osseuses associées ou un CE intra-oculaire. L’échographie (fig. 25-5) doit être maniée avec prudence en cas de suspicion de plaie du globe.
Chez l’enfant, l’examen en consultation éveillée n’est pas toujours facile et il faut éviter de forcer l’ouverture palpébrale pour ne pas aggraver l’issue de tissus intra-oculaires. Il est préférable de faire d’emblée un examen sous anesthésie générale qui sera associé si nécessaire au premier geste chirurgical.
Une antibioprophylaxie parentérale est indispensable dans les plaies du globe chez l’enfant, en évitant l’utilisation des fluoroquinolones. Les antibiotiques habituellement utilisés sont l’imipe-nème (Tienam®) ou la ceftazidime (Fortum®) associés ou non à de la fosfomycine. Une corticothérapie générale est souvent associée au traitement local en raison de la réaction inflammatoire plus importante chez l’enfant.
En cas de plaie, le principe est la suture la plus soigneuse possible en urgence. Des points séparés de Nylon 10/0 de pleine épaisseur sont plus simples à réaliser et assurent une meilleure étanchéité de la cornée. La sclère peut éventuellement être suturée au Vicryl®. Les prolongements très postérieurs doivent parfois être laissés non suturés, le risque de la manipulation du globe étant supérieur au bénéfice de la suture. Les hernies de tissu intra-oculaire doivent être réséquées avec parcimonie : nettoyage du vitré au vitréotome, réintégration autant que possible de la choroïde, de l’iris, de la rétine. Parfois, si la capsule cristallinienne est ouverte avec issue de masses, l’aspiration du contenu cristallinien et le nettoyage des capsules évitent l’apparition rapide d’une inflammation et d’une intumescence.
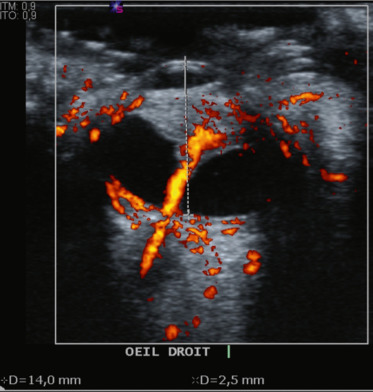
Fig. 25-5 Décollement de rétine total objectivé par l’échographie. Le Doppler montre les vaisseaux centraux. (Remerciements au Dr O. Bergès.)
L’hémorragie intravitréenne est rarement secondaire à une contusion du globe, mais est le plus souvent due à la plaie elle-même, atteignant diversement l’iris, le corps ciliaire ou les vaisseaux rétiniens. Sa principale caractéristique est sa lenteur de résorption en raison du caractère cohérent et non décollé du vitré et le risque d’organisation secondaire. Le plus souvent, le vitré ne se décolle pas dans les jours qui suivent la constitution de l’hémorragie, et il existe donc un risque de tractions et de DR. Ces risques sont en faveur d’une vitrectomie précoce devant toute hémorragie intravitréenne dans un contexte de plaie. Celle-ci masque en effet souvent un point d’impact rétinien susceptible de s’organiser et d’occasionner un DR secondaire. Par ailleurs, la persistance prolongée d’une hémorragie intravitréenne expose au risque d’amblyopie chez les enfants les plus jeunes. Ces risques sont en faveur d’une vitrectomie précoce si l’hémorragie est dense.
Parfois massifs, les hématomes choroïdiens doivent faire retarder une éventuelle vitrectomie. Leur résorption peut favoriser des tractions au sein du vitré préalablement comprimé et un DR tractionnel secondaire.
La rétinopathie contusive (ou œdème de Berlin ou commotio retinae) est secondaire à une contusion du globe. Elle se caractérise par un œdème blanc siégeant au niveau de la rétine externe [3]. Cet œdème n’est pas visible en OCT (fig. 25-6). Le retentissement visuel est variable selon le siège de l’atteinte. Un trou maculaire secondaire peut se former. Il n’y a pas de traitement spécifique.
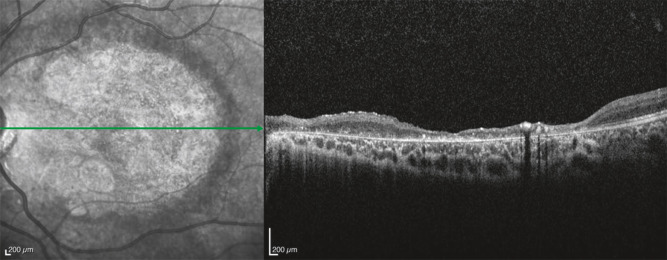
Fig. 25-6 Contusion du pôle postérieur : oedème blanc peu visible en OCT.
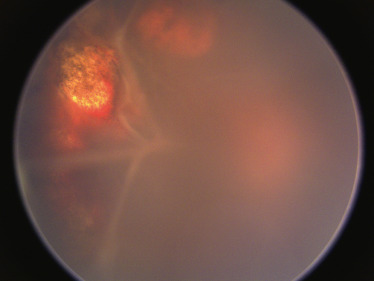
Fig. 25-7 Décollement de rétine à partir des bords d’une grande déchirure au niveau d’un point d’impact rétinien.
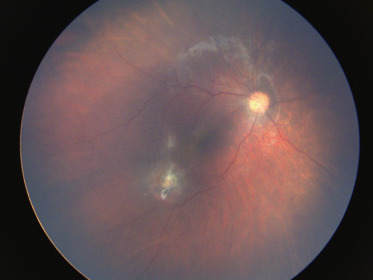
Fig. 25-8 Point d’impact maculaire avec membrane épirétinienne secondaire.
Un trou maculaire peut compliquer la rétinopathie contusive, en raison de la fragilisation de la rétine maculaire œdématiée et des tractions vitréorétinennes tangentielles. Les traumatismes sont la première cause de trou maculaire chez l’enfant. Les trous maculaires post-contusifs peuvent se fermer spontanément dans plus de 30 % des cas, c’est pourquoi une chirurgie n’est envisagée qu’après un délai de 3 mois suivant le traumatisme initial. Cette chirurgie est plus délicate que chez l’adulte en raison du caractère cohérent du vitré et de la difficulté à décoller la hyaloïde postérieure. De plus, le positionnement éventuel après chirurgie et utilisation de gaz n’est pas toujours possible chez l’enfant
Les ruptures choroïdiennes sont souvent secondaires à une contusion violente. Elles peuvent être masquées au début par une hémorragie intravitréenne et/ou un DR. Leur localisation est volontiers maculaire avec un risque de conséquences visuelles. Histologiquement, elles se situent au niveau de la choroïde interne et de l’épithélium pigmentaire. Elles apparaissent comme des lignes irrégulières, blanches et/ou pigmentées. Il existe un risque de néovascularisation secondaire, parfois accessible à une photocoagulation ou des injections intravitréennes d’anti-vascular endothelial growth factor (anti-VEGF).
Les décollements de rétine de l’enfant sont, dans la moitié des cas, d’origine traumatique. Les mécanismes possibles à l’origine du décollement sont :
en cas de plaie perforante :
déchirure rétinienne en regard d’une plaie pénétrante, avec ou sans CE intra-oculaire (fig. 25-7);
point d’impact rétinien de CE (intra-oculaire ou entré et sorti de l’œil) avec hémorragie intravitréenne qui, en s’organisant, est constamment à l’origine d’une traction (fig. 25-8);
incarcération de vitré dans une plaie postérieure et traction secondaire;
dans ces trois cas, une vitrectomie précoce limite le risque de décollement secondaire.
en cas de contusion : dialyse à l’ora, le plus souvent temporale inférieure.
La prise en charge chirurgicale privilégie la chirurgie ab externo, en particulier le cerclage, en raison du caractère cohérent du vitré favorisant les tractions. Chez les enfants les plus petits, ce cerclage doit être coupé après quelques mois pour ne pas entraver la croissance du globe. Mais en cas de prolifération vitréorétinienne de stade C, de déchirures multiples, de déchirure géante, d’hémorragie intravitréenne, une vitrectomie est nécessaire [4].
Ces plaies doivent être suturées d’emblée le plus soigneusement possible (voir plus haut). L’incarcération de vitré et de rétine dans la plaie comporte un risque élevé de décollement, d’emblée ou secondairement.
En cas de CE intra-oculaire, l’extraction se fait en général secondairement mais de façon précoce au cours d’une vitrectomie. L’antibioprophylaxie est primordiale, particulièrement en cas de CE végétal. La conservation du cristallin n’est pas toujours possible.
En cas d’éclatement du globe, la suture initiale vise à rendre la meilleure étanchéité possible et à nettoyer soigneusement tous les débris uvéaux, source d’inflammation et d’ophtalmie sympathique.
Ces neuropathies peuvent résulter de plusieurs mécanismes :
avulsion du nerf optique, avec une absence ou un recul de la papille si le FO est visualisable;
neuropathie optique ischémique par occlusion des artères ciliaires antérieures;
hématome rétrobulbaire;
cisaillement du nerf optique;
section ou blessure dans un foyer de fracture.
La baisse profonde de vision, le déficit pupillaire afférent, le scanner et l’IRM sont les éléments clés du diagnostic. La corticothérapie générale n’améliore que rarement un pronostic très défavorable.
Le suivi est généralement prolongé avec des contrôles répétés sous anesthésie générale pour ablation des fils, traitement des lésions secondaires (cataracte, décollement, CE, etc.), mesure du tonus oculaire, examen du FO, réfraction, etc. Dès que les lésions sont stabilisées, si l’axe visuel est dégagé et la macula saine, la correction optique totale doit être prescrite et la rééducation d’amblyopie entreprise chez les enfants les plus petits.
Les complications les plus redoutables à distance du traumatisme sont le glaucome, souvent difficile à équilibrer même après chirurgie, et l’ophtalmie sympathique.
Les facteurs de mauvais pronostic sont le jeune âge, la mauvaise acuité visuelle initiale, les traumatismes par projectile, les plaies postérieures, les hémorragies intravitréennes, la nécessité d’une vitrectomie, le DR [5].
Environ un quart des nouveau-nés par voie basse présentent des hémorragies rétiniennes [6]. Celles-ci sont liées à la compression thoracique avec trouble du retour veineux lors de l’accouchement. Elles sont plus fréquentes en cas de travail prolongé et d’utilisation de forceps. Elles sont beaucoup plus rares après césarienne. Les hémorragies peuvent être pré-, intra- ou sous-rétiniennes. Elles disparaissent en 2 semaines au maximum. Leur persistance au-delà doit faire suspecter une maltraitance. Les autres traumatismes obstétricaux du SP sont exceptionnels et généralement secondaires au mauvais positionnement d’une cuiller de forceps.
Voir plus loin, chapitre 25.5.
La rétinopathie de Purtscher apparaît après un traumatisme thoracique grave, une embolie graisseuse ou aérienne. La région périmaculaire comporte des plages blanches correspondant à des zones ischémiques et/ou des exsudats, et des hémorragies. Il n’y a pas de traitement spécifique.
Les phototraumatismes peuvent être consécutifs à l’utilisation par l’enfant d’un pointeur laser. Les modèles en vente dans les circuits contrôlés sont d’une puissance limitée et peu dangereuse, mais il est facile de se procurer sur Internet ou auprès de vendeurs à la sauvette des lasers beaucoup plus puissants. Leurs effets sur la rétine sont des brÛlures, des ruptures de la membrane de Bruch éventuellement compliquées de néovascularisation, des zones atrophiques ou pigmentées. La localisation maculaire peut être à l’origine de baisses profondes de l’acuité visuelle.
Chez les enfants présentant un retard ou une maladie mentale, les comportements de coups auto-infligés sur les yeux peuvent être à l’origine d’un DR (fig. 25-9). En cas de cataracte totale dans ce contexte, il faut se méfier des fréquentes lésions associées du SP. L’absence de communication aggrave le retard diagnostique et la prise en charge. On peut en rapprocher le frottement des yeux chez les enfants atopiques favorisant les kératocônes et peut-être les DR.
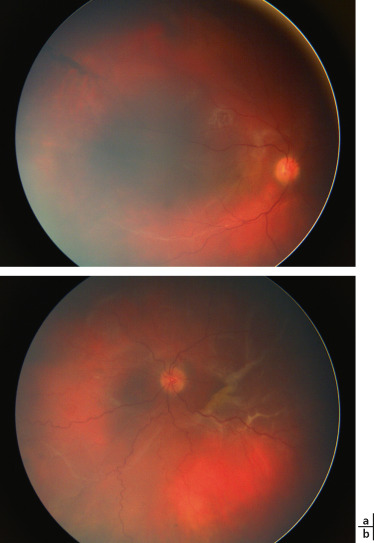
Fig. 25-9 Décollement de rétine bilatéral à progression lente (a : oeil droit ; b : oeil gauche) chez un enfant autiste avec comportement d’automutilation.
La prévention reste le principal traitement des traumatismes oculaires chez l’enfant. L’éviction des objets dangereux et les explications sur les risques sont essentielles. Chez un enfant ayant été victime d’un traumatisme sans atteinte postérieure, l’occlusion régulière de l’autre œil permettra de dépister précocement l’apparition d’un décollement secondaire. De même, chez les enfants ayant perdu un œil par maladie ou accident, toutes les activités comportant un risque de traumatisme de l’autre œil (sports de combat, sports violents type rugby, bricolage, etc.) sont à proscrire.
[1] Denion E. Spécificités des traumatismes oculaires chez l’enfant. In : Goberville M, Dureau P. Ophtalmologie pédiatrique et strabismes. Vol. 3. Paris : Lavoisier ; 2014, p. 98-105.
[2] Kuhn F, Morris R, Witherspoon CD, et al. A standardized classification of ocular trauma. Ophthalmology 1996 ; 103 : 240-3.
[3] Good WV. Accidental trauma in children. In : Taylor D, Hoyt CS. Pediatric ophthalmology and strabismus. London : Elsevier ; 2005, p. 754-68.
[4] Becquet F. Décollements de rétine rhegmatogènes de l’enfant. In : Goberville M, Dureau P. Ophtalmologie pédiatrique et strabismes. Vol. 3. Paris : Lavoisier ; 2014, p. 64-75.
[5] Liu X, Liu Z, Liu Y, et al. Determination of visual prognosis in children with open globe injuries. Eye 2014 ; 28 : 852-6.
[6] Watts P, Maguire S, Kwok T, et al. Newborn retinal hemorrhages : a systematic review. J AAPOS 2013 ; 17 : 70-8.
E. Bui Quoc, B. Fayet
E. B ui Quoc
La traumatologie orbitopalpébrale de l’enfant est vaste, les conditions traumatiques très variables : contusion, lacération, arrachement, présence d’un CE (inerte ou organique), caractère septique ou non, etc.
Le bilan évalue les lésions et les priorités thérapeutiques en cas de traumatisme orbitopalpébral : contexte neurochirurgical (qui prime), atteinte oculaire, atteinte palpébrale, atteinte des voies lacrymales, atteinte des annexes, autres atteintes faciales, fractures orbitaires, etc. Ce bilan est clinique et paraclinique (imagerie), pouvant nécessiter une anesthésie chez un enfant.
Les principes thérapeutiques sont simples :
en urgence :
priorité au pronostic neurochirurgical selon le contexte en cas de traumatisme crânien sévère associé;
priorité à la réparation d’une plaie oculaire;
restauration anatomique des structures palpébrales, annexielles, lacrymales et traitement d’une éventuelle fracture associée.
à moyen terme : préservation fonctionnelle de la vision, de la statique palpébrale, de la fonction lacrymale, de la fonction oculomotrice;
à long terme : traitement à distance des éventuelles séquelles.
Les données épidémiologiques sur la traumatologie orbitopalpébrale chez l’enfant sont très peu nombreuses, et il est difficile de préciser l’incidence et la prévalence de cette pathologie.
Quelques articles évoquent des données parcellaires dans des populations particulières, mais pas spécifiquement pédiatriques, dont l’intérêt est de souligner les circonstances de traumatisme, afin de développer des moyens de prévention ou d’amélioration des circuits de prise en charge en cas de mise en évidence de retard thérapeutique.
Par exemple, Khan [1] décrit la fréquence des antécédents de traumatisme oculaire chez 8283 sujets bengalais (enfants et adultes) de zones rurales, mettant en évidence que 167 d’entre eux, soit 2 % , auraient déjà eu un antécédent de traumatisme oculaire, soit une incidence annuelle de 6,2/1000. On note une majorité d’hommes (sex-ratio de 4:5), et une moyenne d’âge au premier traumatisme de 20 ans. Quarante pour cent des traumatismes sont causés par un instrument non tranchant, 22 % par un objet pénétrant, 18 % par un instrument pointu. La maison est majoritairement le lieu du traumatisme (55 % ). Le traumatisme concerne la paupière dans 15 % des cas, la conjonctive dans 11 % des cas, la cornée dans 10 % des cas. Le délai avant traitement est très long : 5 jours pour une prise en charge médicale, 18 jours pour une prise en charge ophtalmologique. Un traumatisme sur seize conduit à la cécité.
En Centrafrique, une étude prospective a montré que sur une période de 3 ans, 194 traumatismes oculaires chez des enfants de 0 à 15 ans avait été relevés [2]. On retrouve 191 cas unilatéraux et 3 cas bilatéraux soit 197 yeux. Une majorité de garçons est retrouvée (59 % ), soit un sex-ratio de 1,3. À noter que les causes traumatiques sont très majoritairement évitables, puisqu’on relève 18,8 % de bagarres, 19,3 % de jeux et 25,9 % de traumatismes oculaires secondaires à des punitions infligées, etc. Autre fait notable, montrant que la cécité, la malvoyance ou les séquelles dues au traumatisme demeurent évitables, est que le retard de prise en charge demeure : 2 % de prise en charge dans les 6 heures, mais 44,7 % de prise en charge entre 48 heures et 1 semaine. La majorité des cas a consisté en un mécanisme traumatique contusif. Il était noté 15 cas de plaie palpébrale avec ou sans atteinte des voies lacrymales (7,6 % ), le reste des contusions conduisant à 25 cas d’hyphéma (12,7 % ), 19 cas de plaie conjonctivale (9,6 % ), 18 cas de cataracte traumatique (9,4 % ), 19 cas d’ectopie acquise/luxation du cristallin (9,6 % ). Très souvent, les atteintes peuvent être associées entre elles. Les plaies transfixiantes de cornée représentaient 19,8 % des cas et les ruptures du globe 4,5 % . Ainsi, cet article montre bien que les traumatismes palpébraux sont minoritaires par rapport aux traumatismes oculaires purs, même s’ils peuvent être associés, mais surtout que les causes sont évitables.
Autre cause évitable de traumatisme oculaire et orbitopalpébral, les tirs de balle en caoutchouc : une étude de 2003 [3] a rapporté sur une population jeune (moyenne 25 ans; 4 à 60 ans) 42 cas de traumatismes vus sur une période de 3 mois, avec suivi d’au moins 6 mois, et encore une fois une grande majorité de garçons (90 % ). Dans cette cohorte, on a retrouvé une majorité d’atteinte cutanée ou palpébrale (54 % ), avec dans 21 % des cas la balle toujours logée dans l’orbite et dans 33 % des cas une fracture orbitaire associée. Les autres atteintes oculaires associées représentaient, par ordre de fréquence : 40 % d’hyphéma, 38 % de rupture du globe et 26 % d’atteinte rétinienne. Cette traumatologie est très sévère : à la fin du suivi, on note une majorité de patients ayant une vision de moins de 1/10 (53 % ), et seulement 40 % ont plus de 3/10 (6/18 précisément). Cette étude montre que ce type de traumatisme par balle ne lèse pas que l’œil mais aussi le cadre osseux, les tissus « mous » intra-orbitaires et les paupières.
Le bilan lésionnel clinique et paraclinique en cas de traumatisme orbitopalpébral chez l’enfant doit être complet, précis, raisonné, systématique; il porte sur : le cadre osseux, l’enveloppe cutanée et palpébrale, le contenant « mou » oculaire/orbitaire. L’examen étant parfois malaisé chez un enfant traumatisé, la sédation est le plus souvent requise. Dans tous les cas, le bilan lésionnel est renouvelé sous anesthésie générale en préopératoire immédiat.
L’ordre des priorités est à échelonner : parfois le pronostic vital peut être engagé (contexte neurochirurgical, nécessité d’une imagerie rapide à la recherche d’un hématome sous-dural ou d’un hématome extradural, lésions cardiothoraciques, etc.). Le pronostic visuel peut être en jeu à court ou long terme selon le type de lésions pouvant être traité ou pas (plaie oculaire, DR, compression du nerf optique hémorragique ou arrachement, etc.). Il en est de même pour le pronostic de la statique palpébrale, de la fonction lacrymale et de l’esthétique.
Le contexte traumatique peut être contusif, perforant, mixte, localisé ou plus ou moins étendu à l’orbite et aux voies lacrymales, avec ou sans CE.
Parfois, il peut être curieux et inattendu, ainsi cet enfant courant dans la cour de récréation avec un pinceau, chutant avec son pinceau entrant dans sa narine, sortant du cartilage à proximité du sac lacrymal et se plantant dans la paupière supérieure, avec épargne ( « miraculeuse » ?) de toute structure « noble » , et la situation se résolvant par de simples sutures cutanées et palpébrales (fig. 25-10).
Le contexte de morsure par des chiens chez l’enfant est propice à des lésions annexielles et des voies lacrymales. Gonnering rapporte par exemple 16 cas dont deux tiers de moins de 10 ans et la moitié de moins de 5 ans [4]. Ces traumatismes sont aussi pourvoyeurs de lésions multiples superficielles, profondes et osseuses.
Parfois, il ne faut pas oublier une possible maltraitance, et on note dans l’article de Yaya et al. [2] une proportion non négligeable de traumatismes secondaires à des punitions, etc.
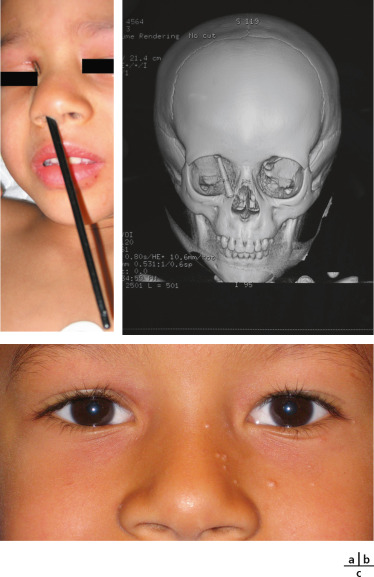
Fig. 25-10 a-c. Traumatisme à corps étranger
Les plaies sont extrêmement variables, avec perte de substance possible (fig. 25-11a) et atteinte du bord libre (fig. 25-11b). L’atteinte des voies lacrymales est à rechercher et à traiter (Fig. 25-11) (voir article spécifique suivant).
Une étude bavaroise de 2001 [5] relève les données cliniques de 180 patients présentant une atteinte orbitopalpébrale pris en charge entre 1997 et 1999, dont 22 enfants de moins de 20 ans. Le traumatisme était contusif dans 140 cas, avec 66 cas du fait d’un travail manuel, 38 cas de chutes, 23 cas secondaires à des violences physiques, 7 cas d’accident automobile ou de deux roues, et 6 cas ayant une cause sportive. Sur le plan anatomique, la plaie était supérieure dans 85 cas, inférieure dans 55 cas et mixte dans 40 cas, avec 43 plaies du bord libre (24 % ) et 28 plaies des voies lacrymales d’excrétion (16 % ). Les plaies étaient septiques dans 24 cas, avec CE dans 19 cas et perte de substance dans 13 cas. L’atteinte palpébrale était associée à une atteinte faciale dans 16 cas, une atteinte superficielle de l’œil dans 31 cas, un traumatisme contusif dans 36 cas, un traumatisme perforant dans 12 cas, une fracture dans 4 cas.
Les fractures du plancher sont évocatrices cliniquement, avec limitation de l’élévation et de l’abaissement de l’œil, témoignant d’une incarcération musculaire nécessitant une intervention chirurgicale (fig. 25-12). En cas de contusion oculaire, une fracture de la lame papyracée (mur interne et antérieur de l’orbite) peut être suspectée par une épistaxis et un emphysème sous-cutané palpébral.
Une classification des fractures orbitaires de l’enfant a été proposée par Losee et al. [6] :
type 1 : fractures purement orbitaires ne requérant pas de chirurgie en l’absence d’énophtalmie aiguë, de dystopie orbitaire verticale, d’incarcération musculaire;
type 2 : fractures complexes craniofaciales requérant une analyse radiologique précise pour proposer le traitement maxillofacial et/ou neurochirurgical approprié;
type 3 : fractures osseuses du cadre requérant une chirurgie.
Selon le mécanisme traumatique, il faut avoir le souci constant de la recherche CE, qui se fera de façon clinique et au moyen de l’imagerie en pré- et peropératoire. Il faut se souvenir que le scanner peut passer à côté d’un CE visible uniquement par l’échographie ou l’IRM.
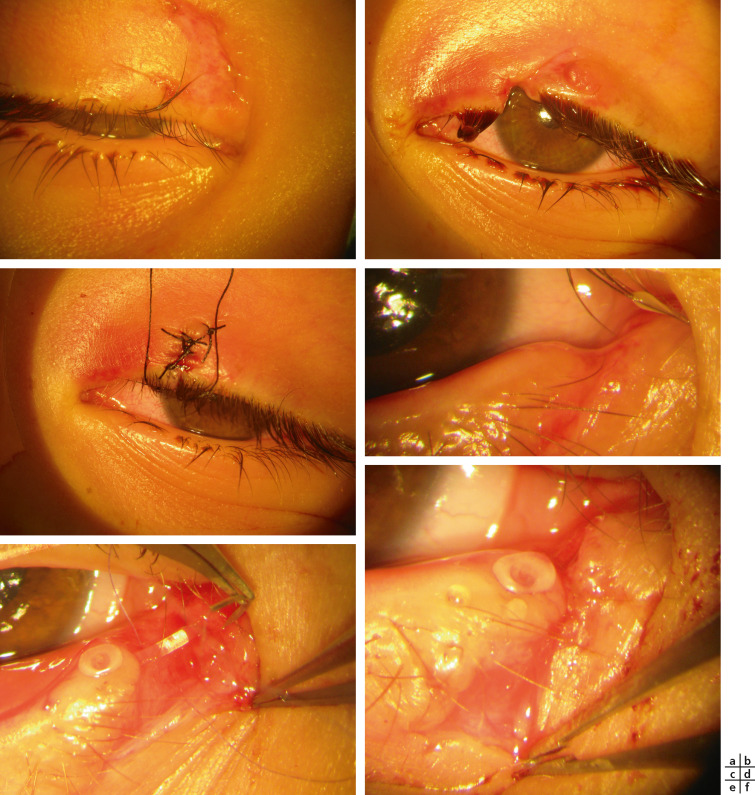
Fig. 25-11 Plaies. a. Palpébrale avec perte de substance. b, c. Du bord libre. d-f. De la voie lacrymale.

Fig. 25-12 Fracture du plancher de l’orbite droite : limitation de l’élévation et de l’abaissement (a-c) et scanner (d-f).
L’imagerie permet la mise en évidence d’un CE, mais également d’une fracture du cadre osseux. Une fracture du toit peut ne pas avoir de conséquence clinique immédiate et n’être diagnostiquée que par l’imagerie, par exemple dans ce cas de chute sur la voie publique en skateboard avec abrasions cutanées majeures et fracture du toit de l’orbite (fig. 25-13). Ces fractures du toit peuvent être isolées et ne sont pas exceptionnelles chez le petit enfant, comme le montre cette série américaine de 36 cas chez 32 enfants, sur 5 ans, où on note 16 cas isolés et 20 cas associés à un dégât crânien plus important [7]. Les cas isolés surviennent chez des enfants d’âge moyen de 2,8 ans, après un traumatisme relativement mineur, de moins de 3 mètres environ (10 pieds); elles ne requièrent pas toujours de traitement neurochirurgical en l’absence de déplacement d’une esquille osseuse dans le lobe frontal.
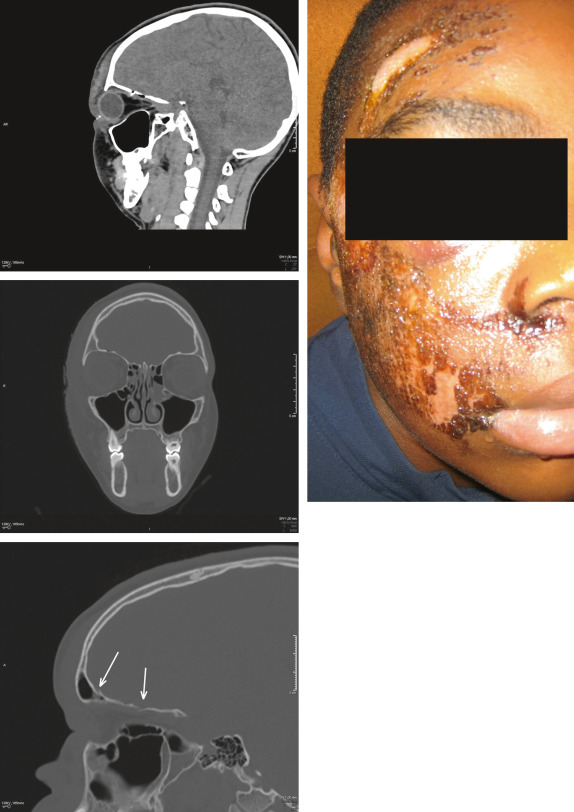
Fig. 25-13 Fracture du toit de l’orbite droite.
La thérapeutique reprend l’ordre de priorité : pronostic vital neurochirurgical, cardiothoracique dans un contexte multitraumatique; pronostic anatomique et fonctionnel de l’œil et des annexes; pronostic esthétique [8, 9, 10].
D’emblée, quelques questions sont à poser portant sur :
le vaccin antitétanique : il faut se méfier des modes antivaccinales et de l’inconscience de certains parents voire de soignants, etc.;
le risque rabique en cas de morsure de chien : c’est rare en France, mais il faut savoir y penser car le traumatisme a pu avoir lieu à l’étranger;
le risque infectieux en cas de plaie souillée : cela requiert un nettoyage rapide, une antibiothérapie préventive, une éventuelle chirurgie de parage. Les morsures de chiens sont pourvoyeuses d’infections spécifiques à bacilles à Gram négatif et sont à traiter avec l’avis d’un spécialiste en infectiologie [6].
Concernant la chirurgie prioritaire des traumatismes du SA et du SP, le lecteur peut se référer aux chapitres 25.1 et 25.2. Quant à la prise en charge des traumatismes des voies lacrymales d’excrétion, elle est traitée ci-après.
Les principes thérapeutiques en chirurgie orbitopalpébrale traumatique chez l’enfant sont :
sous anesthésie générale : confirmer le bilan lésionnel, rechercher un CE;
procéder à l’ablation des tissus nécrosés;
suturer plan par plan : muscles, tissu sous-cutané, tissu cutané; sutures sans tension; si besoin procéder par cicatrisation dirigée, voire greffe/lambeau;
préserver la statique palpébrale, avec mise en continuité de la paupière en cas de plaie du bord libre : un repère et la ligne grise qui doit être affrontée soigneusement;
traiter une fracture osseuse, avec ou sans l’aide d’une équipe maxillofaciale; en urgence différée, la désincarcération musculaire d’un droit inférieur permet la restauration immédiate (fig. 25-14) et à long terme (fig. 25-14) de la fonction d’élévation; les éventuelles séquelles oculomotrices sont traitées ultérieurement s’il existe une déviation résiduelle;
préserver l’esthétique avec des sutures cutanées soigneuses. La question des sutures pose le choix du type de fils à employer, qui doit tenir compte de la cicatrisation et des questions esthétiques propres à l’enfant :
du Vicryl® 6/0 ou 7/0 peut être employé pour le tarse, les plans musculaires orbiculaire et releveur de la paupière supérieure;
la soie 6/0 est la meilleure option; le Prolene® ou l’Ethilon® 6/0 peuvent être également utilisés, tous non résorbables, ce qui requiert une ablation des fils à distance parfois malaisée chez l’enfant;
exceptionnellement, du fil résorbable de Monocryl® 6/0 incolore, par exemple, est une option mais la réaction inflammatoire peut être majorée.
La suture peut se faire par points séparés ou par surjet intradermique.
Dans tous les cas, la cicatrice est protégée, par exemple, par des SteriStrips® et de l’exposition solaire.
Une précision concernant une plaie du bord libre : la ligne grise affrontée bord à bord est suturée à la soie 6/0, à enlever après 1 à 2 semaines.
On peut citer pour exemple la prise en charge rapportée dans l’étude bavaroise [5], où il existe une très grande rapidité de la prise en charge (temps moyen de 3,3 heures entre le traumatisme et la chirurgie), et dans laquelle il y a eu nécessité de recourir à : une suture cutanée simple (100 cas); des sutures cutanée et profonde concernant l’orbiculaire ou le releveur de la paupière supérieure (26 cas); une plastie de la marge palpébrale (43 cas); une suture du système lacrymal (24 cas), la fonction lacrymale requérant la continuité des voies lacrymales d’excrétion et une statique palpébrale satisfaisante. La prise en charge rapide dans cette étude explique qu’il n’y a eu qu’un cas de nécrose postopératoire et qu’un cas d’infection.

Fig. 25-14 Fracture du plancher de l’orbite droite : restauration de l’élévation et de l’abaissement à court (a-c) et long (d-f) terme.
La traumatologie orbitopalpébrale de l’enfant est multiple, avec des associations lésionnelles oculaires, osseuses, des voies lacrymales fréquentes. Le bilan minutieux et hiérarchisé est clinique et paraclinique, afin de vérifier l’intégrité ou l’atteinte de chacune des structures du contenant et du contenu de l’orbite. Le traitement chirurgical est urgent, conditionnant le pronostic anatomique, fonctionnel et esthétique.
[1] Khan AK. Ocular injury : prevalence in different rural population of Bangladesh. Bangladesh Med Res Counc Bull 2013 ; 39 : 130-8.
[2] Yaya G, Bobossi Serengbe G, Gaudeuille A. Les traumatismes oculaires chez les enfants âgés de 0 à 15 ans. Aspects épidémiologiques et cliniques au Centre national hospitalier universitaire de Bangui. J Fr Ophtalmol 2005 ; 28 : 708-12.
[3] Lavy T, Asleh SA. Ocular rubber bullet injuries. Eye (Lond) 2003 ; 17 : 821-4.
[4] Gonnering RS. Ocular adnexal injury and complications in orbital dog bites. Ophthal Plast Reconstr Surg 1987 ; 3 : 231-5.
[5] Herzum H, Holle P, Hintschich C. Lidverletzungen. Epidemiologische Aspekte. Ophthalmologe 2001 ; 98 : 1079-82.
[6] Losee JE, Afifi A, Jiang S, et al. Pediatric orbital fractures : classification, management, and early follow-up. Plast Reconstr Surg 2008 ; 122 : 886-97.
[7] Greenwald MJ, Boston D, Pensler JM, Radkowski MA. Orbital roof fractures in childhood. Ophthalmology 1989 ; 96 : 491-6 ; discussion 496-7.
[8] Murchison AP, Bilyk JR. Management of eyelid injuries. Facial Plast Surg 2010 ; 26 : 464-81.
[9] Lipke KJ, Gümbel HO. Management of injuries of the eye and its adnexa. Facial Plast Surg 2013 ; 29 : 310-5.
B. Fayet, E. Racy
Les principales étiologies des traumatismes des voies lacrymales sont les morsures canines et la traumatologie accidentelle (chutes, accidents de la voie publique).
Les lésions du segment horizontal des voies lacrymales sont plus fréquentes que les lésions du segment vertical.
La traumatologie du segment vertical des voies lacrymales (sac lacrymonasal et canal lacrymonasal) est plus rare et complique une contusion faciale directe, très violente, avec une dislocation des structures osseuses avoisinantes.
La pathologie traumatique des voies lacrymales d’excrétion est une pathologie rare. La problématique de la prise en charge a pour souci une restauration anatomique et fonctionnelle parfaite, avec également le souci de l’esthétique du regard et du visage.
La traumatologie lacrymale de l’enfant représente moins de 1 % des interventions pratiquées dans les centres d’urgence chirurgicale ophtalmologique.
La prédominance de l’atteinte des garçons est une constante dans les données épidémiologiques publiées (75 % ), avec une fréquence encore plus importante après chutes (82 % ).
Il existe une prédominance pour le côté gauche (60 % ) toutes étiologies confondues sauf en cas de morsure canine [1].
Trois circonstances principales sont responsables d’un traumatisme des voies lacrymales. Elles varient en fonction de l’âge de l’enfant :
en période néonatale, il s’agit d’une conséquence éventuelle de l’utilisation de forceps;
chez le petit enfant, il s’agit majoritairement des conséquences d’une chute ou de morsures canines. Il existe en France 1 cas de morsure grave pour 1000 chiens [2]. Elles sont, dans la majorité des cas, le fait d’un chien proche de la famille. Les données sont indicatives car il semble que de nombreux cas ne soient pas déclarés. Il est important de savoir si le chien est primo-mordant ou récidiviste. Il existe des procédures d’euthanasie contraignantes face à un animal dangereux;
chez le grand enfant, la traumatologie classique domine : chutes, accidents de la voie publique, accidents domestiques, etc.
L’atteinte isolée du canalicule inférieur domine nettement (60 % ) quels que soient l’âge, le côté atteint ou le sexe de l’enfant, etc. Les autres atteintes possibles sont par ordre de fréquence :
la section isolée du canalicule supérieur (18 % );
les plaies doubles (14 % );
les plaies du canalicule commun (8 % ).
Les plaies du méat sont exceptionnelles, comme les plaies bilatérales.
Cet ordre de fréquence est retrouvé dans toutes les séries publiées, et ce de façon indépendante de l’étiologie. Cela s’explique par l’anatomie orbitopalpébrale et les deux mécanismes possibles d’une lésion traumatique des voies lacrymales d’excrétion : la contusion et l’arrachement.
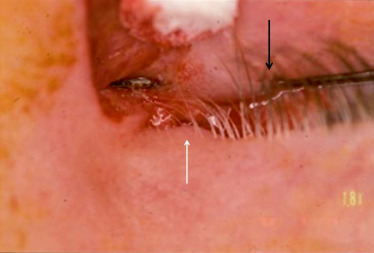
Fig. 25-15 Plaie de la voie lacrymale.
Les traumatismes directs des voies lacrymales entraînent des lésions avec ou sans systématisation, avec une protection relative des saillies osseuses frontales et nasales. Le canalicule inférieur demeure la partie la moins protégée, particulièrement dans son tiers externe à proximité du méat (voir Fig. 25-11). Les plaies du segment vertical des voies d’excrétion sont rares et sont la conséquence d’une contusion directe.
Les tractions palpébrales rompent la paupière au niveau sa plus grande faiblesse anatomique : entre le tarse en dehors et la bifurcation du tendon canthal médial en dedans. La plaie lacrymale est alors obligatoirement située à la jonction entre la portion externe et la portion moyenne du canalicule.
Chez l’enfant, l’association d’une plaie oculaire à une plaie lacrymale est rare avec une fréquence inférieure à 10 % [3, 4 ]. Aucune cause particulière n’est retrouvée à une association de ces plaies et aucune étiologie ne se détache, à l’inverse de l’adulte.
Notons que la première complication oculaire des forceps est les ruptures descemétiques, caractéristiques pas leur orientation parallèle au limbe; les plaies lacrymales sont possibles mais plus rares.
Le diagnostic d’une lésion du segment horizontal des voies lacrymales peut être évident lorsque la statique palpébrale médiocanthale est modifiée avec décalage anormal des méats lacrymaux homolatéraux. Une avulsion du canalicule commun de ses attaches sacculaires est à redouter devant un télécanthus associé à un arrondissement de l’angle de raccordement des paupières [5].
Le diagnostic d’une plaie des canalicules horizontaux est moins évident lorsque la statique palpébrale interne est intacte. L’exploration instrumentale prudente est indispensable devant toute plaie palpébrale passant en dedans du méat. Chez l’enfant, une anesthésie générale est souvent indispensable.
À distance d’un traumatisme, l’inspection peut retrouver une anomalie acquise de la position de la rivière lacrymale (ectropion, antéposition) ou une fistule canaliculaire.
Parfois, c’est l’exploration instrumentale qui fera le diagnostic. La sonde s’arrête en regard d’une cicatrice. L’anamnèse retrouvera le traumatise causal.
Au moment du traumatisme, une lésion du segment vertical des voies lacrymales est suspectée lorsqu’il existe une lésion ou une plaie en regard du sac lacrymal et par l’association d’une épistaxis et d’un emphysème sous-cutané [6], qui sont deux signes inconstants.
Un hématome médiocanthal important peut se compliquer de compression extrinsèque de la voie lacrymale verticale.
Une lésion du segment vertical des voies lacrymales est souvent présente dans un contexte traumatique violent, par exemple une morsure par un chien de grande taille, la canine du chien se plantant dans la gouttière lacrymale, tandis que le reste de la mâchoire prend son appui sur l’autre côté de la face. La répartition des plaies sur le visage, de part et d’autre du nez, doit faire soupçonner ce mécanisme.
Par ailleurs, les traumatismes balistiques du massif facial ainsi que la traumatologie lourde de type Lefort 1 (au niveau de la partie inférieure du canal lacrymonasal au niveau du cornet inférieur et de la paroi inter-sinuso-nasale), Lefort 2 (gouttière lacrymale), Lefort 3 et disjonction orbito-naso-ethmoïdo-frontale (DONEF) peuvent se compliquer d’une compression ou d’une section des voies lacrymales verticales non seulement au moment du traumatisme, mais également lors des efforts de reconstruction chirurgicale initiaux ou secondaires.
Non traitées, ces lésions du segment vertical se compliqueront de mucocèle du sac lacrymal, dont le développement se fait très rapidement après le traumatisme et parfois en quelques heures. Cette dacryocystite chronique ne présente pas de particularité clinique particulière par rapport aux étiologies non traumatiques.
Le traitement sera, sans urgence, une dacryocystorhinostomie [7].
Les principes thérapeutiques en traumatologie lacrymale de l’enfant ne sont pas fondamentalement différents de ceux de l’adulte. Le lecteur trouvera tous les détails dans les traités d’oculoplastique. Nous ne ferons que relater ici les points fondamentaux.
La traumatologie lacrymale n’est pas en soi une urgence thérapeutique immédiate. Différer une intervention de quelques heures pour réunir de bonnes conditions est souhaitable. Cependant, il ne faut pas dépasser un délai thérapeutique de 24 à 36 heures. En effet, avec le temps apparaissent de moins bonnes conditions locales, en particulier une possible nécrose tissulaire, ce qui augmentera la difficulté technique. Au-delà d’une prise en charge chirurgicale à 48 heures, le pronostic anatomique et fonctionnel peut s’aggraver significativement.
L’intervention de réparation chirurgicale peut devenir une urgence quasi immédiate, surtout en cas de lésions associées :
les pertes de substances palpébrales associées posent le problème particulier de la couverture cornéenne;
l’existence d’une plaie oculaire associée requiert en priorité le traitement de celle-ci;
les morsures canines posent un problème infectieux et esthétique. Elles nécessitent une gestion particulière.
Le choix de l’anesthésie dépend en grande partie des gestes qui doivent être effectués.
Le masque facial et la ventilation spontanée sont parfois compatibles avec l’examen oculaire, une suture simple, une intubation canaliculaire.
La protection laryngée (intubation avec ballonnet), est recommandée pour les chirurgies plus complexes et lorsqu’une intubation lacrymonasale poussée est indiquée. Un masque laryngé n’est pas toujours étanche avec risque en cas de saignement d’inondation bronchopulmonaire.
Sur le plan infectieux, il faut redouter dans tous les cas : la rage, le tétanos et les pasteurelloses. Une prise en charge spécifique est requise.
Les infections tissulaires secondaires sont d’autant plus rares que les plaies ont été bien irriguées avec de la Bétadine®, débridées voire drainées.
Il faut récupérer le carnet de vaccination du chien et déclarer en mairie ou dans un poste de police le cas de morsure.
Le chien doit être obligatoirement présenté à un vétérinaire pour une étude comportementale. L’euthanasie canine est parfois requise.
À distance, il faut anticiper les séquelles psycho-affectives et esthétiques qui peuvent être dramatiques.
La réparation palpébrale est capitale car de la bonne position de la rivière lacrymale dépend le premier temps du drainage lacrymal. Les impératifs de la réparation anatomique sont :
la continuité de la rivière lacrymale qui doit être au contact du globe;
le quasi-alignement vertical des méats lacrymaux;
l’arrondi des paupières qui doit suivre le globe oculaire sans antéposition.
Cette réparation palpébrale doit supporter toute la tension tissulaire qui ne peut être laissée ni au canalicule ni à l’intubation.
L’exploration au microscope permet de retrouver les deux fragments d’un canalicule sectionné, et il faut faire des sutures directes terminoterminales de ce canalicule, au monofilament de Nylon [8]. Les points transfixiants chargent toute l’épaisseur du canalicule avec un peu d’orbiculaire adjacent pour réaliser un affrontement terminoterminal sans tension. Le diamètre du fil de Nylon est 9/0 ou 8/0. Le nombre de points est variable selon les conditions locales : de 3 à 8, en pratique déterminé par l’affrontement des berges qui doit être parfait.
L’intubation est contre-indiquée dans les plaies méatique et juxtaméatique.
Elle est indiquée pour les plaies contuses :
on utilise une intubation par une sonde à fixation autostable type Mini-Monoka® [9] pour les sections monocanaliculaires des deux tiers externes du segment horizontal; l’intubation est laissée en place 2 mois environ;
une intubation bi-canaliculo-nasale est indiquée pour les autres localisations traumatiques des voies lacrymales. La durée de l’intubation est de 2 à 4 mois si l’exploration a été normale. Elle est prolongée à au moins 1 an, dans le cas contraire.
La plaie est suturée en trois plans (muqueux, orbiculaire et cutané). La suture de la face latérale du sac se fait à nœuds externes en restant dans l’épaisseur de la paroi muqueuse. Il existe un risque de synéchie si la plaie intéresse simultanément les deux parois du sac. Dans cette situation, associer une sonde Bika® est logique.
Points thérapeutiques essentiels
La prévention des plaies lacrymales impose des recommandations : généralisation du port de la ceinture de sécurité, nécessité d’éduquer le comportement des enfants vis-à-vis des chiens mais aussi, et plus encore, éduquer autant que faire se peut les propriétaires, etc.
La réparation palpébrale est capitale.
La réparation canaliculaire avec affrontement des berges canaliculaires se fait à l’aide de points transfixiants de Nylon 8/0 ou 9/0. L’absence de tension dans cette suture est indispensable et est assurée par les points péricanaliculaires du temps palpébral.
L’intubation lacrymale est facultative. Le choix de la méthode d’intubation est déterminé par le montage le plus simple à réaliser, et occasionnant le moins d’effets indésirables. L’intubation est contre-indiquée dans les plaies méatique et juxtaméatique. L’intubation est principalement indiquée pour les plaies contuses et anciennes. La mini-Monoka® est idéale pour les sections monocanaliculaires situées au tiers moyen. Pour les autres cas, l’intubation bi-canaliculo-nasale est préférable. La durée de l’intubation varie de 2 à 4 mois si l’exploration des voies lacrymales est normale, mais doit être plus prolongé dans le cas contraire.
Le seul traitement efficace de la mucocèle est la dacryocystorhinostomie qu’il faut en règle différer de 6 mois au minimum.
[1] Billson FA, Taylor HR, Hoyt CS. Trauma to the lacrimal system in children. Am J Ophthalmol 1978 ; 86 : 828-33.
[2] Gonnering RS. Ocular adnexal injury and complications in orbital dog bites. Ophthal Plast Reconstr Surg 1987 ; 3 : 231-5.
[3] Ducasse A, Valle D, Scholtes F, et al. Plaies palpébro-lacrymales de l’enfant. J Fr Ophtalmol 2009 ; 32 : 374-9.
[4] Sharma B, Gupta R, Anand R, Ingle R. Ocular manifestations of head injury and incidence of post-traumatic ocular motor nerve involvement in cases of head injury : a clinical review. Int Ophthalmol 2014 ; 34 : 893-900.
[5] Hurwitz JJ, Avram D, Kratky V. Avulsion of the canalicular system. Ophthalmic Surg 1989 ; 20 : 726-8.
[6] Morax S, Bernard JA. Chirurgie des voies lacrymales au cours des enfoncements et des dislocations orbito-nasales. Ann Chir Plast Esthet 1983 ; 28 : 307-13.
[7] Adenis JP, Mathon C, Lebraud P, Franco JL. La dacryocystorhinostomie. Étude rÉtrospective de 165cas. Indications. Technique. Résultats. Étude comparée de 25 cas traumatiques à 165 cas toutes étiologies confondues. J Fr Ophtalmol 1987 ; 10 : 323-9.
[8] Adenis JP, Robin A. La réparation des plaies canaliculaires au monofi lament = avec ou sans intubation ? Premiers résultats. Bull Soc Ophtalmol Fr 1981 ; 81 : 681-2.
[9] Fayet B, Bernard JA, Pouliquen Y. Réparation des plaies canaliculaires récentes avec une sonde mono-canaliculaire à fi xation meatique. Bull Soc Ophtalmol Fr 1989 ; 89 : 819-25.
L. Vera, E. Bui Quoc
Les brÛlures oculaires, en particulier d’origine chimique, sont des urgences ophtalmologiques qui requièrent un traitement immédiat et une évaluation soigneuse des lésions rapidement après l’accident. Si les premières victimes sont la plupart du temps des adultes jeunes lors d’accidents du travail, les enfants sont concernés dans 7 % des cas, en particulier dans le cadre d’accidents domestiques. Comme chez l’adulte, le degré d’ischémie limbique et l’étendue des lésions cornéennes et conjonctivales conditionnent le pronostic. Le traitement démarre par des mesures simples, et se poursuit par des procédures chirurgicales de plus en plus complexes en fonction de la sévérité de l’atteinte, en particulier en cas de déficit limbique en cellules souches. L’objectif de la prise en charge est de freiner la progression des lésions, puis de restaurer l’anatomie et la fonction de la surface oculaire et des tissus adjacents (paupières et voies lacrymales).
Ce sont les plus fréquentes. Elles sont responsables de lésions de l’épithélium de toute la surface oculaire, de la cornée et du SA.
Le degré d’atteinte limbique, cornéenne et conjonctivale dans les premières heures de l’accident, ainsi que la rapidité de la prise en charge sont déterminants pour le pronostic. Les brÛlures chimiques sévères peuvent conduire à une destruction complète de la surface oculaire, une opacification de la cornée, une perte définitive de la vision, voire plus rarement une perte anatomique de l’œil.
Les enfants sont concernés dans 7 % des cas [1], avec deux tiers de garçons impliqués [2, 3 ]. Aux États-Unis, les produits d’entretien domestiques sont le plus souvent en cause, et la majorité des enfants ont entre 1 et 3 ans [4]. La France ne dispose pas de données statistiques disponibles à l’échelle du territoire national. Dans les pays en voie de développement, l’incidence des brÛlures chimiques varie de 1,25 à 4,4 % [5]. Les explosions des sachets de chuna, pâte alcaline comestible utilisée comme additif de tabac à mâcher, sont responsables en Inde de la majorité des accidents par brÛlure de l’enfant [2].
Les bases sont responsables de lésions plus sévères que les acides, car d’emblée plus profondes et surtout évolutives. Les bases sont lipophiles et pénètrent dans l’œil plus rapidement que les acides en dissolvant les lipides des membranes cellulaires. Elles peuvent pénétrer dans la chambre antérieure en lésant les corps ciliaires, l’angle iridocornéen et le cristallin. Ce processus est très rapide et les lésions peuvent être irréversibles dès les 15 premières minutes. Bien que les bases (ammoniac, eau de Javel, soude caustique contenus dans les produits ménagers) engendrent des lésions plus sévères que les acides, un acide tel que l’acide fluorhydrique, que l’on trouve dans les antirouilles, est responsable de lésions très sévères en raison de sa pénétration rapide à travers les membranes cellulaires.
Les acides entraînent une coagulation des protéines de l’épithélium, formant une barrière qui empêche le produit de se propager en profondeur.
Les brÛlures chimiques prises en charge rapidement par un lavage abondant de la surface oculaire, des culs-de-sac et éventuellement des voies lacrymales et une ablation soigneuse des débris nécrotiques et des CE ont plus de chances de conserver une bonne acuité visuelle [6].
La chirurgie peut être utile en phase aiguë en cas de cicatrisation inadaptée de la surface oculaire. En phase chronique, des signes d’insuffisance limbique peuvent apparaître.
La classification de Roper-Hall en quatre grades de gravité croissante, développée dans les années 1960, permet d’établir un pronostic dès la phase initiale, en prenant en compte l’importance de l’opacité cornéenne et l’étendue d’une éventuelle ischémie limbique (Tableau 25-1) [7].
Cependant du fait de l’imprécision de cette classification en particulier pour les formes sévères (grade 4), Dua a établi une nouvelle classification [8] comportant six grades (Tableau 25-2), en fonction de l’atteinte du limbe (quantifiée en quadrants horaires) et de la conjonctive (quantifiée en pourcentage de surface). Cette classification de Dua a été établie grâce aux progrès chirurgicaux de reconstruction de la surface oculaire (auto- ou allogreffe de cellules souches limbiques en particulier). À l’aide de cette classification, on peut établir par exemple qu’une ischémie de 50 % du limbe a davantage de chances de récupérer qu’un déficit de 100 % .
Tableau 25-1 - Classification clinique de Roper-Hall en quatre grades.
Tableau 25-2 - Classification de Dua.
En recherche clinique, un nouvel élément de pronostic de survie du greffon est l’évaluation de la survie des cellules conjonctivales à l’aide des empreintes conjonctivales.
Le patient se présente avec une douleur aiguë, un larmoiement, un blépharospasme et une photophobie importants. Les premiers signes d’une brÛlure sont un œdème et un érythème cutanés péri-oculaires, une désépithélialisation de la peau, et une perte des cils et des sourcils. Puis survient une perte de l’épithélium cornéen et de la conjonctive (fig. 25-16), un chémosis, une inflammation conjonctivale, une ischémie limbique, une opacification et un œdème de la cornée et, dans les cas les plus sévères, une perforation. En cas d’atteinte étendue du limbe, un tableau de déficit en cellules souches limbiques peut s’installer, avec un échec de la réépithélialisation cornéenne, puis une néovascularisation et une conjonctivalisation de la cornée. Une lagophtalmie peut apparaître secondairement à une modification de la mécanique d’ouverture et de fermeture palpébrale, les paupières pouvant être remaniées par l’œdème ou les cicatrices. Cette lagophtalmie peut aussi retarder la réépithélialisation. L’inflammation conjonctivale majeure est responsable de la perte des cellules à mucus, et peut conduire à la constitution d’un syndrome sec. Cela peut être mis en évidence en recherche par des empreintes prélevées sur la conjonctive du patient (fig. 25-17). Les brÛlures étendues peuvent aussi se compliquer de la formation de symblépharons, d’entropion ou d’ectropion et de trichiasis. Une augmentation rapide de la pression intra-oculaire peut survenir par contraction au niveau de la jonction cornéosclérale. Par la suite, l’hypertonie peut apparaître secondairement à la présence de débris dans l’angle iridocornéen, ou à l’inflammation puis à la fibrose de l’angle. Chez l’enfant, le recours à une anesthésie générale est le plus souvent nécessaire dans les cas sévères afin d’évaluer au mieux l’étendue des lésions.
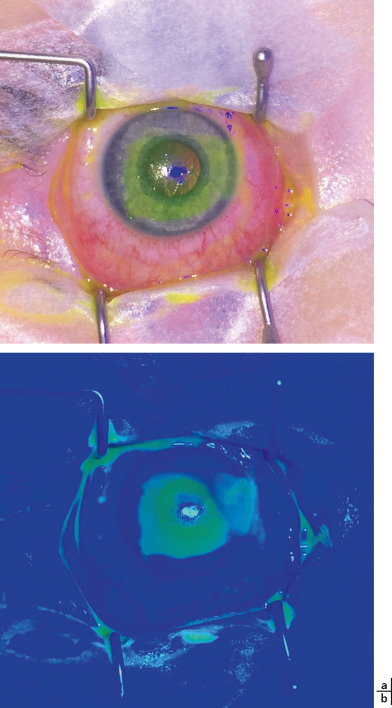
Fig. 25-16 a, b. Ulcère diffus sur 360° à la phase aiguë d’une projection de liquide vaisselle (base) chez un garçon de 4 ans, ayant bénéficié d’une greffe de membrane amniotique ; une cicatrisation totale avec récupération visuelle maximale a été obtenue. (Remerciements au Dr A. Aziz.)
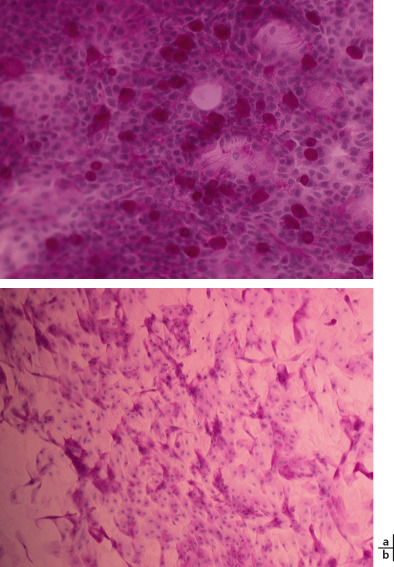
Fig. 25-17 Empreintes conjonctivales. a. Normales : nombreuses cellules à mucus et cellules épithéliales de densité et de morphologie normales. b. Au stade aigu d’une brûlure oculaire : disparition des cellules à mucus et cellules épithéliales désorganisées, allongées.
La précocité du traitement influence favorablement le résultat final [9]. Une irrigation immédiate et abondante permet de laver l’agent chimique. Elle doit être d’une durée au moins égale à 10 minutes. Il faut retirer minutieusement tous les CE, sans oublier les culs-de-sac, avec une pince ou un coton-tige humide selon les disponibilités.
À ce stade, les soins ont pour but de promouvoir la repousse épithéliale, de prévenir l’infection et de maîtriser la réaction inflammatoire.
Le traitement médical commun à tous les grades de brÛlure comprend :
des substituts lacrymaux sans conservateur à volonté, en privilégiant les agents riches en acide hyaluronique [10]. Ils favorisent la réépithélialisation en améliorant l’adhérence du film lacrymal;
un collyre cycloplégique (atropine en concentration adaptée à l’âge de l’enfant) : il peut être prescrit pour la douleur liée aux spasmes ciliaires;
un collyre antibiotique à large spectre;
des antalgiques per os.
Les enfants atteints de brÛlures graves (grades III à VI) doivent être hospitalisés. En plus du traitement de base, on prescrira :
des corticoïdes locaux en instillation horaire, afin d’éviter la destruction secondaire des tissus en limitant la réaction inflammatoire. Ils doivent être progressivement arrêtés en moins de 10 jours au risque de ralentir la repousse épithéliale et la synthèse de collagène [11, 12]. Ils peuvent être réintroduits si nécessaire après la 6e semaine pour lutter contre l’inflammation chronique [13];
des antalgiques par voie intraveineuse;
des tétracyclines par voie générale après l’âge de 8 ans, pour leur action inhibitrice sur les collagénases [14];
de la vitamine C en topique : elle a une action anti-oxydante limitant l’action des radicaux libres libérés durant l’agression chimique. Elle est utile dès le grade III pour remplacer la vitamine C naturellement sécrétée par les corps ciliaires, mais rapidement consommée dans les brÛlures sévères [15];
du sérum de cordon ombilical qui, tout comme la membrane amniotique, est riche en facteurs de croissance (epithelial growth factor [EGF], nerve growth factor [NGF], fibroblast growth factor [FGF], transforming growth factor β ou TGF-β, vitamine A, fibronectine) [16] et qui serait aussi efficace que cette dernière dans les brÛlures de grades III, IV ou V [17]. Son utilisation en France n’a pas encore été rapportée.
Les tissus nécrotiques doivent être débridés, car ils constituent un facteur chimiotactique pour les cellules inflammatoires.
En cas de nécrose conjonctivale étendue, on peut avoir recours de façon précoce à la plastie ténonienne (rapprochement au limbe de lambeaux ténoniens) afin d’éviter la nécrose du SA et la perforation sclérale. L’intervention n’empêche pas la constitution du déficit limibique, mais la greffe de cellules souches limbiques pourra être réalisée dans un second temps (Encadré 25-1).
La greffe de membrane amniotique peut être utilisée en overlay sur toute la surface, elle agit alors comme un pansement. Son application dans les premiers jours d’une brûlure chimique réduit la douleur et accélère la réépithélialisation dans les grades II et III [18]. En cas de préperforation, elle est utilisée en multicouches comme bouchon et sert de support à la repousse épithéliale.
Elle est efficace sur la douleur, permet de diminuer l’inflammation associée au traitement médical et donc limite les séquelles. Son application peut être répétée, car elle se délite au bout d’une semaine en moyenne.
La greffe de cornée à chaud peut être inévitable dans les cas d’amincissement cornéen sévère ou de perforation de diamètre important.
La prise en charge à long terme vise à restaurer la fonction visuelle en préservant la qualité du film lacrymal, en prenant en charge l’insuffisance limbique, la malposition du bord libre, la cataracte, le glaucome.
La lentille sclérale de large diamètre perméable au gaz (prosthetic replacement of ocular surface ecosystem [PROSE]), anciennement lentille de Boston, peut aider la cicatrisation cornéenne, notamment en protégeant la cornée des microtraumatismes liés au clignement lorsque les paupières sont lésées (fig. 25-18) [19].
C. Burillon
Le traitement de l’insuffisance en cellules souches limbiques faisant suite à une brÛlure cornéenne est un long chemin qu’il faut savoir parcourir rapidement chez l’enfant, afin de diminuer le risque d’amblyopie chez le petit enfant et de permettre les acquisitions scolaires correctes chez le plus grand. Lors de brÛlure unilatérale, dès que la surface oculaire est cicatrisée et non inflammatoire, en général 6 mois après le traumatisme, parfois après la réalisation d’une greffe de membrane amniotique, l’autogreffe limbique doit être privilégiée. Cette autogreffe cornéosclérale, d’environ un quart de la circonférence de la cornée saine controlatérale, contient de nombreuses cellules souches épithéliales qui vont proliférer facilement sur la surface cornéenne nettoyée de la prolifération conjonctivale. L’apport d’un morceau de conjonctive en arrière de la cornée prélevée permet de greffer des cellules conjonctivales caliciformes qui ont un rôle dans la restitution du film lacrymal. Quelques mois après, la cornée éclaircie autorise parfois une récupération visuelle incroyable, si le stroma sous-jacent est clair. Dans le cas contraire, la greffe de cornée est proposée avec un risque de rejet amoindri par la diminution voire l’absence de néovaisseaux1 . Dans le cas de brÛlures cornéennes bilatérales, il n’y a parfois que très peu de limbe sain sur l’œil le moins atteint et l’autogreffe tissulaire est impossible. En revanche, le prélèvement de cellules limbiques est possible, avec culture ex vivo, par l’intermédiaire de la thérapie cellulaire, réalisée depuis 1997 par Pelligrini2 . La greffe d’un feuillet de cellules épithéliales limbiques est alors possible sur toute la surface de la cornée la plus atteinte, avec une restitution d’un épithélium de bonne qualité. Si les brÛlures cornéennes sont bilatérales et totales, seules les greffes de cellules souches épithéliales provenant de divers tissus, en cours d’expérimentation actuellement, sont possibles. L’autogreffe de cellules épithéliales de la muqueuse orale cultivées ex vivo a donné de très bons résultats dans une série lyonnaise récente, mais aucun enfant n’avait pu être inclus3 . Une prochaine étude prospective devrait voir le jour prochainement avec une série d’enfants atteints de façon bilatérale.Dans tous les cas, ces autogreffes de tissu ou de cellules permettent de s’affranchir des risques de rejet et d’éviter la mise sous immunosuppresseurs à vie, à la différence des allogreffes, même de donneurs apparentés. Ces autogreffes ne présentent que très peu de complications, qui relèvent plus de la qualité du geste chirurgical que de la technique en elle-même. Par ailleurs, si l’acuité visuelle n’est pas toujours satisfaisante, les signes fonctionnels extrêmement invalidants que présente l’enfant – douleurs, photophobie, spasmes palpébraux – diminuent considérablement après ces chirurgies de réparation de la surface oculaire, ce qui justifie largement leur indication systématique dans les suites de brÛlures oculaires avec déficit en cellules souches limbiques.
1 Durand L, Fages F, Burillon C Greffe lamellaire cornéo-conjonctivale « inlay » , premier temps préparatoire du traitement chirurgical des séquelles de brûlures de cornée J Fr Ophthalmol 1990 ; 13 : 17-23
2 Pellegrini G, Traverso CE, Franzi AT, et al. Long term restoration of damaged corneal surfaces with autologous cultivated corneal epithelium Lancet 1997 ; 349 : 990-993
3 Burillon C, Huot L, Justin V, et al. Cultured autologous oral mucosal epithelial cell sheet transplantation for the treatment of corneal limbal epithelial stem cell deficiency Invest Ophthalmol Vis Sci 2012 ; 53 : 1325-1331
La greffe de membrane amniotique peut être utilisée en overlay sur toute la surface, elle agit alors comme un pansement. Son application dans les premiers jours d’une brÛlure chimique réduit la douleur et accélère la réépithélialisation dans les grades II et III [18]. En cas de préperforation, elle est utilisée en multicouches comme bouchon et sert de support à la repousse épithéliale.
Elle est efficace sur la douleur, permet de diminuer l’inflammation associée au traitement médical et donc limite les séquelles. Son application peut être répétée, car elle se délite au bout d’une semaine en moyenne.
La greffe de cornée à chaud peut être inévitable dans les cas d’amincissement cornéen sévère ou de perforation de diamètre important.
La prise en charge à long terme vise à restaurer la fonction visuelle en préservant la qualité du film lacrymal, en prenant en charge l’insuffisance limbique, la malposition du bord libre, la cataracte, le glaucome.
La lentille sclérale de large diamètre perméable au gaz (prosthetic replacement of ocular surface ecosystem [PROSE]), anciennement lentille de Boston, peut aider la cicatrisation cornéenne, notamment en protégeant la cornée des microtraumatismes liés au clignement lorsque les paupières sont lésées (fig. 25-18) [19].
La greffe de membrane amniotique peut être utilisée lors de la phase de réparation comme adjuvant de différentes techniques de greffe de cellules souches limbiques [20, 21, 22].
La transplantation de cellules souches limbiques (expansion in vivo ou ex vivo) peut être envisagée à distance de la phase aiguë, lorsque l’inflammation est bien contrôlée, et après avoir traité les facteurs irritatifs (trichiasis, symblépharons).
L’autogreffe de cellules limbiques n’est possible qu’en cas d’atteinte unilatérale. Elle ne nécessite pas d’immunosuppression par voie générale en postopératoire, en raison de la compatibilité immunitaire complète.
Une technique relativement récente nommée simple limbal epithelial transplantation (SLET) consiste à greffer un petit fragment de limbe de l’œil sain du patient, sans nécessité d’expandre les cellules ex vivo [23] : des résultats encourageants ont été rapportés y compris sur une cohorte d’enfants [24].
Le traitement des déficits bilatéraux est plus complexe. L’allogreffe conjonctivolimbique de donneur apparenté et l’allogreffe kératolimbique de donneur décédé imposent une immunosuppression locale et générale pour prévenir le rejet. Leur indication doit être bien pesée chez l’enfant en raison de la iatrogénie des immunosuppresseurs et du pronostic parfois sombre des allogreffes [25].
La pratique des greffes après expansion ex vivo de cellules épithéliales de muqueuse buccale ou de progéniteurs limbiques du patient est encore limitée par le coÛt humain et matériel et par la réglementation.
À distance de la reconstruction limbique et après réépithélialisation cornéenne, une kératoplastie transfixiante ou une kératoplastie lamellaire profonde peuvent être envisagées, si le résultat obtenu n’est pas suffisant.
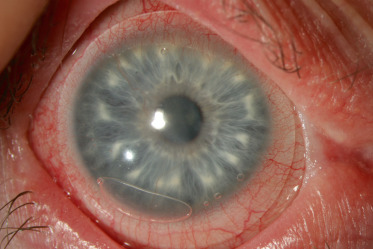
Fig. 25-18 Séquelles de brûlures cornéennes avec néovascularisation cornéenne et mise en place d’un verre scléral. (Remerciements au Pr M. Muraine.)
Les brÛlures thermiques sont essentiellement observées après projection d’eau ou d’huile chaudes. La sévérité des lésions dépend de la durée du contact. Lors des brÛlures par flamme, le réflexe de fermeture des paupières limite les lésions oculaires. Le pronostic dépend alors de l’atteinte associée de la face et des paupières. Les brÛlures par cigarette sont fréquentes. Elles provoquent une ulcération épithéliale, voire stromale peu profonde, localisée. La cicatrisation est rapide et le plus souvent sans séquelles visuelles.
Plus récemment, des brÛlures thermiques et chimiques ont été rapportées suite à l’explosion de cigarettes électroniques [26].
Les rayons ultraviolets du soleil sont responsables de kératite ponctuée superficielle dans l’aire de la fente palpébrale, d’apparition retardée (6 à 12 heures).
Les rayonnements infrarouges provoquent des lésions oculaires par effet thermique, par exemple lors des expositions solaires prolongées (éclipses). La cornée peut être atteinte (kératite ponctuée superficielle), mais des opacités cristalliniennes ou une atteinte rétinienne sont possibles (maculopathie solaire).
Les brÛlures oculaires chez l’enfant sont des accidents rares mais souvent graves. Le traitement peut être long et s’étendre sur plusieurs années. Il ne faudra pas négliger, en particulier chez les enfants de moins de 6 ans, le traitement de l’amblyopie.
Le but du traitement est de restaurer l’anatomie et la fonction de l’œil. Le traitement débute sur les lieux de l’accident par des gestes simples et peut nécessiter des chirurgies complexes en phase séquellaire.
Les progrès constants de la thérapie cellulaire font espérer une réhabilitation visuelle de qualité même dans les cas les plus sévères. Cependant le premier « traitement » reste avant tout préventif par l’éducation des parents et des enfants sur la dangerosité des accidents domestiques en particulier.
[1] Kuckerlkorn R, Luft I, Kottek AA. Chemical and thermal eye burns in the residential area of RWTH Aachen. Analysis of accidents in 1 year using a new automated documentation of findings. Klin Monatsbl Augenheilkd 1993 ; 203 : 34-42.
[2] Vaipayee RP, Shekhar H, Sharma N, Jhanji V. Demographic and clinical profile of ocular chemical injuries in the pediatric age group. Ophthalmology 2014 ; 121 : 377-80.
[3] El-Mekawey, HE, Abu El Einen AG, Abdelmamoud M, et al. Epidemiology of ocular emergencies in the Egyptien population : a five-year retrospective study. Clin Ophthalmol 2011 ; 5 : 955-60.
[4] D’Souza AL, Nelson NG, Mc Kenzie LB. Pediatric burn injuries treated in US emergencies departments between 1990 and 2006. Pediatrics 2009 ; 124 : 1424-30.
[5] Xie YF, Tan YY, Tang S. Epidemiology of 377 patients with chemical burn in Guangdong province. Burns 2004 ; 30 : 569-72.
[6] Arffa R. Grayson’s diseases of the cornea. In : Arffa R. Ed. Chemical injuries. 3rd ed. St. Louis : Mosby-Year Book ; 1991, p. 649-65.
[7] Roper-Hall MJ. Thermal and chemical burns. Transactions of the Ophthalmological Societies of the United Kingdom 1965 ; 85 : 631-53.
[8] Dua HS, King AJ, Joseph A. A new classification of ocular surface burns. Br J Ophthalmol 2001 ; 85 : 1379-83.
[9] Shrage NF, Langefeld S, Zschocke J, et al. Eye burns : an emergency and continuing problem. Burns 2000 ; 26 : 689-99.
[10] Aragona P, Papa V, Micali A, et al. Long term treatment with sodium hyaluronatecontaining artificial tears reduces ocular surface damage in patients with dry eye. Br J Ophthalmol 2002 ; 86 : 181-4.
[11] Donshik PC, Berman NB, Dohlman CH, et al. Effect of topical corticosteroids on ulceration in alkali-burned corneas. Arch Ophthalmol 1978 ; 96 : 2117-20.
[12] Beams R, Linabery L, Grayson M. Effect of topical corticosteroids on corneal wounds strenght. Am J Ophthalmol 1968 ; 66 : 1131-33.
[13] Davis AR, Ali QH, Aclimandos WA, Hunter PA. Topical steroid use in the treatment of ocular alkali burns. Br J Ophthalmol 1997 ; 81 : 732-4.
[14] Hoang-Xuan T, Hannouche D. Medical treatment of ocular burns. J Fr Ophthalmol 2004 ; 27 : 1175-8.
[15] Brodovsky SC, Mc Carthy CA, Snibson G, et al. Management of alkali burns : an 11-year retrospective review. Ophthalmology 2000 ; 107 : 1829-35.
[16] Sharma N, Goel M, Velpandian T, et al. Evaluation of umbilical cord serum therapy in acute ocular chemical burns. Invest Ophthalmol Vis Sci 2011 ; 52 : 1087-92.
[17] Sharma N, Singh D, Maharana PK, et al. Comparison of amniotic membrane transplantation and umbilical cord serum in acute ocular chemical burns : a randomized controlled trial. Am J Ophthalmol 2016 ; 168 :157-63.
[18] Meller D, Pires RTF, Mack RJS, et al. Amniotic membrane transplantation for acute chemical or thermal burns. Ophthalmology 2000 ; 107 : 980-90.
[19] Rosenthal P, Cotter J. The Boston scleral lens in the management of severe ocular surface disease. Ophthalmology Clinics of North America 2003 ; 16 : 89-93.
[20] Kheirkhah A, Casas V, Raju VK, Tseng SCG. Sutureless amniotic membrane transplantation for partial limbal stem cell deficiency. Am J Ophthalmol 2008 ; 145 : 787-94.
[21] Javadi M, Baradaran-Rafii A. Living-related conjunctival-limbal allograft for chronic or delayed-onset mustard gas keratopathy. Cornea 2009 ; 28 : 51-7.
[22] Liang L, Sheha H, Tseng SC. Long-term outcomes of keratolimbal allograft for total limbal stem cell deficiency using combined immunosuppressive agents and correction of ocular surface deficits. Arch Ophthalmol 2009 ; 127 : 1428-34.
[23] Sangwan VS, Basu S, MaxNeil S, Balasubramanian D. Simple limbal epithelial transplantation (SLET) : a novel surgical technique for the treatment of unilateral limbal stem cell deficiency. Br J Ophthalmol 2012 ; 96 : 931-4.
[24] Basu S, Sureka SP, Shanbhag SS, et al. Long-term clinical outcomes in 125 cases of unilateral chronic ocular surface burns. Ophthalmology 2016 ; 123 : 1000-10.
[25] Miri A, Al-Deiri B, Dua HS. Long-term outcomes of autolimbal and allolimbal transplants. Ophthalmology 2010 ; 117 : 1207-13.
[26] Paley GL, Echalier E, Eck TW, et al. Corneoscleral laceration and ocular burns caused by electronic cigarette explosions. Cornea 2016 ; 35 : 1015-8.
g. peCh-gourg
Le syndrome de l’enfant secoué constitue une forme particulière de maltraitance, également qualifiée de traumatisme crânien non accidentel, touchant essentiellement les enfants de moins de 1 an. Malgré les campagnes d’information et de prévention, son incidence ne semble pas diminuer. Le chiffre de 200 enfants touchés chaque année en France sous-estime vraisemblablement la réalité. La maltraitance touche toutes les couches de la société. Les principaux facteurs de risque identifiés pour l’enfant sont le sexe masculin, un antécédent de prématurité, une gémellité, un contexte d’hospitalisation prolongée ou de maladie chronique.
Les lésions sont consécutives à des mouvements de secouements importants administrés par un adulte sur un nourrisson en le tenant généralement par le tronc et sans lui soutenir la tête [1]. Du fait de l’hypotonie axiale à ce stade de développement et d’un rapport de poids tête/corps élevé chez le nourrisson, ces mouvements entraînent un balancement d’avant en arrière de l’extrémité céphalique. Cette alternance d’accélération-décélération est responsable des lésions vasculaires cérébrales et ophtalmologiques par arrachement veineux ou thrombose post-traumatiques : hématomes sous-duraux souvent bilatéraux à prédominance interhémisphérique, hémorragies sous-arachnoïdiennes, thrombophlébites cérébrales, contusions parenchymateuses, hémorragies rétiniennes (généralement bilatérales).
Les motifs d’admission aux urgences sont variés : macrocrânie évolutive et/ou tension de la fontanelle constatées par le pédiatre, épisode de malaise, vomissements itératifs, convulsions, trouble de la vigilance, coma. Le diagnostic d’enfant secoué doit être évoqué devant un décès inexpliqué d’un nourrisson et, d’une façon générale, devant toute suspicion de maltraitance sur un enfant de moins de 1 an (fractures non expliquées, lésions cutanées ou viscérales post-traumatiques, etc.) même en absence de symptomatologie neurologique.
Classiquement, les parents ne rapportent aucun traumatisme crânien ou éventuellement un traumatisme banal sans rapport avec les conséquences observées.
La tomodensitométrie (TDM) cérébrale est réalisée en urgence et montre essentiellement les lésions hémorragiques intracrâniennes. L’hématome sous-dural bilatéral est le plus classiquement retrouvé (fig. 25-19). Il peut être hyperdense, témoignant du caractère aigu de l’hémorragie, iso- ou hypodense en cas de lésions plus anciennes chronicisées, ou de densité mixte faisant évoquer des lésions d’âges différents [2, 3]. Une injection de produit de contraste doit être effectuée à la recherche de thrombose veineuse.
L’IRM cérébrale peut également être réalisée à la phase initiale de la prise en charge (fig. 25-20), mais elle devra surtout être répétée à distance dans un but de surveillance des lésions cérébrales et à visée pronostique [4]. Elle permet de décrire les lésions parenchymateuses secondaires aux phénomènes ischémiques et contusifs. Elle étudie également la jonction craniocervicale qui peut être lésée par les secouements.
Un bilan hématologique doit être effectué à la recherche d’une anomalie de l’hémostase ou de la coagulation qui pourrait constituer le diagnostic différentiel d’une maltraitance.
De façon systématique, il convient de compléter ces examens par un bilan général de maltraitance : radiographies du squelette corps entier, scintigraphie osseuse si nécessaire, échographie abdominale.
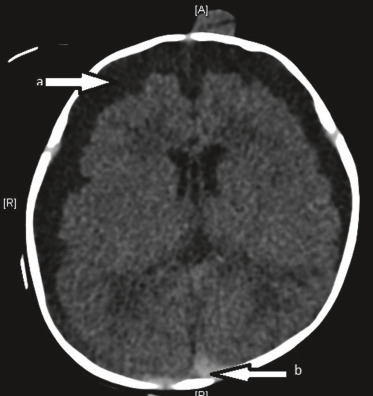
Fig. 25-19 Vergetures endothéliodescemétiques post-traumatiques.
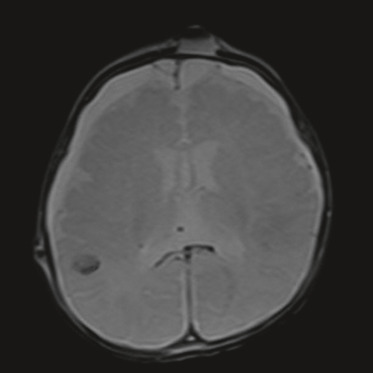
Fig. 25-20 Vergetures endothéliodescemétiques post-traumatiques.
L’examen ophtalmologique est d’une importance capitale [5]. Il doit être effectué par un ophtalmologiste thésé dans les meilleurs délais en raison du caractère fugace des lésions les plus frustes. La description des hémorragies rétiniennes selon trois types à partir des recommandations de la Haute autorité de santé (HAS) (Encadré 25-2) revêt un caractère médico-légal.
Type 1 : hémorragies intrarétiniennes, en flammèches, en taches ou ponctiformes, situées au pôle postérieur de l’œil.
Type 2 : hémorragies en dôme prérétiniennes, de petite taille, localisées au pôle postérieur de l’œil, autour de la papille et le long des arcades vasculaires, ou en moyenne périphérie. Elles sont isolées ou associées à des hémorragies rétiniennes de type 1.
Type 3 : hémorragies multiples de tous types (intra-, préou sous-rétiniennes), profuses, tapissant toute la rétine ou l’éclaboussant jusqu’à la périphérie, associées à un placard hémorragique prémaculaire, uni- ou bilatéral.
On considère que les hémorragies rétiniennes sont pathognomoniques du syndrome de l’enfant secoué lorsqu’elles sont bilatérales, nombreuses, de la rétine jusqu’à la périphérie avec parfois rétinoschisis hémorragique, pli rétinien périmaculaire (fig. 25-21). Mais des formes plus frustes peuvent se voir. L’absence d’hémorragie rétinienne (20 % des cas) n’élimine pas le diagnostic.
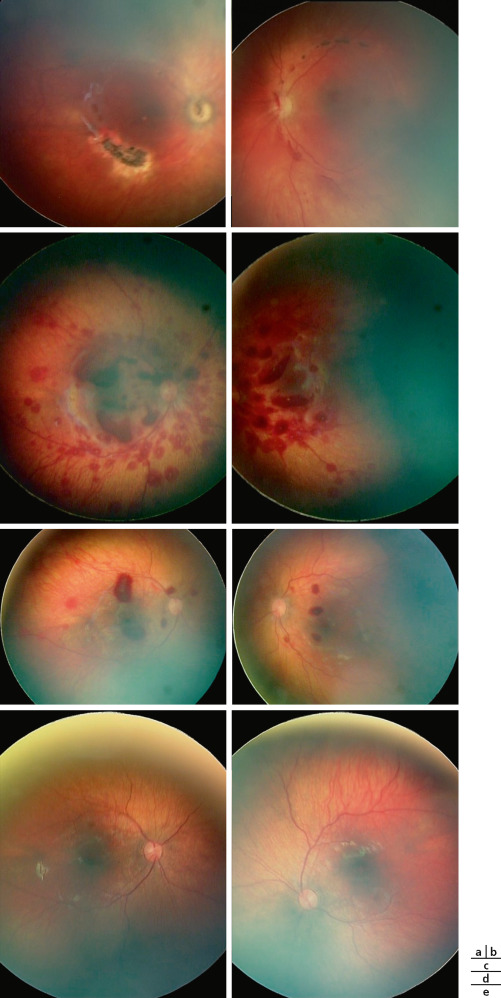
Fig. 25-21 Rétinophotographies de nouveau-nés victimes du syndrome de l’enfant secoué. OEil droit (a) et oeil gauche (b). Lésions initiales de type 3 bilatérales selon la classification de la HAS (2011) avec vastes hémorragies prémaculaires ayant nécessité une vitrectomie d’évacuation. Séquelles à 3 mois : persistance d’hémorragies intravitréennes et rétiniennes sur les bords de l’hématome maculaire, cicatrices rétiniennes atrophiques et pigmentées en regard des hémorragies et des tractions rétiniennes les plus importantes, atrophie optique bilatérale par section axonale des voies visuelles. c-e. Autre enfant : examen initial montrant de multiples hémorragies bilatérales intrarétiniennes et prérétiniennes en dômes maculaires de type 3 à droite et 2 à gauche selon la classification de la HAS (2011) (c) ; évolution à 15 jours du traumatisme initial (d) ; évolution à 2 mois avec régression quasi complète des hémorragies, apparition d’une discrète pâleur papillaire (e). (Remerciements au Pr D. Denis et collaborateurs.)
En parallèle à la prise en charge médico-chirurgicale des conséquences du traumatisme (drainage d’un hématome sous-dural, traitement médicamenteux d’une épilepsie, etc.), des mesures de protection de l’enfant s’imposent en urgence du fait du haut risque de récidive de maltraitance. L’enfant doit toujours être hospitalisé. Un signalement judiciaire au procureur de la République doit être effectué par les médecins ayant l’enfant en charge lorsque le diagnostic de syndrome de l’enfant secoué est considéré comme probable (Tableau 25-3). L’officier de police judiciaire délivre alors un ordre de garde provisoire au service dans lequel l’enfant est hospitalisé et une enquête pénale est ouverte. Lorsque le diagnostic est considéré comme possible (Tableau 25-3), la HAS recommande de transmettre une information préoccupante au conseil départemental [6].
Tableau 25-3 – Critères diagnostiques de syndrome de l’enfant secoué.
La mortalité globale en rapport avec le syndrome de l’enfant secoué varie selon les études entre 10 et 40 % [7]. D’après une étude canadienne [8], sur 295 enfants survivants évalués à la sortie de l’hôpital, 22 % étaient considérés comme indemnes, 55 % avaient des signes neurologiques et 65 % un déficit visuel.
À plus long terme, les séquelles rapportées sont un retard de développement psychomoteur, des déficits moteurs d’origine cérébrale, une épilepsie, des troubles du comportement, des troubles des apprentissages et des déficits visuels [9]. Un suivi pluridisciplinaire prolongé est donc indispensable.
[1] Caffey J. The whiplash shaken infant syndrome : manual shaking by the extremities with whiplash-induced intracranial and intraocular bleedings, linked with residual permanent brain damage and mental retardation. Pediatrics 1974 ; 54 : 396-403.
[2] Girard N, Brunel H, Dory-Lautrec P, Chabrol B. Neuroimaging differential diagnoses to abusive head trauma. Pediatr Radiol 2016 ; 46 : 603-14.
[3] Duhaime AC, Christian CW, Rorke LB, Zimmerman RA. Nonaccidental head injury in infants—the “shaken-baby syndrome”. N Engl J Med 1998 ; 338 : 1822-9.
[4] Bonnier C, Nassogne MC, Saint-Martin C, et al. Neuroimaging of intraparenchymal lesions predicts outcome in shaken baby syndrome. Pediatrics 2003 ; 112 : 808-14.
[5] Levin AV. Ocular manifestation of child abuse. Ophthalmology Clinics of North America 1990 ; 3 : 249-64.
[6] Laurent-Vannier A, Nathanson M, Quiriau F, et al. A public hearing « shaken baby syndrome : guidelines on establishing a robust diagnosis and the procedures to be adopted by healthcare and social services staff » . Guidelines issued by the Hearing Commission. Ann Phys Rehabil Med 2011 ; 54 : 600-25.
[7] Barlow K, Thopmson E, Johnson D. The neurological outcome of non-accidental head injury. Dev Neurorehabil 2004 ; 7 : 195-203.
[8] King WJ, MacKay M, Sirnick A, et al. Shaken baby syndrome in Canada : clinical characteristics and outcomes of hospital cases. Can Med Assoc J 2003 ; 168 : 155-9.
[9] Jayawant S, Parr J. Outcome following subdural haemorrhages in infancy. Arch Dis Child 2007 ; 92 : 343-7.