Dysfonctionnements meibomiens et blépharites
S. Doan, D. Brémond-Gignac, M. Castelain, B. Cochener, C. Albou-Ganem, B. Mortemousque, T. Hoang-Xuan
Les dysfonctionnements des glandes de meibomius (DGM) sont très fréquents et représentent la première cause de sécheresse oculaire, en rapport avec une hyperévaporation lacrymale. DGM et blépharites surviennent le plus fréquemment dans le cadre d’une rosacée ou d’une dermite séborrhéique qu’il faut rechercher à l’examen clinique. On peut aussi les retrouver chez la femme ménopausée et dans le cadre d’allergies, de conjonctivites fibrosantes ou de toute autre conjonctivite chronique. L’examen clinique du bord libre palpébral est essentiel afin d’évaluer la qualité du meibum, l’inflammation du bord libre et le retentissement sur la surface oculaire : instabilité lacrymale, pannus cornéen, kératite ponctuée inférieure. Une surinfection palpébrale expliquera également les complications inflammatoires comme les infiltrats catarrhaux, les kératoconjonctivites phlycténulaires, les (épi)sclérites. Les examens complémentaires comme la meibographie, l’interférométrie du film lacrymal, la microscopie confocale in vivo et la recherche de Demodex peuvent compléter le diagnostic qui reste avant tout clinique.
Les dysfonctionnements des glandes de Meibomius (DGM) et les blépharites représentent une part importante des pathologies de la surface oculaire. Ils sont en effet la principale cause de sécheresse oculaire, et la plus importante cause de sécheresse évaporative [1, 2]. Ils peuvent être primitifs ou secondaires à une inflammation chronique de voisinage conjonctivale ou cutanée, ce qui explique leur fréquence. Ils sont également à l’origine d’un polymorphisme clinique faisant la particularité des DGM et de la rosacée qui en est une étiologie majeure.
On parle de DGM lorsque la fonction meibomienne est perturbée. Il s’agit le plus souvent d’un déficit de délivrance du meibum au niveau de la surface oculaire, qui peut être lié à une diminution de la quantité de cette sécrétion, à son hyperviscosité ou encore à une obstruction des glandes meibomiennes. Plus rarement, il existe une hyperproduction d’un meibum pathologique, caractérisant la séborrhée meibomienne ou meiborrhée.
La blépharite est une inflammation des paupières, en général prédominant sur le bord libre. On distingue les blépharites antérieures, siégeant en avant de la ligne grise et touchant les cils ou la partie cutanée du bord libre, des blépharites postérieures qui concernent les glandes de Meibomius (on parle alors de meibomite) et le versant conjonctival du bord libre. La blépharite est dite mixte en cas d’atteinte antérieure et postérieure. Un DGM peut être associé ou non à une blépharite postérieure.
Le DGM et les blépharites sont très fréquents, leur prévalence étant probablement nettement sous-estimée [3]. Les ophtalmologistes ne les recherchent pas systématiquement et une grande partie de ces pathologies est asymptomatique. Une étude récente espagnole retrouve une prévalence de 8,6 % de DGM symptomatiques et 21,9 % de DGM asymptomatiques [4]. Les prévalences globales sont cependant très variables selon les études, car les critères et méthodologies diffèrent. Ainsi, celle rapportée par la Salisbury study est de 3,5 % [5], alors qu’elle est de 69 % dans la Beijing eye study [6]. On peut raisonnablement retenir les valeurs moyennes de 30 à 39 % rapportées par des études américaine et espagnole [4, 7]. Les DGM semblent beaucoup plus fréquents en Asie qu’en Europe ou en Amérique du Nord [8]. Ils augmentent clairement avec l’âge ce qui souligne le rôle des androgènes. La prévalence du DGM de 33 % avant 30 ans, passe à 72 % après 60 ans [7].
La sécheresse oculaire est une pathologie oculaire fréquente bien documentée dont la prévalence varie de 5 à 35 % selon la tranche d’âge [9]. Deux études récentes montrent que les DGM représentent la première cause de sécheresse évaporative et aussi de sécheresse, toutes causes confondues [1, 10]. Les causes de sécheresse oculaire sont : évaporative pure (avant tout par DGM) dans 35 à 58 % des cas, une hypoproduction lacrymale pure dans 4 à 11 % des cas et mixte dans 25 à 31 % des cas. La part des DGM dans la sécheresse représenterait ainsi jusqu’à 89 % des cas.
Les facteurs de risque de DGM évoqués sont [8] :
-
des facteurs oculaires : surtout la blépharite chronique antérieure ou postérieure et l’infestation par Demodex ; le port de lentille de contact d’autant plus qu’il existe une conjonctivite gigantopapillaire ; plus rarement les syndromes de Gougerot-Sjögren, de Lyell et de Stevens-Johnson, la maladie du greffon contre l’hôte, la pemphigoïde des muqueuses, les allergies oculaires, l’aniridie, le floppy eyelid syndrome, la dégénérescence cornéenne nodulaire de Salzmann, l’ichtyose, les dysplasies ectodermiques ;
-
des facteurs généraux : l’âge ; la ménopause ; la rosacée (odds ratio [OR] = 3,50) ; la dermite séborrhéique ; le psoriasis ; la maladie de Parkinson ; le diabète (OR = 2,23) ; la polyarthrite rhumatoïde (OR = 16,50) ; une maladie cardiovasculaire (OR = 1,80) [4] ; des médicaments comme l’isotrétinoïne, les anti-androgènes, les substituts hormonaux de la ménopause, les antihistaminiques H1, les antidépresseurs ; le syndrome d’insensibilité androgénique.
La fréquence d’une atteinte oculaire concomitante à la rosacée est très variable, de 3 à 58 % selon les études [11]. Le DGM et ses complications oculaires peuvent être isolés sans atteinte cutanée dans 25 % des cas.
Concernant les blépharites, Lemp rapporte aux États-Unis une prévalence de 37 à 47 % [3]. Par ailleurs, la fréquence des symptômes dans la population américaine semble être plus élevée chez l’adulte jeune que chez les personnes âgées. Les blépharites sont bien sûr plus fréquentes dans la rosacée et les dermites séborrhéiques.
Chez l’enfant, le DGM est révélé par des chalazions récidivants ou une blépharo-kératoconjonctivite éventuellement phlycténulaire. Sa prévalence est de 12 à 15 % dans deux cohortes pédiatriques américaine et indienne [12, 13]. Les auteurs soulignent que les blépharites représentent la première cause de référence dans leur unité d’ophtalmopédiatrie spécialisée.
Le meibum est produit par les glandes de Meibomius enchâssées dans le tarse palpébral supérieur (30 à 40 glandes) et inférieur (20 à 25 glandes) et qui s’abouchent au niveau du bord libre à la jonction mucocutanée. Ce sont des glandes sébacées modifiées, holocrines [14], constituées chacune d’un canal principal vertical entouré d’acini.
Le meibum est l’unique source de lipides lacrymaux. Il a avant tout pour rôle de limiter l’évaporation des larmes. Les conséquences d’un DGM sont une évaporation lacrymale exagérée, une sécheresse dite évaporative et une instabilité lacrymale. Mais le meibum a également d’autres rôles :
-
il lisse la surface oculaire et améliore la qualité optique du dioptre cornéen antérieur ;
-
il facilite l’étalement du film lacrymal ;
-
il empêche la contamination des larmes par la sueur.
Le meibum normal a l’aspect et la consistance d’une huile, et est composé essentiellement de cires et stérols estérifiés [14, 15] qui forment la couche superficielle dite apolaire, car hydrophobe, du film lipidique lacrymal dont le rôle est de limiter l’évaporation des larmes. Il contient également triglycérides, phospholipides et cérébrosides qui sont en quantité moindre et sont à l’interface des couches apolaire du film lipidique et aqueuse du film lacrymal. À la fois hydrophobe et hydrophile, ces éléments sont essentiels à la stabilité du film lacrymal en assurant une adhérence et un étalement corrects de la couche lipidique sur celle aqueuse.
Plusieurs facteurs indépendants régulent la fonction des glandes de Meibomius :
-
les androgènes et les œstrogènes ont un rôle trophique sur les glandes de Meibomius qui ont des récepteurs spécifiques pour ces hormones [16]. Un DGM apparaît à la ménopause et l’andropause, ou en cas de traitement anti-androgénique ;
-
une régulation nerveuse est suggérée par la riche innervation des glandes meibomiennes, de type majoritairement cholinergique parasympathique, avec des neuropeptides tels que le calcitonin gene-related peptide (CGRP), la substance P et le vasoactive intestinal polypeptide (VIP) [17] ;
-
les médicaments comme l’isotrétinoïne, utilisée dans le traitement de l’acné, inhibent la croissance des meibocytes et leur production lipidique, et induisent une kératinisation et une atrophie des glandes meibomiennes [18].
Les nombreuses anomalies de composition du meibum au cours des DGM expliquent la symptomatologie clinique, en dépit d’une grande variabilité interindividuelle.
La température de fusion du meibum s’élève de 32 à 35 degrés, induisant l’augmentation de sa viscosité et sa stagnation, et l’obstruction des glandes de Meibomius. Ceci serait en rapport avec une diminution du taux d’acides gras mono-insaturés et d’acides gras branchés, et une augmentation du taux de stérols estérifiés et de la longueur des chaînes carbonées [15].
L’instabilité de la couche lipidique des larmes peut être expliquée par la diminution du taux de lipides polaires, en particulier phosphatidyl éthanolamine et sphingomyéline, et de triglycérides, qui sont essentiels au bon étalement de la couche superficielle de lipides non polaires hydrophobes sur la couche aqueuse.
Les acides gras libres et les peroxydes d’acides gras retrouvés en quantité anormalement élevée sont irritants et toxiques pour l’épithélium des glandes meibomiennes et celui de la surface oculaire [19].
En cas de séborrhée meibomienne, le meibum est fluide mais il est produit en quantité anormalement importante. Il contient en particulier des peroxydes d’acides gras qui sont très irritants et peuvent également induire une kératinisation glandulaire.
Les techniques d’exploration des lipides meibomiens les plus récentes comme la « lipidomique » objectivent de nombreuses autres modifications fines de la composition meibomienne, dont la signification n’est pas encore éclaircie [20].
Au cours des DGM obstructifs, on observe une augmentation de la flore microbienne commensale (Staphyloccus aureus, Staphyloccus epidermidis, Propionibacterium acnes) qui est naturellement présente dans les glandes meibomiennes et au niveau du bord libre. Les prélèvements bactériologiques à ce niveau sont plus souvent positifs en cas de blépharite, jusqu’à 98 % des cas [21]. L’analyse de la classification de McCulley indique que la seule présence d’une inflammation clinique doit faire suspecter une surinfection [22].
Les bactéries responsables possèdent une activité lipasique naturelle (triglycéride lipase, cholestérol estérase et cire estérase) [23, 24]. Il en résulte de nombreuses modifications du meibum, avec en particulier la production d’acides gras libres aux dépens des esters de cire et de cholestérol. Il se crée un véritable cercle vicieux [25] car le dysfonctionnement meibomien s’en trouve majoré (voir fig. 3-19). Le cholestérol libre favorise également la prolifération bactérienne [26]. Il est cependant difficile d’affirmer si celle-ci est un facteur aggravant ou la cause même du dysfonctionnement meibomien.
Les bactéries, en particulier les staphylocoques, peuvent aussi provoquer une inflammation locorégionale qui répond à des mécanismes variés. Les acides gras libres et peroxydes d’acides gras résultant de leur activité lipasique induisent une inflammation non spécifique. La libération de toxines et d’antigènes de la paroi bactérienne au niveau de la surface oculaire non seulement y contribue, mais engendre également des réactions plus spécifiques d’hypersensibilité de type III et IV selon la classification de Gell et Coombs qui expliquent des formes cliniques spécifiques comme la kératoconjonctivite phlycténulaire, les infiltrats catarrhaux [27] et probablement l’inflammation conjonctivale et les sclérites.
Enfin, l’infection chronique des follicules pilosébacés annexés aux cils réalise une blépharite antérieure croûteuse. L’infection aiguë est à l’origine d’un orgelet qui est un furoncle du cil, alors que le chalazion est un granulome aigu meibomien aseptique.
Les antibiotiques utilisés pour les DGM et les surinfections ont pour but de diminuer la charge en bactéries et, également par ce biais, leur activité lipasique et celle des métalloprotéases. L’efficacité anti-enzymatique est obtenue à des doses moindres que celles requises pour une action antibactérienne efficace : 40 mg/jour contre 100 mg/jour pour la doxycycline par exemple [28].
La responsabilité du Demodex dans les blépharites est un sujet qui reste très controversé.
Le Demodex est un acarien de moins de 500 microns faisant partie de la flore commensale de la peau et du bord libre palpébral (fig. 4-1). On décrit deux espèces différentes, Demodex follicularum et Demodex brevis [29]. D. follicularum serait plus souvent retrouvé sur les cils et D. brevis, plus petit, dans les glandes de Meibomius. Ils peuvent se déplacer de 16 mm par heure, en général la nuit. Ils se nourrissent de sébum qu’ils dégradent grâce à des lipases. N’ayant pas d’anus, ils meurent après un cycle de vie de 14 jours.
Il existe une tolérance spécifique pour le Demodex, et leur nombre est régulé par des mécanismes d’immunité innée. Le Demodex pourrait avoir un rôle de contrôle de la prolifération locale des bactéries en les ingérant. Il s’agit d’une symbiose. En cas d’immunosuppression locale ou générale (virus de l’immunodéficience humaine ou VIH, atopie, corticoïdes, etc.), le Demodex peut proliférer et cela s’appelle alors une parasitose.
Le portage cutané de Demodex augmente avec l’âge : 0 % à la naissance, 20 à 80 % chez l’adulte, 100 % après 60 ans [30]. Des chiffres équivalents sont retrouvés au niveau palpébral [31]. Cela s’expliquerait par une modification du sébum et une baisse des défenses immunitaires.
Dans des conditions pathologiques, le Demodex peut causer une réaction inflammatoire. Chez les patients présentant une rosacée papulopustuleuse, il existe un infiltrat inflammatoire lymphocytaire CD4+ folliculaire et périfolliculaire cutané plus important chez ceux avec démodécidose [32]. Les mécanismes n’en sont pas clairs : réaction granulomateuse à corps étranger contre l’enveloppe parasitaire ; stimulation de l’immunité innée ; (trans)portage de bactéries de surface comme Staphylococcus epidermidis ; portage de bactéries internes telles Bacillus oleronius qui sont capables de générer une sensibilisation spécifique de l’organisme avec immunoréactivité sérique, comme cela a été décrit chez des patients atteints de rosacée papulopustuleuse [33].
Cependant, en l’absence de modèle expérimental chez l’animal, on ne peut établir un lien formel de cause à effet entre la présence de Demodex et une blépharite, ce d’autant que les traitements spécifiques comme l’ivermectine n’ont qu’une efficacité très inconstante.
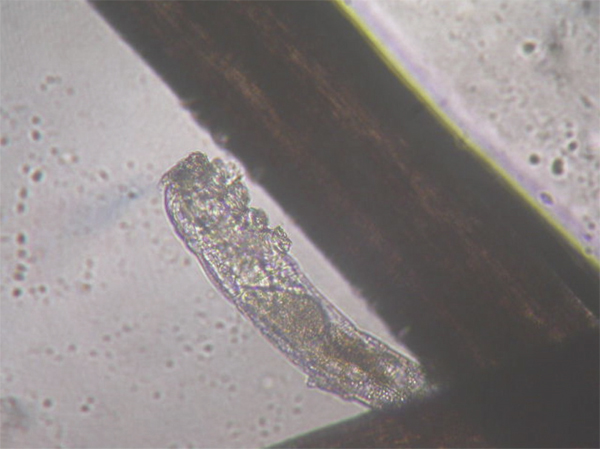
Fig. 4-1 Demodex folliculorum en microscopie optique.
(Source : collection laboratoire du centre hospitalier national d’ophtalmologie des Quinze-Vingts, Paris.)
Une relation entre rosacée et infection à Helicobacter pylori a été avancée dans quelques rares publications, en particulier en ce qui concerne les bouffées vasomotrices [34]. L’association entre ces deux pathologies très fréquentes est probablement fortuite et cette hypothèse semble aujourd’hui abandonnée.
Cette levure serait incriminée dans les dermites séborrhéiques et, par extension, dans les blépharites associées à ces dermatoses. Quelques cas de blépharites rebelles à Malassezia cédant à un traitement antifongique oral ont été rapportés [35].
Une kératinisation des méats des glandes de Meibomius et de la partie distale de leurs canaux excréteurs apparaît quasi constamment avec le temps. Elle aggrave le dysfonctionnement meibomien obstructif et est à l’origine d’une dilatation puis d’une atrophie glandulaires [36, 37]. Cette hyperkératinisation serait favorisée surtout par l’âge, une diminution des androgènes ou un traitement par isotrétinoïne. Les lipides cytotoxiques présents dans le meibum pathologique et l’inflammation peuvent également stimuler la kératinisation.
L’hyperosmolarité lacrymale cause aussi une inflammation qui induit une kératinisation de l’épithélium cornéen par la synthèse de protéines de cornification [38]. On pourrait émettre l’hypothèse d’un mécanisme semblable au niveau des méats meibomiens.
Un clignement réflexe incomplet est très fréquemment mis en évidence par un examen sémiologique fin ou des systèmes d’analyse vidéo comme les modèles récents d’interférométrie du film lacrymal. Il en résulte non seulement une souffrance de la surface cornéoconjonctivale inférieure, mais également une kératinisation de toute la marge palpébrale. Le DGM est alors aggravé par deux mécanismes :
-
l’obstruction des méats meibomiens par la kératine ;
-
la diminution de la vidange mécanique meibomienne liée à la mauvaise contraction de l’orbiculaire et à l’absence de pression entre paupières supérieures et inférieures.
On peut en rapprocher les malocclusions palpébrales diurnes ou nocturnes qui ont les mêmes conséquences.
Toute inflammation conjonctivale chronique peut entraîner un DGM et, à l’inverse, les DGM primitifs tels que la rosacée oculaire induisent une inflammation. Cette dernière est démontrée par les empreintes conjonctivales mettant en évidence une surexpression de marqueurs d’inflammation comme l’antigène HLA-DR et la molécule d’adhésion ICAM1, et une diminution de la mucine MUC5AC [39]. La biopsie conjonctivale montre aussi un infiltrat de cellules mononucléées composé de lymphocytes, avec un ratio CD4/CD8 anormalement élevé, et de macrophages, avec parfois présence de granulomes [40, 41].
Les métalloprotéases matriciellles (MMP), enzymes de dégradation tissulaire, semblent jouer un rôle particulièrement important dans la rosacée, en particulier MMP-9 et leur inducteur EMMPRIN (extracellular matrix metalloproteinase inducer) [42]. Le taux de MMP-9 est élevé dans les larmes et corrélé à la sévérité clinique et biologique (taux d’interleukine-1 alpha dans les larmes) de la maladie [43, 44]. MMP-9 et EMMPRIN clivent les occludines de l’épithélium cornéen qui perd alors son imperméabilité. MMP-3 est aussi augmentée en cas de lésions cornéennes [45].
Il existe plusieurs cercles vicieux (voir fig. 3-19) participant à l’auto-entretien des DGM [25] :
-
l’obstruction et l’hyperviscosité meibomiennes favorisent la prolifération de la flore saprophyte bactérienne qui, par ses lipases, dégrade les lipides meibomiens [23, 24]. La viscosité du meibum s’en trouve alors augmentée et du cholestérol libre est produit, aidant en retour à la prolifération bactérienne [26] ;
-
le DGM induit une sécheresse évaporative avec hyperosmolarité qui provoque, par le biais d’une inflammation, la production de protéines possiblement à l’origine d’une kératinisation des méats meibomiens [38], qui aggrave à son tour le DGM.
Plusieurs classifications existent pour les DGM et les blépharites, se basant sur des considérations anatomiques, étiologiques, physiopathologiques ou cliniques :
-
la classification anatomique des blépharites différencie les formes antérieures (blépharites séborrhéiques et staphylococciques) des formes postérieures (DGM et meibomites). On peut distinguer les atteintes primitives des formes secondaires à une inflammation de voisinage. Cette classification est celle retenue dans la rubrique Étiologies (voir plus loin) et est résumée dans l’encadré 4-1 ;
Encadré 4-1 - Étiologies et classification des blépharitesDGM et blépharites postérieures primitives
• Âge et ménopause
• Rosacée
• Dermite séborrhéique
• Anomalies meibomiennes congénitales (dysplasies ectodermiques, ichtyoses)
• DGM iatrogènes :
▪ isotrétinoïne et rétinoïdes
▪ anti-androgéniques, contraceptifs
▪ chimiothérapies
DGM et blépharites postérieures secondaires
• Conjonctivites allergiques chroniques (conjonctivites perannuelles, kératoconjonctivites vernales et atopiques)
• Conjonctivites fibrosantes sévères (pemphigoïde des muqueuses, syndromes de Stevens-Johnson et de Lyell)
• Syndrome de Gougerot-Sjögren, réaction du greffon contre l’hôte
• Traitement au long cours par collyres
• Port de lentilles de contact
• Traumatisme chirurgical
Blépharites antérieures primitives
• Dermite séborrhéique
• Psoriasis
• Blépharites infectieuses :
▪ staphylococcique
▪ Demodex
▪ fongique
▪ pédiculose
Blépharites antérieures secondaires à une atteinte cutanée
• Eczéma palpébral
• Lupus érythémateux chronique discoïde
• Molluscum contagiosum
• Infection herpes simplex virus (HSV) et varicella-zoster virus (VZV)
-
la classification des blépharites selon McCulley repose sur leur aspect clinique et leur mécanisme [22]. Sa complexité rend cependant difficile son utilisation en pratique courante. Elle distingue les blépharites staphylococcique, séborrhéique isolée, séborrhéique staphylococcique, séborrhéique avec séborrhée meibomienne, séborrhéique avec meibomite secondaire, et la kératoconjonctivite meibomienne primitive ;
-
la dernière classification est celle proposée par l’International Workshop on Meibomian Gland Dysfunction parue en 2011 [46]. Elle analyse les dysfonctionnements meibomiens par leurs mécanismes anatomiques et distingue les formes hypersécrétantes comme dans la blépharite séborrhéique de celles hyposécrétantes dont il existe deux types, l’un avec DGM obstructif comme dans la rosacée et l’autre dit cicatriciel où les méats meibomiens sont fibrosés, comme dans la pemphigoïde des muqueuses.
Les symptômes en rapport avec la sécheresse oculaire sont l’objet des plaintes les plus fréquentes. Ils sont peu spécifiques, à type de sensations de brûlures oculaires ou de corps étranger. Ils sont souvent exacerbés dans les endroits climatisés ou lors du travail sur écran, de la lecture et de la conduite automobile. Un larmoiement paradoxal et une vision fluctuante traduisent une instabilité lacrymale. Une rougeur oculaire est habituelle et doit faire évoquer une complication aiguë cornéenne si elle s’associe à une photophobie et à une douleur.
Le patient peut également se plaindre de ses paupières, à cause d’un prurit, d’une rougeur du bord libre avec sensation de brûlure à ce niveau, de paupières lourdes et gonflées, ou de la présence de croûtes. On interrogera sur l’existence de chalazions ou d’orgelets dans les antécédents et sur une prise d’isotrétinoïne ou d’autres médicaments (contraceptifs oraux, chimiothérapies) susceptibles d’altérer la fonction meibomienne.
L’atteinte cutanée du visage, dans le cadre d’une rosacée ou d’une dermite séborrhéique, doit être recherchée car elle peut être fugace. Il s’agit pour la rosacée de flushes déclenchés par les émotions, la chaleur ou la prise d’alcool, ou d’une rougeur permanente évoluant vers des éruptions pseudo-acnéiques. Dans la dermite séborrhéique, on retrouvera plutôt des épisodes de rougeur cutanée avec prurit et sensation de brûlures sur une peau plutôt grasse, avec présence de squames dans les zones d’hyperséborrhée.
L’examen du bord libre palpébral est la clé du diagnostic en cas de DGM ou de blépharite.
Le DGM peut être évoqué par la présence de bouchons obturant l’abouchement des glandes de Meibomius (fig. 4-2). On peut analyser les glandes meibomiennes du côté conjonctival tarsal et noter une dilatation, un enkystement, voire un chalazion (fig. 4-3), une atrophie glandulaire partielle ou complète (fig. 4-4), une kératinisation méatique, une rétraction du bord libre liée à l’atrophie d’une glande. Le bord libre peut être épaissi et irrégulier.
Le testing meibomien, ou meibopression, est une manœuvre fondamentale qui seule permet un examen qualitatif et quantitatif du meibum. L’aspect palpébral peut être tout à fait normal, alors que le testing meibomien montrera la présence d’un meibum anormal. C’est le cas dans la forme clinique appelée non obvious meibomian gland dysfunction [47]. La pression de la face antérieure des paupières, près du bord libre, fait sourdre le meibum au niveau des méats meibomiens. On peut utiliser un dispositif dédié qui permet d’appliquer une pression calibrée sur les paupières. Le meibum normal est transparent et huileux, et s’exprime facilement. Un meibum pathologique sort difficilement et prend un aspect louche et visqueux (fig. 4-5). L’absence totale d’expression de meibum traduit une atrophie meibomienne de mauvais pronostic car les soins des paupières seront inefficaces.
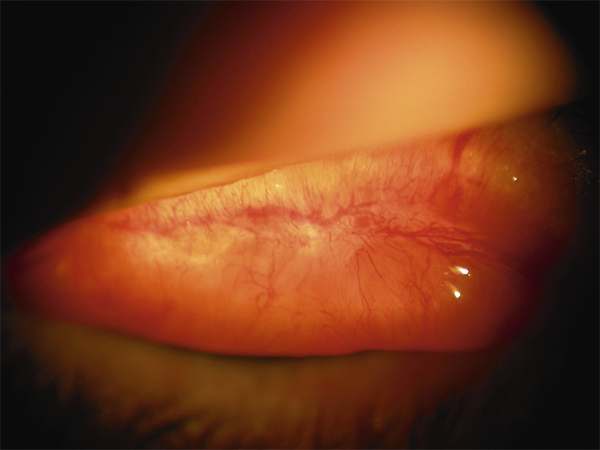
Parfois le meibum est très fluide, abondant et spumeux. La présence de « mousse » au niveau du bord libre signe une séborrhée meibomienne, ou meiborrhée (fig. 4-6), qui est une forme de DGM plutôt rencontrée dans les dermites séborrhéiques. Ce meibum dénaturé est particulièrement irritant.
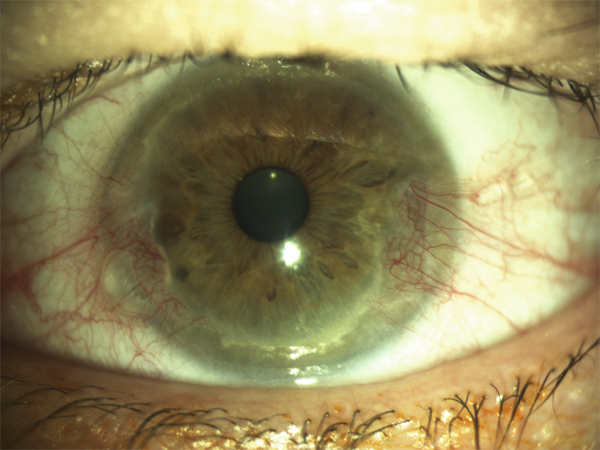
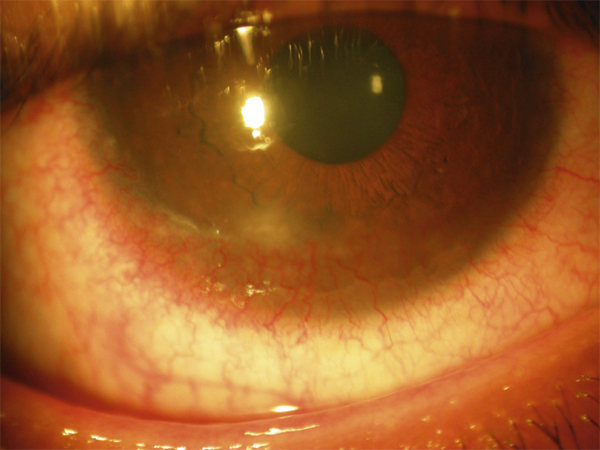
Des télangiectasies peuvent siéger sur le bord libre ou la face antérieure des paupières (fig. 4-7). Elles sont physiologiques chez le sujet âgé lorsqu’elles sont peu nombreuses. Dans la blépharite postérieure, on notera une inflammation au niveau des méats meibomiens et sur toute la ligne postérieure avec un œdème et une hyperhémie du bord libre (fig. 4-8).
Le chalazion correspond à un granulome d’une glande de Meibomius obstruée et n’est théoriquement pas infectieux. Il apparaît de façon aiguë sous forme d’une voussure inflammatoire et douloureuse du bord libre ou de la paupière. Après une à plusieurs semaines d’évolution, il peut disparaître, fistuliser à la peau ou à la conjonctive, ou s’enkyster. Chez l’enfant présentant des chalazions récurrents, il faut rechercher un trouble de la réfraction mal corrigé ou, plus souvent, un dysfonctionnement meibomien primitif (rosacée de l’enfant).
Chez l’adulte plutôt âgé, un chalazion multirécidivant malgré un traitement adapté doit faire suspecter un adénocarcinome meibomien, tumeur très rare mais dont le pronostic est redoutable.

Fig. 4-2 Bouchons kératinisés des méats meibomiens.

Fig. 4-3 Chalazions.

Fig. 4-4 Glandes de Meibomius dilatées, rétrécies ou absentes.
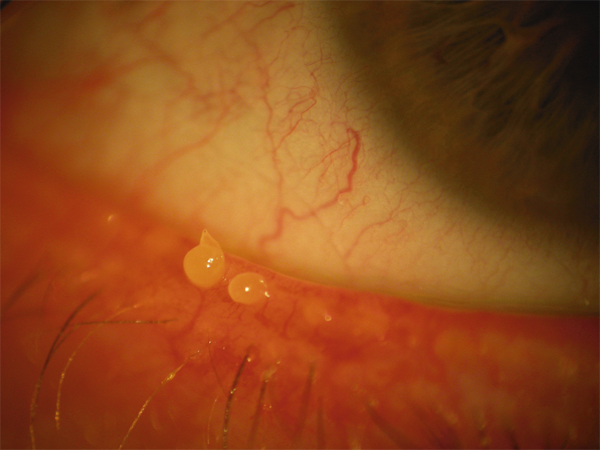
Fig. 4-5 Meibum visqueux objectivé par meibopression.

Fig. 4-6 Larmes mousseuses dans une séborrhée meibomienne.

Fig. 4-7 Télangiectasies sous-cutanées palpébrales antérieures.

Fig. 4-8 Blépharite postérieure.
Dans la blépharite séborrhéique, on note des télangiectasies cutanées, et surtout des collerettes et des croûtes de sébum gras au niveau de la base des cils (fig. 4-9). Les poils palpébraux présentent également parfois le même type de collerettes. Les cils peuvent être fragiles et tomber spontanément. Leur analyse retrouve quelquefois le parasite Demodex, dont le rôle reste incertain [48].
Une surinfection staphylococcique est suspectée en cas d’inflammation [22] avec ulcères du bord libre, sécrétions purulentes, orgelets et chute des cils (fig. 4-10).
L’orgelet est une complication aiguë et correspond à un furoncle d’une glande de Zeiss annexée au follicule pilosébacé ciliaire. Il se manifeste par une pustule blanche douloureuse à la base d’un cil (fig. 4-11).

Fig. 4-9 Collerettes à la base des cils.

Fig. 4-10 Blépharite staphylococcique avec inflammation, croûtes, ulcères du bord libre et perte de cils.
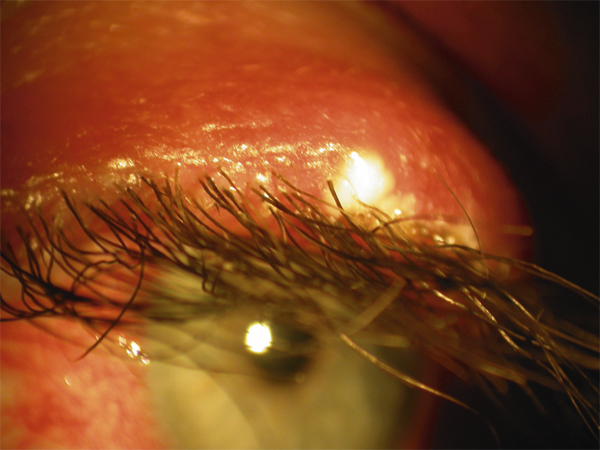
Fig. 4-11 Orgelet.
On retrouve très fréquemment un clignement abortif. Le clignement volontaire est normal, mais le clignement réflexe incomplet. Ceci aggrave la stagnation meibomienne et la kératinisation des méats meibomiens.
Une lagophtalmie avec occlusion volontaire incomplète aura les mêmes conséquences.
Enfin, un trichiasis peut être noté dans les formes avec fibrose conjonctivale.
L’instabilité lacrymale par évaporation excessive est un marqueur important des DGM obstructifs [49]. Le temps de rupture du film lacrymal (break-up time ou BUT) est diminué, inférieur à 10 secondes. Il existe parfois des débris gras dans les larmes. Le test de Schirmer est souvent normal mais peut être abaissé dans les formes évoluées [2]. La vision fluctuante est une conséquence de l’instabilité lacrymale.
Les larmes peuvent aussi former une mousse visible sur le bord libre palpébral inférieur traduisant une séborrhée meibomienne (voir fig. 4-6).
Il existe souvent une hypertrophie papillaire conjonctivale, qui peut faire évoquer à tort une allergie, ainsi que des follicules surtout dans les formes granulomateuses de rosacée.
Une hyperhémie conjonctivale bulbaire fluctuante est habituelle.
Dans la rosacée, une fibrose conjonctivale est classique (fig. 4-12). Elle est en général discrète sous forme de stries blanchâtres sous les conjonctives palpébrales, mais elle est parfois à l’origine de symblépharons et d’un comblement des culs-de-sac conjonctivaux pouvant évoquer une pemphigoïde des muqueuses. Le trichiasis est rare.
Une conjonctivite phlycténulaire (fig. 4-13), se traduisant par des petites phlycténules, levures translucides en tête d’épingle au niveau de la conjonctive bulbaire et du limbe, est plutôt l’apanage de la rosacée du sujet jeune.
Épisclérite et sclérite nodulaire se rencontrent également dans la rosacée. Un bilan systémique s’impose pour éliminer une autre cause d’inflammation. Plus rarement, on peut observer des granulomes conjonctivaux bulbaires dans le cadre d’une rosacée granulomateuse.
L’atteinte inférieure est la plus fréquente et doit faire évoquer un DGM ou une blépharite.
Une kératite ponctuée superficielle est habituelle, banale et non spécifique. Elle peut être accentuée par un clignement abortif ou une malocclusion palpébrale.
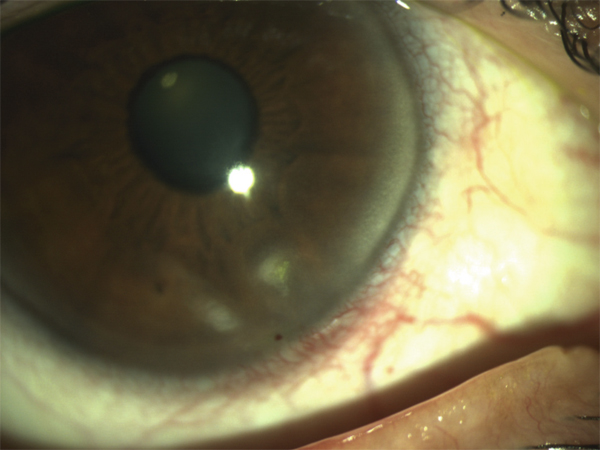
Une insuffisance limbique localisée se traduira par un pannus inférieur accompagné d’un fin pinceau néovasculaire qui est également extrêmement évocateur (fig. 4-14).
Les complications immunologiques cornéennes sévères de la rosacée sont peu fréquentes, mais elles peuvent menacer la vision et l’intégrité cornéenne. Il en existe deux types très caractéristiques de la maladie, les ulcères ou infiltrats catarrhaux et les phlyctènes et phlycténules :
-
les ulcères ou infiltrats catarrhaux sont également appelés infiltrats marginaux staphylococciques stériles (fig. 4-15). Ils apparaissent de façon brutale au limbe et ne doivent pas être confondus avec des abcès cornéens qui sont en pratique beaucoup plus rares. Ils sont arrondis ou ovales de quelques millimètres, blanc grisâtre, avec un espace libre par rapport au limbe. Ils entraînent une photophobie avec douleur et larmoiement intenses. Ils évoluent rarement vers la perforation en l’absence de traitement adapté. Ils laissent des cicatrices cornéennes juxtalimbiques quasiment pathognomoniques (fig. 4-16) qui sont souvent néovascularisées en pinceau ou en éventail, avec un amincissement arciforme ou arrondi en regard d’une taie stromale. Leur siège est classiquement inférieur, et parfois supérieur. Un siège temporal ou nasal doit faire rechercher une autre étiologie comme un port de lentilles de contact ou une vascularite systémique ;
-
les phlyctènes limbiques, également d’apparition rapide mais plus progressive, sont arrondies et blanc rosé. Les phlycténules cornéennes et limbiques sont plus chroniques et ressemblent à celles de la conjonctive. La kératoconjonctivite phlycténulaire, qui affecte l’enfant et l’adulte jeune, tire son nom de ces lésions.
On note plus rarement dans la rosacée des lésions cornéennes chroniques périphériques qui peuvent prendre plusieurs aspects :
-
un amincissement périphérique sectoriel ou circonférentiel pouvant être néovascularisé et s’apparentant à une dégénérescence de Terrien lorsqu’il est chronique ou à un ulcère de Mooren lorsqu’il est aigu ;
-
une dystrophie de la membrane basale périphérique de type Cogan, rarement symptomatique ;
-
des ptérygoïdes (fig. 4-17) qui ont une évolution circonférentielle et centripète et peuvent menacer la vision en l’absence de traitement chirurgical. Elles sont caractérisées par la présence de petites formations kystiques à leur surface et cantonnées au limbe ;
-
des nodules de Salzmann ovalaires en relief, en général périphériques en regard des bords libres palpébraux et menaçant rarement la vision. Ils sont associés à une opacification sous-épithéliale cornéenne et peuvent être aggravés par une malocclusion palpébrale.
S’il est habituel de distinguer les blépharites antérieures des postérieures et les atteintes primitives des atteintes secondaires par inflammation de voisinage, en pratique, toutes ces formes sont souvent diversement associées.
L’âge et la ménopause sont probablement les causes les plus fréquentes de DGM, par le biais de la déficience des sécrétions androgéniques [50]. Le plus souvent, il existe une fibrose cicatricielle méatique glandulaire sans inflammation.
La rosacée qui intéresse la peau et les yeux représente la cause la plus importante de blépharites postérieures ou mixtes. Elle prédomine après 40 ans, elle touche rarement les enfants. Elle est plus fréquente chez la femme (sex-ratio 2/1) et les personnes à carnation claire (peau, iris et cheveux).
L’atteinte oculaire est isolée dans 25 % des cas et est associée à une atteinte cutanée dans 25 % des cas aussi. Dans la moitié des cas restants, la peau est seule concernée mais peut secondairement s’associer à des lésions des yeux.
Les signes cutanés de la rosacée sont liés à des anomalies vasculaires primitives du visage et des phénomènes vasomoteurs [51]. L’érythrose faciale respecte le pourtour des yeux et de la bouche. Les bouffées vasomotrices (ou flushes) sont déclenchées par les boissons et les aliments chauds, l’alcool, les épices, ainsi que la chaleur. La dilatation des petits vaisseaux du derme superficiel entraîne un œdème dermique quasi permanent. L’exposition solaire prolongée augmente ces phénomènes. Les follicules du visage sont le siège d’une colonisation accrue par un parasite saprophyte, le Demodex follicularum. Il entraîne une inflammation folliculaire et périfolliculaire responsable vraisemblablement des papules et des pustules. Mais il existe aussi exceptionnellement de véritables démodécies du visage avec blépharite où le Demodex est très abondant, mais sans signe, notamment vasculaire, de rosacée [52].
On distingue quatre formes d’atteintes cutanées de la rosacée qui peuvent être diversement associées :
-
la forme érythématotélangiectasique qui débute par des flushes laissant place à une érythrose permanente avec couperose surtout des joues et du nez (voir fig. 4-3) ;
-
la forme papulopustuleuse qui se différencie de l’acné vulgaire par l’absence de comédons et de points noirs (fig. 4-18) ;
-
le rhinophyma ou forme granulomateuse centrofaciale à prédominance nasale est plus tardif (fig. 4-19) ;
-
la forme avec rosacée oculaire.
Certains médicaments sont susceptibles d’aggraver une rosacée cutanée et/ou une dermite séborrhéique :
-
les corticoïdes locaux peuvent être à l’origine d’une rosacée stéroïdienne ;
-
les dérivés nicotiniques, les inhibiteurs calciques, les prostacyclines provoquent ou aggravent les phénomènes de flush ;
-
l’isotrétinoïne majore l’érythrose faciale ;
-
certains neuroleptiques augmentent la sécrétion sébacée.
L’atteinte oculaire de la rosacée est extrêmement polymorphe (tableau 4-1). Le DGM est le plus souvent de type obstructif, plus rarement hyperproductif (séborrhée meibomienne), et parfois absent. Les chalazions récidivants doivent faire rechercher la rosacée, en particulier chez l’enfant.
La blépharite est fréquente, postérieure ou mixte (associée à une blépharite séborrhéique), marquée par des télangiectasies du bord libre et de la peau palpébrale.
Outre la sécheresse évaporative chronique, des crises d’inflammation conjonctivale et/ou palpébrale sont classiques.
Tableau 4-1 Signes oculaires de la rosacée
Si la rosacée est considérée comme rare chez l’enfant [53–56], son diagnostic est probablement sous-évalué, pour plusieurs raisons : méconnaissance de l’entité clinique ; absence ou discrétion de l’atteinte cutanée ; pathologie mucocutanée atopique souvent associée masquant la rosacée ; unilatéralité fréquente de l’atteinte oculaire ; aspect cornéen parfois évocateur d’un herpès [57]. Plusieurs appellations sont retrouvées dans la littérature pour désigner la même entité : blépharo-kératoconjonctivite ; kératoconjonctivite phlycténulaire ; kératoconjonctivite meibomienne [58]. La maladie est potentiellement sévère, avec menace pour la vision de l’enfant [59]. Elle peut apparaître dès la naissance, concerne l’enfant mais également le sujet jeune, avec une légère prédilection pour les filles. Un typage HLA-A26, -B35 et -DR8 a été retrouvé avec une plus grande prévalence dans une étude japonaise [60]. L’atteinte oculaire serait plus sévère dans la population indo-pakistanaise [61]. Un terrain atopique est souvent présent.
Les signes cutanés sont très inconstants et volontiers fluctuants, mais restent similaires à ceux de la forme de l’adulte, à l’exception du rhinophyma (voir fig. 4-18) [53, 56]. Chez l’adolescent, la rosacée et l’acné vulgaire peuvent coexister [55], mais dans cette dernière les comédons et les flushes sont absents.
Les signes oculaires d’appel sont les chalazions récidivants, une rougeur oculaire souvent unilatérale, une photophobie, plus rarement une baisse de vision. L’association des deux premiers signes doit faire penser au diagnostic. Au stade initial, on note une blépharite croûteuse et des chalazions. Une amétropie mal corrigée doit être éliminée. La kératoconjonctivite phlycténulaire est inconstante, mais potentiellement sévère. Elle est souvent unilatérale. On note : des phlycténules conjonctivales (voir fig. 4-13), limbiques voire cornéennes ; un pannus cornéen inférieur (fig. 4-20) ; une kératite ponctuée inférieure ; des infiltrats nodulaires superficiels chroniques ressemblant à une kératite de Thygeson et laissant des cicatrices ponctuées (fig. 4-21) ; des infiltrats catarrhaux plus profonds et aigus évoluant rarement vers la perforation mais induisant volontiers des cicatrices néovascularisées parfois astigmatogènes et amblyogènes (fig. 4-22).
Surtout responsable d’une blépharite antérieure, la dermite séborrhéique peut s’associer à une blépharite postérieure avec DMG obstructif ou hyperproductif.
Les anomalies meibomiennes congénitales sont des maladies génétiques rares :
-
les dysplasies ectodermiques sont liées à un défaut de développement du feuillet ectodermique. Il existe fréquemment des troubles de la sudation, une hypotrophie des cheveux et des anomalies de développement dentaire. L’atteinte oculaire associe atrophie meibomienne, hypotrophie des cils et des sourcils (hypotrichose) et syndrome sec évaporatif [62]. Il est décrit parfois une kératoconjonctivite sèche avec insuffisance limbique secondaire. La photophobie est le symptôme le plus souvent rapporté. On peut citer la dysplasie ectodermique hypohydrotique, les syndromes EEC (ectrodactyly-ectodermal dysplasia-cleft) et AEC (ankyloblepharon-ectodermal dysplasia-cleft lip/palate), le KID syndrome (kératite, ichtyose, surdité) ;
-
les ichtyoses congénitales sont également associées à un DGM.
-
L’isotrétinoïne et les rétinoïdes oraux utilisés en dermatologie agissent en atrophiant les glandes sébacées [18]. Le DGM peut être très sévère et persiste parfois malgré l’arrêt du traitement.
-
Les traitements anti-androgéniques et certains contraceptifs oraux induisent un DGM par déficit en androgènes. Une castration chirurgicale aura un effet similaire.
-
Les chimiothérapies anticancéreuses interfèrent avec les cellules en division, en particulier meibomiennes.
-
Le port de lentilles de contact est à l’origine d’un DGM dont le mécanisme n’est pas clair.
Toute inflammation chronique de la conjonctive peut provoquer une blépharite et un DGM par contiguïté :
-
les conjonctivites allergiques chroniques, telles que la conjonctivite perannuelle, la kératoconjonctivite vernale et la kératoconjonctivite atopique, causent toujours à des degrés variables un DGM. Une fibrose conjonctivale et meibomienne peut être associée aux deux dernières entités ;
-
les conjonctivites fibrosantes sévères comme les pemphigoïdes des muqueuses et les syndromes de Stevens-Johnson et de Lyell induisent inflammation et fibrose meibomiennes ;
-
le syndrome de Gougerot-Sjögren et la réaction du greffon contre l’hôte (GVH) peuvent générer un DGM avec blépharite qui aggrave une sécheresse quantitative souvent déjà sévère [63] ;
-
les collyres au long cours, en particulier antiglaucomateux, sont parfois à l’origine d’un DGM de mécanisme toxique ou allergique ;
-
un traumatisme chirurgical comme une chirurgie de la cataracte peut également causer ou décompenser un DGM [64], probablement par toxicité des anesthésiants et désinfectants locaux, des collyres postopératoires et par l’inflammation faisant suite à l’intervention.
Il s’agit de l’atteinte primitive des cils et du bord libre antérieur.
La dermite séborrhéique est une étiologie majeure des blépharites antérieures et mixtes de type séborrhéique. Cette pathologie cutanée est très fréquente et est l’apanage de l’homme adulte. Elle serait plus sévère chez les alcooliques, les parkinsoniens, les patients atteints d’infection par le VIH ou d’un cancer des voies aérodigestives supérieures. Elle est classiquement augmentée par les contrariétés, le stress, le surmenage et la fatigue qui semblent stimuler la sécrétion sébacée.
Le sébum est un bon milieu de culture pour une levure : Malassezia furfur. Sa prolifération est vraisemblablement à l’origine des signes cliniques de la dermite séborrhéique que sont la rougeur, les petites squames grasses et parfois la démangeaison. La symptomatologie peut être fugace et ses éléments doivent être recherchés à l’interrogatoire.
L’atteinte cutanée prédomine, comme le suggère son nom, dans les zones où les glandes sébacées sont abondantes [65] : visage – front, sourcils, nez, oreilles et bord libre des paupières (fig. 4-23), cuir chevelu, région présternale et dos.
L’atteinte oculaire est une blépharite séborrhéique qui est souvent associée à un DMG obstructif ou à une séborrhée meibomienne. Les symptômes oculaires et palpébraux peuvent être très marqués. Le prurit et les sensations de brûlure du bord libre palpébral sont évocateurs. On retrouve des croûtes et collerettes de sébum à la base des cils, mais aussi des poils palpébraux. Des larmes mousseuses témoignent d’une séborrhée meibomienne.
Les blépharites fongiques en particulier à Malassezia furfur peuvent avoir la même apparence clinique, mais sont en pratique rares [35].

Fig. 4-23 Dermite séborrhéique du visage.
Des manifestations oculaires intéressent 10 % des psoriasiques et sont plus fréquentes en cas d’atteinte articulaire associée. Il s’agit d’une blépharite antérieure volontiers squameuse, d’une conjonctivite, d’une sécheresse oculaire, d’une kératite ou d’une uvéite. Une blépharite peut être observée de manière isolée avec les rhumatismes psoriasiques.
Il existe des formes de sébopsoriasis (avec blépharite) notamment dans le sida ; elles sont, parfois difficiles à distinguer d’une dermite séborrhéique, mais le diagnostic est évoqué devant les squames normalement plus épaisses et les localisations des lésions érythématosquameuses qui sont spécifiques du psoriasis : cuir chevelu, conduits auditifs externes, coudes, genoux, région sacrée, ongles [66]. Les traitements de type rétinoïdes, comme l’isotrétinoïne, utilisés pour les formes sévères, peuvent aggraver le DGM en induisant une atrophie meibomienne.
L’entité même des blépharites infectieuses est discutée, car la responsabilité d’agents comme le staphylocoque et le Demodex en tant que causes primitives est controversée.
Elle se traduit par une inflammation marquée du bord libre prédominant classiquement sur son versant antérieur, même si l’on note souvent une atteinte postérieure associée. Il existe des croûtes à la base des cils qui peuvent chuter, et éventuellement des ulcères du bord libre et des orgelets. Infiltrats catarrhaux, kératoconjonctivite phlycténulaire et sclérite/épisclérite sont des complications immunologiques de cette surinfection. Il est à noter qu’une infection par Propionibacterium acnes peut entraîner un tableau similaire.
Très controversée, la blépharite à Demodex se manifeste surtout par une forme antérieure de type séborrhéique, avec présence de croûtes et collerettes de sébum à la base des cils [48].
Elles sont rares, chroniques et marquées en particulier par des ulcères du bord libre. Divers germes ont été rapportés, comme Candida albicans, surtout chez les atopiques [67], ou Malassezia furfur [35]. Quelques rares cas de blépharites trichophytiques ou microsporiques ont été décrits [68]. Elles peuvent s’accompagner d’une teigne tondante des cils.
Elle est liée à l’infestation par le parasite Pediculus hominis (pou de tête ou du corps) ou plus souvent par Phtyrius pubis (pou du pubis). Elle peut réaliser un tableau trompeur de blépharite antérieure croûteuse très prurigineuse. Les cils sont parsemés de lentes. Les poux sont accrochés entre deux cils. La contamination s’effectue par contact avec un sujet infesté (maladie sexuellement transmissible ou MST), avec ses affaires personnelles ou la literie. Le traitement repose sur l’ablation des poux et des lentes à la pince, après application d’une pommade visant à les asphyxier.
En cas de dermatite atopique avec atteinte palpébrale, une blépharite antérieure est presque constante. Une surinfection à staphylocoque n’est pas rare, on retrouve par contre moins souvent une surinfection à Candida.
Le lupus érythémateux chronique discoïde intéresse fréquemment le visage, le cuir chevelu, les oreilles. L’atteinte des paupières sous la forme d’une blépharite chronique est moins habituelle [69]. Elle est rarement isolée, mais peut alors entraîner un retard diagnostique responsable de lésions cicatricielles définitives et de complications oculaires. La paupière inférieure est atteinte dans son tiers externe, avec présence des trois lésions élémentaires du lupus érythémateux chronique : l’érythème parfois télangiectasique, l’hyperkératose ponctuée et plus tardivement l’atrophie [69].
Ce poxvirus est responsable de nodules cutanés à centre ombiliqué pouvant siéger sur toute la paupière dont le bord libre. Le tableau est souvent trompeur si le Molluscum n’est pas vu. On note classiquement une blépharite antérieure très croûteuse avec conjonctivite folliculaire et phlycténulaire chronique asymétrique, parfois une eczématisation cutanée et rarement une atteinte cornéenne. Il touche les enfants et les immunodéprimés, se transmet par contact et grattage du Molluscum (auto-inoculation). Le traitement repose sur l’ablation des lésions par curetage, chirurgie ou laser.
Les autres infections cutanées palpébrales virales, en particulier herpes simplex virus (HSV) ou varicella-zoster virus (VZV), ou bactériennes peuvent également provoquer une blépharite antérieure souvent croûteuse.
Les examens complémentaires ne sont pas indispensables pour le diagnostic des DGM qui est avant tout clinique. Ils permettent cependant d’affiner le bilan en procurant des données chiffrées et ont pour certains un intérêt pour la recherche clinique.
La meibographie permet d’examiner in vivo la morphologie et la distribution des glandes de Meibomius. Il existe deux méthodes, une par transillumination de la paupière éversée grâce à une source lumineuse appliquée au contact de la paupière, l’autre, sans contact par éclairage direct infrarouge (650–700 nm). Plusieurs dispositifs médicaux sans contact couplés à une caméra infrarouge sont sur le marché tel le système Cobra avec le logiciel Phoenix®, les systèmes Topcon BG-4M®, Eyetop®, Sirius®, Oculus® ou la fibre optique L-3920® (Inami). L’appareil LipiView® combine une image infrarouge et une transillumination.
Les glandes normales sont hyporéflectives et apparaissent sous forme de grappes de raisin avec des acini (fig. 4-24). Les canaux et orifices sont hyperréflectifs entourés par les acini glandulaires. Certains appareils proposent un logiciel qui permet une quantification en calculant semi-automatiquement la surface des glandes visibles par rapport à celle de la paupière [70]. Les résultats de la meibographie semblent corrélés aux symptômes, au BUT et à l’épaisseur du film lipidique [71].
La tomographie par cohérence optique (optical coherence tomography ou OCT) et l’ophtalmoscopie à balayage laser (scanning laser ophthalmoscopy ou SLO) permettraient également de réaliser une meibographie infrarouge, mais ces techniques sont peu développées pour le moment [72].
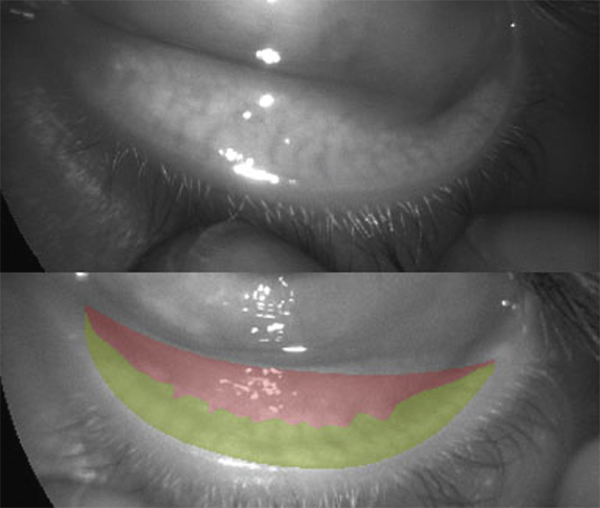
Fig. 4-24 Meibographie en infrarouge. Visualisation des glandes de Meibomius après segmentation (en vert).
L’IVCM a été utilisée pour visualiser les glandes de Meibomius. En cas de DGM, on note en particulier une diminution de la densité et une augmentation du diamètre des acini meibomiens (fig. 4-25), et éventuellement une inflammation périglandulaire [73, 74]. Ces modifications sont corrélées à l’obstruction meibomienne retrouvée à l’examen clinique, avec d’excellentes sensibilité et spécificité. Les Demodex peuvent aussi être observés par cette méthode, sur les cils mais également dans les glandes meibomiennes et les follicules pilosébacés annexés aux cils. L’IVCM permet enfin d’évaluer l’effet des traitements du DGM.
La technique d’interférométrie du film lacrymal en lumière froide permet d’estimer l’épaisseur de la composante lipidique in vivo. Une lumière blanche projetée obliquement génère des franges colorées dites interférométriques lorsqu’elle traverse le film lipidique et est réfléchie par l’interface lipides/eau. La couleur de chaque frange est un reflet de l’épaisseur du film lipidique. On peut également évaluer sa qualité grâce à l’observation dynamique des franges interférométriques.
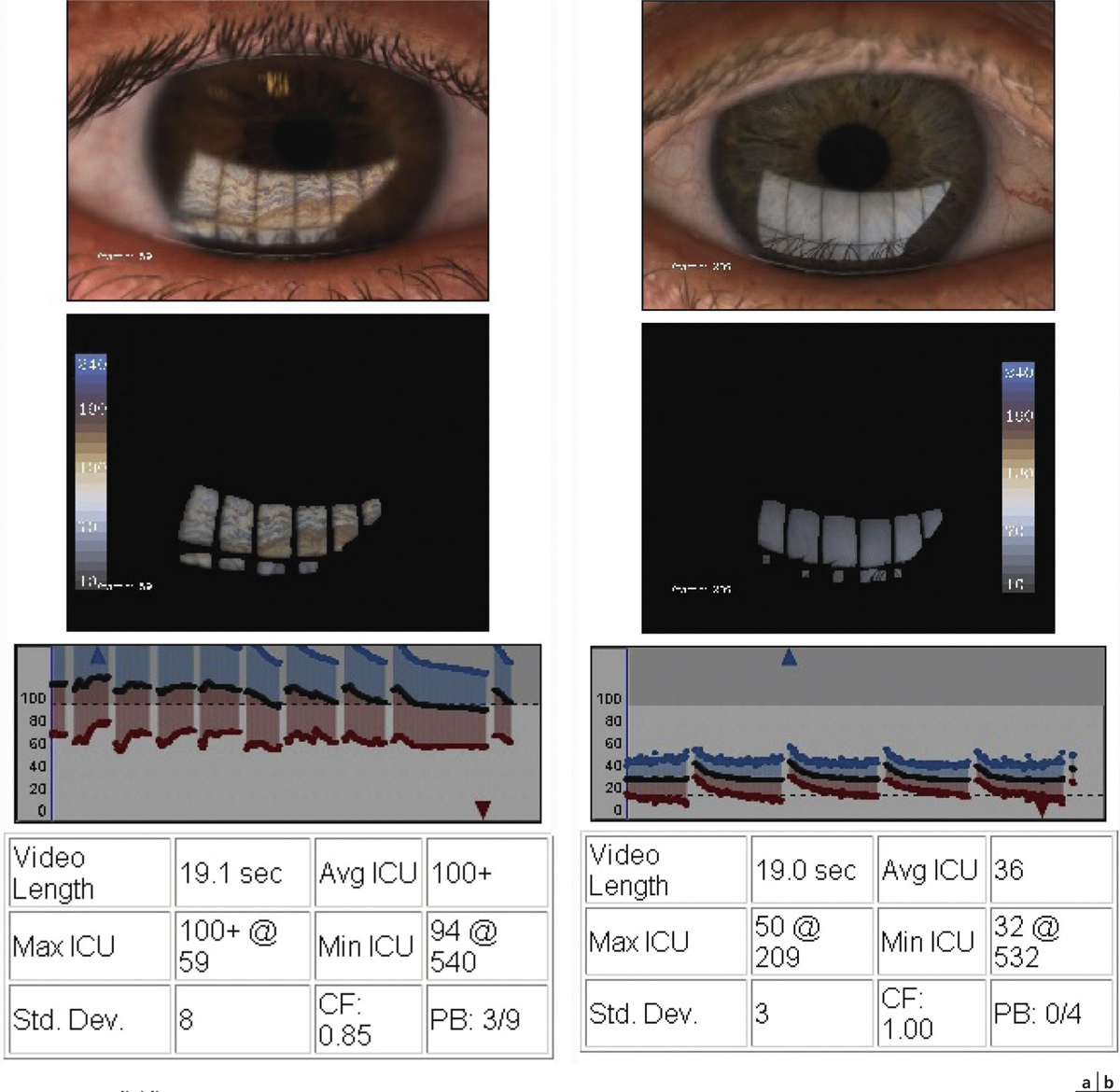
Plusieurs modèles existent : Tearscope® (Keeler), DR1® (Kowa) et, plus récemment, LipiView® (TearScience). Ce dernier appareil permet d’enregistrer une vidéo de 19 secondes par œil et de traiter 14 millions de pixels par seconde. Un film lipidique normal d’épaisseur supérieure à 100 nm génère des franges d’interférence très colorées (fig. 4-26a). Lorsqu’il est pauvre, d’épaisseur inférieure à 60 nanomètres, les images sont uniformément grises (fig. 4-26b) [75]. Le LipiView® mesure l’épaisseur moyenne du film lipidique sur l’hémicornée inférieure et suit ses modifications au cours du clignement. L’appareil évalue automatiquement la qualité de ce dernier en fournissant le pourcentage de clignements abortifs.
Elle s’effectue avant tout en prélevant huit à dix cils par côté, si possible ceux comportant des croûtes ou des collerettes. On peut utiliser l’alcool absolu, la potasse ou la fluorescéine (méthode Couston) pour mobiliser les Demodex et dissoudre les croûtes [76]. L’observation se fait entre lame et lamelle (voir fig. 4-1). Le seuil de positivité du prélèvement n’est pas consensuel : au-delà de cinq Demodex pour dix cils pour certains, au-delà de trois Demodex pour un cil pour d’autres [77]. L’IVCM [78] et la polymerase chain reaction (PCR) sont également en cours d’évaluation pour l’apport diagnostique.
Elle n’est utile qu’en cas d’échec thérapeutique ou de suspicion de germe atypique en particulier fongique.
Après prélèvement puis séparation, les lipides meibomiens peuvent être identifiés par méthodes chimiques ou par spectrométrie de masse qui est la méthode la plus employée pour des analyses globales. La lipidomique est une méthode d’avenir pour déterminer de façon exhaustive la composition lipidique du meibum ou des larmes [20].
Les DGM et les blépharites sont probablement les pathologies de la surface oculaire les plus communément rencontrées, car pouvant être primitives ou s’intégrant dans d’autres pathologies inflammatoires. L’examen clinique est capital pour établir le diagnostic et classer l’atteinte dans les différents cadres nosologiques. Les examens complémentaires peuvent apporter des critères objectifs et éventuellement guider l’étiologie.
[1] Tong L, Chaurasia SS, Mehta JS, et al. Screening for meibomian gland disease : its relation to dry eye subtypes and symptoms in a tertiary referral clinic in singapore. Invest Ophthalmol Vis Sci 2010 ; 51 : 3449-54.
[2] Lemp MA, Mahmood MA, Weiler HH. Association of rosacea and keratoconjunctivitis sicca. Arch Ophthalmol 1984 ; 102 : 556-7.
[3] Lemp MA, Nichols KK. Blepharitis in the United States 2009 : a survey-based perspective on prevalence and treatment. Ocul Surf 2009 ; 7 : S1-S14.
[4] Viso E, Rodriguez-Ares MT, Abelenda D, et al. Prevalence of asymptomatic and symptomatic meibomian gland dysfunction in the general population of Spain. Invest Ophthalmol Vis Sci 2012 ; 53 : 2601-6.
[5] Schein OD, Munoz B, Tielsch JM, et al. Prevalence of dry eye among the elderly. Am J Ophthalmol 1997 ; 124 : 723-8.
[6] Jie Y, Xu L, Wu YY, et al. Prevalence of dry eye among adult Chinese in the Beijing Eye Study. Eye (Lond) 2009 ; 23 : 688-93.
[7] Hom MM, Martinson JR, Knapp LL, et al. Prevalence of Meibomian gland dysfunction. Optom Vis Sci 1990 ; 67 : 710-2.
[8] Schaumberg DA, Nichols JJ, Papas EB, et al. The international workshop on meibomian gland dysfunction : report of the subcommittee on the epidemiology of, and associated risk factors for, MGD. Invest Ophthalmol Vis Sci 2011 ; 52 : 1994-2005.
[9] Aubart-Cohen F, Klein I, Alexandra JF, et al. Long-term outcome in Susac syndrome. Medicine (Baltimore) 2007 ; 86 : 93-102.
[10] Lemp MA, Crews LA, Bron AJ, et al. Distribution of aqueous-deficient and evaporative dry eye in a clinic-based patient cohort : a retrospective study. Cornea 2012 ; 31 : 472-8.
[11] Hoang-Xuan T, Baudouin C, Creuzot-Garcher C. Ocular rosacea. In : Inflammatory diseases of the conjunctiva. Stuttgart-New York : Thieme ; 2001, p. 97-108.
[12] Gupta N, Dhawan A, Beri S, et al. Clinical spectrum of pediatric blepharokeratoconjunctivitis. J AAPOS 2010 ; 14 : 527-9.
[13] Hammersmith KM, Cohen EJ, Blake TD, et al. Blepharokeratoconjunctivitis in children. Arch Ophthalmol 2005 ; 123 : 1667-70.
[14] Bron AJ, Tiffany JM. The meibomian glands and tear film lipids. Structure, function, and control. Adv Exp Med Biol 1998 ; 438 : 281-95.
[15] McCulley JP, Shine WE. Meibomian gland function and the tear lipid layer. Ocul Surf 2003 ; 1 : 97-106.
[16] Sullivan DA, Sullivan BD, Ullman MD, et al. Androgen influence on the meibomian gland. Invest Ophthalmol Vis Sci 2000 ; 41 : 3732-42.
[17] Knop E, Knop N, Millar T, et al. The international workshop on meibomian gland dysfunction : report of the subcommittee on anatomy, physiology, and pathophysiology of the meibomian gland. Invest Ophthalmol Vis Sci 2011 ; 52 : 1938-78.
[18] Lambert RW, Smith RE. Pathogenesis of blepharoconjunctivitis complicating 13-cis-retinoic acid (isotretinoin) therapy in a laboratory model. Invest Ophthalmol Vis Sci 1988 ; 29 : 1559-64.
[19] Kellum RE. Acne vulgaris. Studies in pathogenesis : relative irritancy of free fatty acids from C2 to C16. Arch Dermatol 1968 ; 97 : 722-6.
[20] Lam SM, Tong L, Reux B, et al. Lipidomic analysis of human tear fluid reveals structure-specific lipid alterations in dry eye syndrome. J Lipid Res 2014 ; 55 : 299-306.
[21] Yactayo-Miranda Y, Ta CN, He L, et al. A prospective study determining the efficacy of topical 0.5 % levofloxacin on bacterial flora of patients with chronic blepharoconjunctivitis. Graefes Arch Clin Exp Ophthalmol 2009 ; 247 : 993-8.
[22] McCulley JP, Dougherty JM, Deneau DG. Classification of chronic blepharitis. Ophthalmology 1982 ; 89 : 1173-80.
[23] Dougherty JM, McCulley JP. Comparative bacteriology of chronic blepharitis. Br J Ophthalmol 1984 ; 68 : 524-8.
[24] Dougherty JM, McCulley JP. Bacterial lipases and chronic blepharitis. Invest Ophthalmol Vis Sci 1986 ; 27 : 486-91.
[25] Baudouin C. Revisiter les dysfonctionnements meibomiens. J Fr Ophtalmol 2014 ; sous presse.
[26] Shine WE, Silvany R, McCulley JP. Relation of cholesterol-stimulated Staphylococcus aureus growth to chronic blepharitis. Invest Ophthalmol Vis Sci 1993 ; 34 : 2291-6.
[27] Mondino BJ, Kowalski RP. Phlyctenulae and catarrhal infiltrates. Occurrence in rabbits immunized with staphylococcal cell walls. Arch Ophthalmol 1982 ; 100 : 1968-71.
[28] Del Rosso JQ, Webster GF, Jackson M, et al. Two randomized phase III clinical trials evaluating anti-inflammatory dose doxycycline (40-mg doxycycline, USP capsules) administered once daily for treatment of rosacea. J Am Acad Dermatol 2007 ; 56 : 791-802.
[29] Lacey N, Ni Raghallaigh S, Powell FC. Demodex mites--commensals, parasites or mutualistic organisms ? Dermatology 2011 ; 222 : 128-30.
[30] Elston DM. Demodex mites : facts and controversies. Clin Dermatol 2010 ; 28 : 502-4.
[31] Norn MS. Demodex folliculorum. Incidence and possible pathogenic role in the human eyelid. Acta Ophthalmol Suppl 1970 ; 108 : 7-85.
[32] Georgala S, Katoulis AC, Kylafis GD, et al. Increased density of Demodex folliculorum and evidence of delayed hypersensitivity reaction in subjects with papulopustular rosacea. J Eur Acad Dermatol Venereol 2001 ; 15 : 441-4.
[33] Jarmuda S, O’Reilly N, Zaba R, et al. Potential role of Demodex mites and bacteria in the induction of rosacea. J Med Microbiol 2012 ; 61 : 1504-10.
[34] Sacca SC, Pascotto A, Venturino GM, et al. Prevalence and treatment of Helicobacter pylori in patients with blepharitis. Invest Ophthalmol Vis Sci 2006 ; 47 : 501-8.
[35] Derbel M, Benzina Z, Ghorbel I, et al. Blépharite mycosique à Malassezia : à propos d’un cas. J Fr Ophtalmol 2005 ; 28 : 862-5.
[36] Gutgesell VJ, Stern GA, Hood CI. Histopathology of meibomian gland dysfunction. Am J Ophthalmol 1982 ; 94 : 383-7.
[37] Hykin PG, Bron AJ. Age-related morphological changes in lid margin and meibomian gland anatomy. Cornea 1992 ; 11 : 334-42.
[38] Pelegrino FS, Pflugfelder SC, De Paiva CS. Low humidity environmental challenge causes barrier disruption and cornification of the mouse corneal epithelium via a c-jun N-terminal kinase 2 (JNK2) pathway. Exp Eye Res 2012 ; 94 : 150-6.
[39] Pisella PJ, Brignole F, Debbasch C, et al. Flow cytometric analysis of conjunctival epithelium in ocular rosacea and keratoconjunctivitis sicca. Ophthalmology 2000 ; 107 : 1841-9.
[40] Abu el Asrar AM, Geboes K, Maudgal PC, et al. Immunocytological study of phlyctenular eye disease. Int Ophthalmol 1987 ; 10 : 33-9.
[41] Hoang-Xuan T, Rodriguez A, Zaltas MM, et al. Ocular rosacea. A histologic and immunopathologic study. Ophthalmology 1990 ; 97 : 1468-75.
[42] Huet E, Vallee B, Delbe J, et al. EMMPRIN modulates epithelial barrier function through a MMP-mediated occludin cleavage : implications in dry eye disease. Am J Pathol 2011 ; 179 : 1278-86.
[43] Afonso AA, Sobrin L, Monroy DC, et al. Tear fluid gelatinase B activity correlates with IL-1alpha concentration and fluorescein clearance in ocular rosacea. Invest Ophthalmol Vis Sci 1999 ; 40 : 2506-12.
[44] Barton K, Monroy DC, Nava A, et al. Inflammatory cytokines in the tears of patients with ocular rosacea. Ophthalmology 1997 ; 104 : 1868-74.
[45] Sobrin L, Liu Z, Monroy DC, et al. Regulation of MMP-9 activity in human tear fluid and corneal epithelial culture supernatant. Invest Ophthalmol Vis Sci 2000 ; 41 : 1703-9.
[46] Nelson JD, Shimazaki J, Benitez-del-Castillo JM, et al. The International Workshop on Meibomian Gland Dysfunction : report of the definition and classification subcommittee. Invest Ophthalmol Vis Sci, Special Issue 2011 ; 52 : 1930-7.
[47] Blackie CA, Korb DR, Knop E, et al. Nonobvious obstructive meibomian gland dysfunction. Cornea 2010 ; 29 : 1333-45.
[48] Gao YY, Di Pascuale MA, Li W, et al. High prevalence of Demodex in eyelashes with cylindrical dandruff. Invest Ophthalmol Vis Sci 2005 ; 46 : 3089-94.
[49] The Definition and Classication of Dry Eye Disease : report of the definition and classication subcommittee of the International Dry Eye Workshop (2007). Ocul Surf 2007 ; 5 : 75-95.
[50] Tamer C, Oksuz H, Sogut S. Androgen status of the nonautoimmune dry eye subtypes. Ophthalmic Res 2006 ; 38 : 280-6.
[51] Jansen T. Formes cliniques et classification de la rosacée. Ann Dermatol Venereol 2011 ; 138 : S138-147.
[52] Anane S, Mokni M, Beltaief O. Démodécie rosacéiforme et blépharite chronique. Ann Dermatol Venereol 2011 ; 138 : 30-4.
[53] Chamaillard M, Mortemousque B, Boralevi F, et al. Cutaneous and ocular signs of childhood rosacea. Arch Dermatol 2008 ; 144 : 167-71.
[54] Lacz NL, Schwartz RA. Rosacea in the pediatric population. Cutis 2004 ; 74 : 99-103.
[55] Erzurum SA, Feder RS, Greenwald MJ. Acne rosacea with keratitis in childhood. Arch Ophthalmol 1993 ; 111 : 228-30.
[56] Bourrat E, Rybojad M, Deplus S, et al. Rosacea with ocular involvement in a child. Ann Dermatol Venereol 1996 ; 123 : 664-5.
[57] Doan S. Inflammation de la surface oculaire – Sécheresse oculaire. In : Dureau P. Ed. Opthalmologie pédiatrique et strabismes – Segment antérieur. Paris : Lavoisier ; 2014, p. 53-60.
[58] Suzuki T. Meibomitis-related keratoconjunctivitis : implications and clinical significance of meibomian gland inflammation. Cornea 2012 ; 31 Suppl 1 : S41-44.
[59] Doan S, Gabison EE, Nghiem-Buffet S, et al. Long-term visual outcome of childhood blepharokeratoconjunctivitis. Am J Ophthalmol 2007 ; 143 : 528-9.
[60] Suzuki T, Mitsuishi Y, Sano Y, et al. Phlyctenular keratitis associated with meibomitis in young patients. Am J Ophthalmol 2005 ; 140 : 77-82.
[61] Viswalingam M, Rauz S, Morlet N, et al. Blepharokeratoconjunctivitis in children : diagnosis and treatment. Br J Ophthalmol 2005 ; 89 : 400-3.
[62] Kaercher T. Ocular symptoms and signs in patients with ectodermal dysplasia syndromes. Graefes Arch Clin Exp Ophthalmol 2004 ; 242 : 495-500.
[63] Shimazaki J, Goto E, Ono M, et al. Meibomian gland dysfunction in patients with Sjogren syndrome. Ophthalmology 1998 ; 105 : 1485-8.
[64] Han KE, Yoon SC, Ahn JM, et al. Evaluation of dry eye and meibomian gland dysfunction after cataract surgery. Am J Ophthalmol 2014 ; 157 : 1144-50.e1.
[65] Collège des enseignants de dermato-vénéréologie de France. Dermatite séborrhéique. Ann Dermatol Venereol 2003 ; 130 : 186-8.
[66] Cribier B. Psoriasis : formes rares ou inhabituelles. Ann Dermatol Venereol 2012 ; 139 : S39-45.
[67] Huber-Spitzy V, Bohler-Sommeregger K, Rocker-Mettinger E, et al. Ulcerative blepharitis in atopic patients--is Candida species the causative agent ? Br J Ophthalmol 1992 ; 76 : 272-4.
[68] Creach P, Auffret N, Buot G, et al. Teigne tondante ciliaire et blépharite à Microsporum canis. Ann Dermatol Venereol 1995 ; 122 : 773-4.
[69] Panse I, Cordoliani F, Rybojad M, et al. Discoid lupus erythematosus involving the eyelids : 4 cases. Ann Dermatol Venereol 2004 ; 131 : 58-60.
[70] Pult H, Nichols JJ. A review of meibography. Optom Vis Sci 2012 ; 89 : E760-769.
[71] Pult H, Riede-Pult BH, Nichols JJ. Relation between upper and lower lids’ meibomian gland morphology, tear film, and dry eye. Optom Vis Sci 2012 ; 89 : E310-315.
[72] Hwang HS, Park CW, Joo CK. Novel noncontact meibography with anterior segment optical coherence tomography : Hosik meibography. Cornea 2013 ; 32 : 40-3.
[73] Matsumoto Y, Sato EA, Ibrahim OM, et al. The application of in vivo laser confocal microscopy to the diagnosis and evaluation of meibomian gland dysfunction. Mol Vis 2008 ; 14 : 1263-71.
[74] Ibrahim OM, Matsumoto Y, Dogru M, et al. The efficacy, sensitivity, and specificity of in vivo laser confocal microscopy in the diagnosis of meibomian gland dysfunction. Ophthalmology 2010 ; 117 : 665-72.
[75] Finis D, Pischel N, Borrelli M, et al. Factors influencing the measurement of tear film lipid layer thickness with interferometry. Klin Monbl Augenheilkd 2014 ; 231 : 603-10.
[76] Batellier L, Doan S, Brignole-Baudouin F, et al. Diagnostic biologique des conjonctivites. Encycl Méd Chir (Elsevier, Paris). Ophtalmologie, 21-130-B-10. 2011.
[77] Salem DA, El-Shazly A, Nabih N, et al. Evaluation of the efficacy of oral ivermectin in comparison with ivermectin-metronidazole combined therapy in the treatment of ocular and skin lesions of Demodex folliculorum. Int J Infect Dis 2013 ; 17 : e343-347.
[78] Randon M, Liang H, El Hamdaoui M, et al. In vivo confocal microscopy as a novel and reliable tool for the diagnosis of Demodex eyelid infestation. Br J Ophthalmol 2014 ; sous presse.