Explorations
M. M’Garrech, A. Rousseau, E. Barreau, M. Labetoulle
L’interrogatoire, complet et méthodique, éventuellement à l’aide de questionnaires, est un temps indispensable dans l’examen clinique des pathologies de la surface oculaire (PSO). Il est possible de profiter de ce temps pour réaliser une inspection générale du patient, en lumière ambiante (aspect de la peau du visage et état des paupières). L’examen biomicroscopique de la surface de l’œil permet à la fois le diagnostic positif et l’estimation du niveau de gravité. L’instillation de fluorescéine donne des indications sur la gravité et les mécanismes pathogéniques des atteintes épithéliales, et permet d’estimer la stabilité des larmes. L’examen des paupières est un complément indispensable de l’examen clinique, car les dysfonctionnements des glandes de Meibomius (DGM) sont très fréquents dans les PSO. Les tests de production lacrymale (test de Schirmer I surtout) et la mesure de la sensibilité cornéenne restent des examens d’actualité, notamment dans les formes sévères.
Un examen clinique complet est bien entendu le temps indispensable et primordial de la prise en charge des patients souffrant de pathologies de la surface oculaire (SPO). On peut distinguer quatre étapes dans cet examen clinique : l’interrogatoire, l’inspection, l’examen à la lampe à fente et les tests des fonctions lacrymales. Sur le plan pratique, la séquence diagnostique des pathologies de la surface oculaire est résumée dans l’encadré 2-1 [1].
• Inspection générale
• Histoire clinique et description des symptômes
• Analyse de l’épithélium cornéen et conjonctival sans colorants
• BUT (break-up time) à la fluorescéine (si possible avec filtre jaune)
• Analyse de l’épithélium cornéen et conjonctival et de la qualité des larmes, avec la fluorescéine (± vert de lissamine)
• Éventuellement, test de Schirmer en fonction du contexte
• Examen clinique des paupières (et des glandes de Meibomius selon le contexte)
• Synthèse de l’ensemble des données
Comme souvent en médecine, un interrogatoire efficace permet de gagner un temps précieux pour poser le bon diagnostic : le temps consacré à cette étape cruciale n’est jamais perdu sur le long terme. Il convient donc de ne pas négliger ce temps d’écoute. Une des principales astuces est justement de commencer l’interrogatoire en laissant le patient exprimer spontanément sa plainte, il choisit ainsi d’abord ses mots pour décrire la gêne ressentie et l’histoire de sa maladie. Le médecin avisé prendra ensuite la main sur les échanges, en précisant les symptômes, puis en orientant l’interrogatoire par des questions explorant telle ou telle hypothèse diagnostique, tout en évitant d’être trop directif ou suggestif.
Les signes fonctionnels doivent être relevés précisément, à la fois dans leur nature et leur calendrier éventuel.
La rougeur oculaire peut être alternativement considérée comme un signe physique ou fonctionnel, car les patients s’en plaignent spontanément et elle n’est pas toujours continue dans la journée, selon les étiologies. Sa recherche fait donc aussi partie de l’interrogatoire.
L’intensité de la rougeur et sa localisation (diffuse ou focale, uni- ou bilatérale) sont autant d’éléments importants pour l’orientation diagnostique [2]. Il convient d’ailleurs de rappeler qu’une rougeur périkératique a une valeur sémiologique forte, puisque dans le cadre des PSO, elle oriente d’emblée vers une kératite épithéliale.
Il est logique de constater une certaine baisse de vision dans les atteintes de la surface de l’œil, à condition cependant qu’elles touchent la cornée. Le degré de BAV dépend de l’importance des lésions et de leur situation par rapport au centre optique (une atteinte dans les 3 mm centraux étant un signe de gravité). Le patient peut aussi décrire une sensation de perte de qualité optique, alors même que la mesure avec les échelles classiques retrouve une acuité visuelle à 10/10. Les techniques de mesure des aberrations optiques et de diffusion de la lumière ont démontré que ces patients présentent effectivement des anomalies de la perception visuelle [3, 4] qui peuvent d’ailleurs largement être aggravées par la survenue ultérieure d’une sécheresse oculaire. De plus, l’acuité visuelle peut subir des pertes rapides entre les clignements dans les sécheresses oculaires modérées à sévères, ce qui explique ces sensations de fluctuation optique ou de brouillard décrites par les patients et qui disparaissent temporairement en clignant des yeux [5].
Souvent mentionnée spontanément, la notion de douleur est souvent confondue avec des sensations d’inconfort, de gêne. Les anomalies de surface génèrent plutôt des douleurs superficielles (sensation de corps étranger, de brûlure, etc.), mais les syndromes inflammatoires sévères, les sclérites notamment, entraînent typiquement des douleurs plus profondes, lancinantes, voire insomniantes. Associé à une kératite apparemment isolée, ce type de douleurs est aussi très évocateur d’une origine amibienne, responsable d’une kératonévrite. Les douleurs dépassant le strict cadre de l’orbite peuvent orienter le diagnostic, comme les douleurs ou paresthésies du scalp, dans le cadre d’un zona ophtalmique [6]. Des céphalées sus-orbitaires, intermittentes et répétitives, augmentant avec les efforts visuels, orientent vers des troubles de la réfraction, dont on sait qu’ils peuvent aussi se manifester sous formes d’anomalies de la surface.
Ces trois sensations sont assez liées en pratique, mais certains patients évoquent plus volontiers l’une ou l’autre. Elles sont très évocatrices d’une atteinte épithéliale, conjonctivale et/ou cornéenne. Lorsqu’elles sont chroniques et progressent au fur et à mesure de la journée, elles évoquent volontiers un mécanisme de sécheresse oculaire avec une forte composante d’insuffisance de sécrétion [7]. À l’inverse, un maximum des signes au lever évoquerait plutôt une atteinte palpébrale de type meibomite (pas d’effet de rinçage pendant la nuit). Cette différence n’est cependant pas d’une fiabilité absolue.
Lorsque ces sensations apparaissent brutalement, associées à des sécrétions mucopurulentes, elles évoquent une conjonctivite infectieuse ; lorsque leur intensité confine à une réelle sensation douloureuse et s’accompagne d’une photophobie, elles évoquent une atteinte cornéenne.
Le patient peut évoquer directement la sensation de manquer de larmes, d’avoir l’œil sec ou lourd, ou encore « gluant » ou « cireux », le tout évoquant manifestement un manque de lubrification. Mais paradoxalement, ces symptômes ne font pas partie de ceux les plus fréquemment cités de façon spontanée par les patients réellement atteints de syndrome de l’œil sec. Par ailleurs, ils ne sont pas pathognomoniques, et un patient allergique peut les éprouver, notamment en cas d’atteinte chronique.
La gêne à la lumière est nettement plus fréquente que la véritable photophobie. Cette dernière est classique dans les syndromes algiques majeurs du segment antérieur, comme les kératites épithéliales, mais aussi certaines uvéites aiguës très sévères et les crises d’hypertonie par fermeture de l’angle. La simple gêne à la lumière évoque plutôt une altération avancée de l’épithélium conjonctival et/ou une altération modérée de l’épithélium cornéen. N’oublions pas de citer le diagnostic différentiel des douleurs (dont des céphalées) avec photophobie qui accompagnent les syndromes méningés.
Il s’agit le plus souvent d’un larmoiement réflexe, en réponse à une agression directe de la surface oculaire. Il est donc quasi constant dans les suites d’un traumatisme cornéen ou conjonctival, et son caractère inextinguible doit faire évoquer la persistance d’un corps étranger, enfiché dans la cornée ou dans la conjonctivale tarsale supérieure.
Le larmoiement est aussi constant, ou presque, dans les infections (conjonctivites, kératites), de même que pendant les phases de recrudescence d’une atteinte allergique. Lorsqu’il est chronique et sans autre signe d’appel, les voies lacrymales doivent être explorées. Enfin, rappelons la valeur sémiologique du larmoiement clair dans les glaucomes congénitaux.
De façon paradoxale, le larmoiement peut aussi être décrit par les patients débutant un syndrome de sécheresse oculaire, notamment quand il existe déjà une inflammation des tissus de la surface oculaire (par meibomite, syndrome de Gougerot-Sjögren, etc.) mais pas encore la baisse de sensibilité cornéenne. Le larmoiement est alors typiquement aggravé par l’exposition aux agressions, comme le froid, l’air climatisé et surtout le vent. Il s’agit là encore d’un larmoiement réflexe qui, malheureusement pour le patient, va s’estomper au fur et à mesure que la maladie s’installe.
Ce sont les deux aspects de la réponse de la surface oculaire à une agression aiguë. Ils peuvent être rencontrés dans les allergies, voire les yeux secs (par accolement en réalité des substituts lacrymaux plus ou moins visqueux et ayant séché). Dans ce dernier cas, il peut parfois n’être observé qu’une mousse, collante, au bord des paupières, témoin d’une sécrétion séreuse chronique.
Mais les sécrétions abondantes et les cils collés évoquent en première intention une infection, surtout lorsqu’ils apparaissent brutalement. On distingue volontiers les sécrétions séreuses, claires, observées pendant les infections virales ou chlamydiennes, des sécrétions purulentes ou mucopurulentes, typiquement bactériennes. Là encore, la distinction n’est que théorique.
Des sécrétions peu abondantes, mousseuses et matinales évoquent une sécheresse oculaire. Un accolement chronique des cils associé à des squames accrochés aux cils évoque une blépharite.
Il s’agit de deux signes évoquant fortement une composante allergique, notamment dans les atteintes récurrentes ou chroniques. Ils peuvent aussi être rencontrés dans certaines infections (leur apparition est alors brutale et associée à d’autres signes évocateurs).
Ils sont aussi spontanément décrits par une quantité significative de patients atteints de sécheresse oculaire apparemment isolée. Même dans ce contexte, ils doivent orienter le clinicien vers la recherche d’une composante allergique, dont le traitement peut permettre de mieux maîtriser la maladie de fond.
Il s’agit d’une dimension évoquée souvent d’emblée par le patient, et dont le médecin doit tenir compte, quitte à poser des questions concrètes à ce propos. Plusieurs études ont montré l’impact majeur des pathologies chroniques de la surface oculaire, en premier lieu la sécheresse oculaire, qui peut générer de graves troubles dépressifs [8]. Le retentissement de la sécheresse oculaire sur la qualité de vie a été montré comme équivalent à celui généré par une angine de poitrine modérée à sévère, voire une hémodialyse chronique [9]. Il peut par ailleurs y avoir des incompréhensions majeures entre le patient et son médecin, car il existe une discordance parfois surprenante dans cette maladie entre les signes fonctionnels et les signes physiques [10], ce qui peut laisser croire parfois que le patient se plaint plus que son atteinte ne semble le légitimer. La réponse aux traitements est elle-même assez discordante parfois, en témoigne l’absence de critères de référence définitifs pour suivre l’évolution d’une sécheresse oculaire. Connaître cet aspect complexe des atteintes de la surface oculaire permet de mieux orienter la prise en charge thérapeutique, en modulant la fréquence des visites en fonction de la gravité perçue par le patient.
Les questionnaires ont d’abord été développés à des fins de recherche clinique, mais ils sont désormais souvent utilisés en pratique quotidienne (au moins pour les plus simples d’entre eux) car ils permettent d’avoir une idée rapide sur la variété et la gravité ressentie des symptômes.
L’OSDI (ocular surface disease index) est devenu le questionnaire le plus utilisé dans la sécheresse oculaire en raison de son aspect pratique, au prix cependant d’une certaine simplification de l’analyse qu’on peut en faire [9] (voir fig. 3-9). Ce test explore la qualité de vie et de vue sur 12 items répartis en trois parties : symptômes visuels (cinq questions), limitation des activités liées à la vision (quatre questions) et difficulté d’adaptation à des situations environnementales (trois questions). Pour chaque question, le patient doit répondre sur la fréquence de la gêne ressentie, de « jamais » à « tout le temps ». Après calcul, on obtient un score compris entre 0 et 100. De façon consensuelle, on considère que le syndrome de sécheresse est patent quand le score est de 18 ou plus, et qu’il s’agit d’une atteinte sévère au-delà de 33 à 35 [1]. Une variation de 5 à 7 points d’OSDI est cliniquement significative pour les sécheresses oculaires minimes à modérées, tandis que cette valeur se situe entre 7 et 13 points chez les patients souffrant d’une sécheresse oculaire sévère [11].
D’autres questionnaires sont aussi largement utilisés en recherche clinique, car ils apportent d’autres informations utiles à la compréhension de l’efficacité d’une nouvelle thérapeutique potentielle. Pour exemple, on peut citer :
le questionnaire de McMonnies qui comporte 15 questions permettant d’obtenir une sensibilité de 87 à 98 % pour le diagnostic de sécheresse oculaire et une spécificité entre 87 et 97 % [12] ;
le score de Schein qui comporte six questions permettant d’étudier la prévalence de la sécheresse oculaire [13] ;
le dry eye questionnaire (DEQ) proposant 21 items sur la prévalence, la fréquence, la sévérité et le degré de la gêne occasionnée par les symptômes [5] ;
l’impact of dry eye on everyday life questionnaire (IDEEL) qui comporte 57 questions reparties en trois modules (activités quotidiennes, satisfaction au traitement et gêne liée aux symptômes) permettant de réaliser des études épidémiologiques et cliniques [14] ;
le National Eye Institute visual function questionnaire (NEI-VFQ25) proposant 25 items sur la qualité de vie liée à la santé et à la vue. Son avantage serait une moindre sensibilité à la sévérité d’une maladie oculaire sous-jacente, ce qui permet de faire la part de la gêne occasionnée par une maladie précise.
Tableau 2-1 Quelques exemples de questionnaires pour analyser les symptômes de maladies de la surface oculaire et la qualité de vie.
Les différents types de pathologies de la surface oculaire varient en fonction de l’âge et du sexe des patients, et il convient bien évidemment d’orienter l’enquête étiologique en fonction de ces données. À titre d’exemple, des signes compatibles avec un syndrome de sécheresse oculaire évoqueront en priorité une véritable insuffisance de sécrétion chez une femme d’âge mûr [17], alors qu’une participation allergique devra être cherchée chez un sujet jeune [21]. De même, une conjonctivite chez un adulte évoquera, a priori, une origine virale et bactérienne banale, alors que chez le nouveau-né, une origine chlamydienne ou gonococcique sera recherchée et chez le nourrisson, une imperméabilité des voies lacrymales.
Elle peut être un argument majeur dans certains contextes. Des opacités cornéennes associées à une conjonctivite plus ou moins chronique font volontiers évoquer un trachome chez un patient récemment immigré d’une zone endémique. De même, les patients mélanodermes, et surtout d’origine africaine, développent des formes limbiques, particulièrement inflammatoires, de kératoconjonctivite allergique ou des atteintes de la surface oculaire dans le cadre de sarcoïdose systémique (conjonctivites, épisclérites/sclérites, sécheresse oculaire) [22].
Il peut s’agir d’un argument majeur de l’enquête étiologique. Outre les anomalies génétiques que cela peut éventuellement évoquer (voir plus loin), le plus fréquent est de découvrir un terrain familial d’allergie pour les maladies chroniques de la surface ou, à l’inverse, pour les conjonctivites ou kératoconjonctivites aiguës, une notion d’épidémie évoquant en premier lieu une adénovirose. Dans le cadre des sécheresses oculaires, il n’est pas inutile non plus de demander si des collègues de travail ou les gens vivant sous le même toit partagent le même type d’anomalie, ce qui oriente vers le rôle toxique (et/ou allergisant) d’un polluant (voir plus loin).
L’exposition dans les activités privées ou professionnelles à des facteurs pathogéniques potentiels pour la surface oculaire doit être un des sujets abordés lors de l’interrogatoire, en fonction de la plainte exprimée par le patient.
Le travail à l’écran prolongé, a fortiori lorsque l’écran est situé plus haut que la tête du patient est un facteur déclenchant ou aggravant de sécheresse oculaire. Plusieurs études ont montré que la fréquence de clignement peut réduire d’un facteur 2 dans ce type d’activités, avec une altération du film lacrymal qui peut apparaître en 3 heures [23] et à terme une diminution de la sécrétion lacrymale [23], cette conséquence ultime étant toutefois contestée. Des résultats similaires ont aussi été décrits avec d’autres activités nécessitant une attention visuelle soutenue, comme la conduite automobile [24].
L’exposition aux ventilations climatisées est un autre facteur de risque classique d’aggravation des symptômes liés à la sécheresse oculaire [25] et aux allergies. Une étude a suggéré que 48 % des sujets soumis régulièrement à ce type de ventilations présentent des signes de sécheresse [25]. De même, les températures chaudes peuvent favoriser plusieurs types d’atteintes en fonction du contexte. Les chauffages domestiques, qui diminuent l’hygrométrie de l’air ambiant, peuvent favoriser des symptômes de sécheresse oculaire. À l’inverse, une hygrométrie élevée dans une ambiance chaude favorise le développement des acariens et des moisissures, facteurs d’allergie. Une chaleur naturelle peut aussi favoriser l’apparition de sécheresse oculaire (dans les climats de type saharien) ou d’infections (notamment fongiques) dans les ambiances tropico-équatoriales [26].
L’exposition aux polluants est un autre facteur de risque de décompensation de maladies de la surface oculaire, qu’il s’agisse de polluants physiques ou chimiques [27]. La première catégorie est représentée par les particules industrielles, notamment celles de fibres minérales synthétiques (matériaux d’isolation) [28] ou celles liées à la combustion (diesel) [29]. Parmi les produits chimiques, certains comme les aldéhydes (peintures, bois aggloméré, cires) et les ammoniums quaternaires (désinfectants ménagers, conservateurs alimentaires, produits cosmétiques), dont le chlorure de benzalkonium, sont connus pour leur effet irritant et déstabilisant pour le film lacrymal [30]. Les composés organiques volatiles (matériaux de construction, colles, revêtements, moisissures) ne sont en général pas irritants aux concentrations usuelles, mais peuvent le devenir lorsque l’air ambiant en contient d’avantage [31]. Il en est de même pour le monoxyde de carbone (CO) et la fumée de tabac, que la consommation soit active ou passive. La fumée de tabac contient du CO, de la nicotine, et de très nombreux polluants organiques volatiles, dont l’effet délétère sur la sécheresse oculaire ou l’allergie passe notamment par une augmentation des neurotrophines lacrymales (nerve growth factor ou NGF, brain-derived neurotrophic factor ou BDNF, neurotrophin-3 ou NT-3 et neurotrophin-4 ou NT-4) [32]. On peut aussi citer dans cette catégorie les polluants biologiques, notamment les moisissures (Alternaria, Aspergillus, etc.) déjà évoquées à propos des systèmes de ventilation. Ils ont un effet irritant, déstabilisent le film lacrymal et induisent des réactions allergiques, directement ou par les enzymes ou les composés organiques volatiles émis par ces micro-organismes. De même, les contacts avec des animaux domestiques (notamment chien, chat, cheval, etc.) ou leur entretien (litière, aquarium) sont autant d’éléments à analyser dans certaines maladies de la surface oculaire, en premier lieu les allergies. Enfin, la pratique de certaines activités sportives ou culturelles peut participer à aggraver le dérèglement de la surface oculaire dans certaines situations : chlore des piscines, résine et diluants utilisés dans les activités picturales, etc.
Enfin, le sick building syndrome (SBS) englobe tous les problèmes de santé en rapport avec la pollution atmosphérique à l’intérieur d’un bâtiment. Il est secondaire, généralement, à des défauts dans le chauffage, la ventilation et la climatisation qui induisent une pollution d’origine multifactorielle : chimique et biologique. Sur le plan ophtalmologique, il se traduit par une irritation oculaire en rapport avec une sécheresse ou une allergie oculaire [33].
Il s’agit probablement d’un des premiers éléments à éclaircir lors de la prise en charge d’une maladie de la surface oculaire. À titre d’illustration, dans une étude multicentrique rétrospective sur 9 600 patients, plus de 40 % de ceux traités pour un glaucome ou une hypertonie présentaient des symptômes de sécheresse oculaire et plus de 20 % présentaient des signes cliniques objectifs, à type de kératite, blépharite et hyperhémie conjonctivale [34]. D’autres études ont aussi retrouvé des signes d’œil sec chez la moitié des patients traités par collyres antiglaucomateux, ces atteintes étant sévères dans 27 % des cas [35], pouvant même aboutir à des lésions de fibrose conjonctivale [36]. Les antiglaucomateux ne sont pas les seuls en cause : les antiviraux topiques (en particulier de première génération) [37], les antibiotiques (en particulier les quinolones et les aminosides) ainsi que les collyres antimycotiques ont aussi un fort potentiel épithéliotoxique [38]. Les anesthésiants topiques sont l’exemple extrême, puisque des instillations répétées (en automédication non contrôlée) exposent à la survenue rapide d’une kératite neurotrophique [39]. Enfin, le rôle des conservateurs, en particulier le chlorure de benzalkonium (BAK) n’est plus à démontrer dans le déclenchement d’anomalies transitoires puis pérennes de la surface oculaire [40].
Lors de l’interrogatoire, tous les traitements doivent donc être notés, en cours comme anciens (en précisant la date de la dernière prise), sans oublier les mesures effectuées en automédication. On profite de ce temps pour évaluer la tolérance à certains principes actifs (les effets potentiellement toxiques de certains principes actifs ou excipients, dont les conservateurs, sont largement traités dans le chapitre 12-I), les allergies éventuelles, la qualité de la compliance.
La recherche d’antécédents infectieux est un élément important de l’anamnèse, car ils peuvent faire le lit de plusieurs autres types d’atteintes de la surface oculaire, en particulier un syndrome sec [41]. Les antécédents anciens ou récents de conjonctivite ou de kératite devront être recherchés, en précisant :
si les deux yeux ou non ont été atteints ;
les facteurs déclenchants éventuels de ces infections ;
leur caractère unique ou récidivant ;
l’origine microbienne exacte, prouvée ou suspectée ;
les traitements mis en place et leur efficacité.
Ainsi, à tire d’exemple, une kératoconjonctivite acquise dans un contexte épidémique et/ou associée à une atteinte des voies aériennes supérieures évoque une origine adénovirale, dont on sait qu’elle peut induire des opacités sous-épithéliales chroniques, une fibrose conjonctivale dans les culs-de-sac et une sécheresse oculaire résiduelle [42]. De même, une kératite unilatérale et récidivante évoque en premier lieu une origine herpétique, et ces épisodes peuvent expliquer la présence d’opacités cornéennes, et même une sécheresse oculaire dans l’œil atteint comme dans l’œil apparemment épargné [43]. Citons encore le trachome, dont les complications potentielles et à long terme pour la surface oculaire sont multiples (malpositions palpébrales, trichiasis, symblépharons, néovascularisation, opacités cornéennes, fibrose conjonctivale, dysfonction meibomienne, sécheresse oculaire sévère) [41]. Enfin, la survenue d’une infection cornéenne chez un porteur de lentilles de contact doit faire craindre en premier lieu une infection bactérienne, mais une infection amibienne ou fongique doit aussi être évoquée. Mais toutes peuvent induire des opacités sévères, des troubles de la ré-épithélialisation et, à nouveau, une sécheresse oculaire.
Ces différents exemples illustrent la diversité des complications à long terme des infections de la surface oculaire, qu’il faut donc systématiquement rechercher à l’interrogatoire devant toute anomalie de la surface oculaire.
Par argument de fréquence, la sécheresse oculaire doit être recherchée en priorité. Des questions simples permettent d’en retrouver les principaux signes fonctionnels, si le patient ne les a pas exprimés spontanément dans les premiers temps de l’entretien (voir plus haut). Il convient de rechercher d’autres localisations de sécheresse, notamment buccale et génitale, et de poser les questions sur les pathologies en relation et les traitements systémiques (voir plus loin).
Quoi qu’il en soit, les symptômes de sécheresse oculaire sont à la fois très peu corrélés entre eux et peu corrélés à la gravité de l’atteinte objective de la cornée et de la conjonctive [44]. Les symptômes d’œil sec sont peu spécifiques et peuvent être présents dans toutes les PSO. La sécheresse oculaire constitue un facteur de risque de kératites bactériennes [45], inflammatoires et trophiques [41], de même qu’elle peut favoriser l’allergie [46].
Les signes fonctionnels d’allergie doivent aussi être recherchés à l’interrogatoire, car l’hypersensibilité à un ou plusieurs allergènes peut aggraver les autres pathologies de la surface oculaire et/ou introduire des éléments confondants dans les symptômes.
Enfin, une recherche systématique des autres maladies oculaires fréquentes (glaucome, dégénérescence maculaire liée à l’âge ou DMLA, etc.) permet de croiser les réponses avec les données décrites ci-après.
La survenue d’une pathologie de la surface oculaire dans les suites, même retardées, d’une chirurgie oculaire est un argument majeur de l’enquête étiologique.
Il est désormais reconnu qu’un syndrome de sécheresse oculaire peut devenir symptomatique après une chirurgie oculaire, en particulier les gestes à visée réfractive, les phako-exérèses et les blépharoplasties. L’incidence de la sécheresse oculaire dans les suites d’un Lasik (laser in situ keratomileusis) à charnière nasale ou supérieure est respectivement de 47 % et 53 % [47]. Une hypoesthésie cornéenne est d’ailleurs quasi constante dans les mois suivant un Lasik [48]. Plus de 10 % des patients opérés de blépharoplastie développent une sécheresse oculaire durant plus de 2 semaines en postopératoire [49]. De nombreux auteurs ont objectivé l’apparition ou l’aggravation des signes de sécheresse oculaire après phako-émulsification (diminution du temps de rupture du film lacrymal, du test de Schirmer et de la hauteur du ménisque lacrymal ; métaplasie squameuse conjonctivale) [50].
Ce type d’anomalies peut prendre plusieurs mois, voire années, avant de se résoudre, puisque 20 % des patients opérés par Lasik présentent encore des signes d’œil sec 6 mois après la chirurgie [51]. Dans certains cas, la sécheresse oculaire peut même être définitive. Il est alors probable que la chirurgie n’a fait que décompenser une pathologique jusqu’alors latente, mais prête à se manifester à la moindre perturbation supplémentaire.
La sécheresse oculaire n’est pas la seule anomalie qui peut apparaître après chirurgie ou même un geste ophtalmologique à visée diagnostique. Il peut bien évidemment s’agir d’infection, bactérienne surtout, mais aussi virale (notamment adénovirus dans les périodes épidémiques). Les dystrophies de la membrane basale épithéliale (secondaires ou primitives, de type Cogan) peuvent se compliquer de troubles de la ré-épithélialsation après chirurgie de la cataracte ou réfractive [52], comme c’est d’ailleurs aussi le cas chez les patients porteurs d’une kératite neurotrophique, même subclinique [53]. Enfin, les traitements pré-, per- et postopératoires peuvent participer à ces complications iatrogéniques. Une fonte stromale aseptique peut être induite par l’utilisation de collyres aux anti-inflammatoires non stéroïdiens (AINS) [54]. Les cas suivants sont moins sévères mais aussi plus fréquents : les anesthésiques topiques utilisés pour le geste peuvent aussi induire des lésions épithéliales, rapidement résolutives, de même que les corticoïdes peuvent retarder la cicatrisation cornéenne.
Les porteurs des lentilles de contact sont plus exposés que la population générale au développement d’anomalies de la surface oculaire. Inversement, les lentilles de contact peuvent être salutaires dans plusieurs types de maladies de la surface oculaire, mais l’effet bénéfique sur le confort peut rapidement être dépassé par les complications infectieuses, etc.
Outre les complications trophiques et inflammatoires propres au port de lentilles de contact (voir chapitre 10), les porteurs de lentilles développent une sécheresse oculaire dans 50 à 98 % des cas [19]. Ils peuvent aussi développer des infections, notamment bactériennes, amibiennes et fongiques, avec des particularités épidémiologiques et thérapeutiques (voir chapitre 6) [55].
L’interrogatoire sur le port des lentilles doit donc être assez précis, en notant le matériau, l’ancienneté et le temps de port, le respect ou non des mesures d’hygiène et des règles de manipulation, etc.
Tout traumatisme oculaire peut favoriser et décompenser une pathologie de surface oculaire. Les paragraphes précédents sur la chirurgie et les lentilles de contact ne sont finalement que des cas particuliers de traumatisme oculaire. Les brûlures par un agent thermique ou chimique peuvent entraîner, parfois de façon définitive, des opacités cornéennes et/ou des atteintes limbiques, potentiellement responsables d’un syndrome d’ulcération épithéliale récurrente ou d’une néovascularisation cornéenne. Les autres complications classiques sont le symblépharon, le trichiasis, le dystichiasis, l’entropion ou ectropion, la sténose des voies lacrymales. Les traumatismes par des agents végétaux exposent à des infections cornéennes, en particulier fongiques et bactériennes.
L’interrogatoire doit préciser les circonstances de survenue du traumatisme (à renseigner de façon détaillée s’il s’agit d’un accident du travail), la nature du traumatisme, les mesures prises par l’accidenté et son entourage. À ce propos, les instillations de divers produits dans le but de corriger les conséquences de l’accident peuvent elles-mêmes être délétères (instillation d’une base pour « tamponner » un acide, par exemple).
Temps élémentaire de tout examen clinique ophtalmologique, la mesure de l’acuité visuelle doit être couplée à une mesure de la correction portée et/ou de la correction optimale. Les anomalies orthoptiques majeures doivent aussi être notées, car on sait l’incidence d’une mauvaise correction optique et des anomalies orthoptiques sur la qualité de la surface oculaire, et l’éventuelle décompensation d’anomalies sous-jacentes. Un moindre confort (mesuré par le score OSDI) et un plus faible temps de rupture du film lacrymal sont d’ailleurs plus fréquemment notés chez les myopes forts que les emmétropes [56].
Leur nature est très diverse en fonction des PSO. À titre d’exemple, un syndrome grippal et/ou une adénopharyngite sont des prodromes fréquents d’une kératoconjonctivite adénovirale, de même que des douleurs du scalp avant la survenue d’une kératite peuvent faire évoquer un mécanisme de réactivation du virus varicelle–zona, même en l’absence de vésicules cutanées (zoster sine herpete). Un autre exemple typique est celui des atteintes herpétiques dont la nature peut être suspectée aussi sur celle du facteur déclenchant les récidives (chirurgie, exposition aux ultraviolets, etc.). De même, la rechute d’yeux rouges avec larmoiement à chaque séjour au même endroit ou à une époque donnée suggère fortement une allergie. Enfin, l’aggravation de l’inconfort oculaire lors d’une exposition au vent, à la fumée, à l’air conditionné ou au travail sur écran est un élément très en faveur d’un facteur, primitif ou non, isolé ou pas, de sécheresse oculaire.
L’analyse des antécédents généraux est orientée en fonction du type d’anomalies de la surface oculaire présent ou suspecté.
Dans le cadre d’une sécheresse oculaire, il est logique de rechercher des antécédents (ou des signes en faveur) d’un syndrome de Gougerot-Sjögren (SGS) primitif ou secondaire à une autre pathologie auto-immune ou infectieuse (polyarthrite rhumatoïde, hépatite virale C, etc.). Les autres causes d’atteinte inflammatoire des glandes lacrymales (comme la sarcoïdose) ou des paupières (acné rosacée et dermatite séborrhéique) doivent aussi être évoquées, de même que les antécédents de greffe de moelle osseuse [57] ou de pathologie cancéreuse par le biais des traitements. Enfin, quelques maladies sont rarement suffisantes pour déclencher à elles seules une sécheresse oculaire, mais elles peuvent l’aggraver. Il s’agit des causes de neuropathies périphériques (diabète) et les allergies. Leur recherche est d’ailleurs systématique dans les anomalies de la surface oculaire, tant on sait leur grande prévalence dans la population (15 à 20 %) et leur intrication avec les autres pathologies de surface [58].
Dans les maladies inflammatoires de la cornée et de la sclère, l’enquête s’oriente à nouveau sur la polyarthrite rhumatoïde, mais aussi sur les maladies de Wegener, la péri-artérite noueuse, la polychondrite atrophiante, etc. (voir chapitre 7). Des antécédents de varicelle ou de zona sont importants à prendre en compte en cas de sclérite ou d’épisclérite [59]. Pour les atteintes conjonctivales aiguës ou récidivantes, la recherche de toute autre manifestation atopique (asthme, dermatite, rhume des foins, etc.) peut apporter des éléments majeurs pour le bilan étiologique.
Certaines maladies de la surface orientent encore plus précisément l’interrogatoire sur les antécédents systémiques. L’existence de kératite limbique supérieure (kératite de Théodore) est, par exemple, classiquement associée aux dysthyroïdies (plutôt hyperthyroïdie), mais une anasarque peut se manifester aussi par un conjonctivochalasis. De même, une atteinte conjonctivale avec dacryoadénite ou parotidite évoque en premier lieu un syndrome de Mikulicz dans le cadre d’une sarcoïdose et un syndrome oculoglandulaire de Parinaud fait évoquer en priorité une maladie des griffes du chat.
Enfin, l’analyse des antécédents généraux peut aussi inclure, en fonction du terrain, la recherche de maladies génétiques. À titre d’exemples, le syndrome d’Allgrove, maladie autosomique récessive, se manifeste par une alacrymie congénitale avec des signes neurologiques, et la dysautonomie familiale (syndrome de Riley-Day) est associée à un manque important de larmes émotionnelles et réflexes.
Il s’agit de la suite logique de l’interrogatoire sur les antécédents.
Les traitements topiques, en cours ou anciens, ont théoriquement déjà été étudiés dans l’analyse de l’histoire de la maladie oculaire.
Pour les traitements systémiques, il est préférable de récupérer l’ordonnance complète du patient, mais aussi rechercher des prises anciennes de médicaments pouvant induire des anomalies persistantes de la surface oculaire. Il convient de préciser : l’indication, la date de début, la posologie, la tolérance, la compliance, les effets indésirables (même extra-oculaires) déjà observés. Le détail des traitements susceptibles d’induire des anomalies de la surface oculaire est donné dans le chapitre 12-II.
L’examen est réalisé de façon bilatérale et comparative. On l’organise habituellement en quatre temps : inspection en lumière ambiante, mesure des capacités visuelles, examen à la lampe à fente avant puis après instillation de colorants.
Ce premier temps peut être réalisé pendant l’installation du patient dans le cabinet et l’interrogatoire, car la plupart des anomalies recherchées ne nécessitent pas plus qu’une observation du patient.
On recherche en premier les anomalies palpébrales évidentes comme un ectropion, un entropion, et d’autres caractéristiques importantes pour mieux comprendre les anomalies de surface.
L’ectropion (fig. 2-1) peut être classé en fonction de la sévérité :
minime : simple éversion de cils ;
modéré : perte de contact entre le globe oculaire et la paupière ou diastasis oculopalpébral ;
constitué : éversion de la paupière qui, dans les cas évolués, développe un véritable effacement palpébral.
L’ectropion peut aussi être classé en fonction de la topographie :
total : sur toute la longueur de la paupière ;
segmentaire : latéral, moyen, nasal ;
lacrymal : localisé au point lacrymal et correspondant à une forme clinique particulière de l’ectropion nasal.
Dans tous les cas, l’ectropion peut générer des anomalies de la surface oculaire, notamment une sécheresse, d’abord localisées en croissant de lune inférieur (surexposition par manque de contact), puis touchant une portion de plus en plus grande vers le haut de la surface oculaire [60].
L’entropion (fig. 2-2) peut être permanent ou n’apparaître qu’après un clignement (forme de début des entropions spasmodiques). L’enroulement du bord libre de la paupière vers le globe oculaire provoque un glissement des cils sur la surface cornéenne et crée une irritation de la cornée. Il se manifeste par une sensation de corps étranger, voire une baisse d’acuité visuelle lorsque la cornée est très altérée. On peut retrouver une hyperhémie conjonctivale aux stades initiaux, puis à terme des ulcérations, des opacités et une néovascularistaion cornéenne dans les formes très avancées.
D’autres anomalies palpébrales peuvent être observées à ce stade et rentrent dans l’analyse globale du cas clinique. On peut tout d’abord citer les cicatrices de traumatisme qui déforment le bord palpébral. On peut aussi noter un œdème palpébral, une éruption vésiculeuse (évoquant un zona), des lésions eczématiformes (en faveur d’une dermatite atopique), des lésions tumorales d’allure bénigne ou maligne (carcinomes basocellulaires ou beaucoup plus rarement spinocellulaires), un ou plusieurs chalazions (évoquant un terrain de rosacée), un orgelet. On peut encore évaluer la position des canthi et leur forme (canthus rond et laxité canthale externe par exemple), et l’aspect de la lamelle postérieure tarsoconjonctivale (rétraction tarsale). Enfin, l’existence d’une exophtalmie, avec rétraction de la paupière supérieure et visibilité anormale de la sclère en regard du limbe inférieur, évoque une ophtalmopathie basedowienne qui se complique volontiers d’une kératite d’exposition et d’une inflammation globale de la surface oculaire. La présence, généralement chez les enfants, de petites papilles cutanées palpébrales ombiliquées de quelques millimètres évoque un molluscum contagiosum.
On examine le bord libre palpébral à la recherche de signes de blépharite :
antérieure qui intéresse la partie cutanée du bord libre (présence d’une collerette ou de squames autour des cils) ;
postérieure, appelée aussi meibomite, qui intéresse la partie muqueuse du bord (présence des télangiectasies, modification des orifices des glandes meibomiennes).
La qualité et la fréquence du clignement permettent au film lacrymal de bien couvrir la surface oculaire et sont essentielles à la bonne santé de cette dernière. La fréquence normale est de l’ordre de 17 fois par minute [61]. L’augmentation de cette fréquence est évidente dans toutes les lésions aiguës (kératites infectieuses, traumatiques, etc.), mais elle peut aussi évoquer une altération chronique de la surface oculaire. Elle est d’ailleurs assez bien corrélée au temps de rupture du film lacrymal dans les sécheresses oculaires par hyposécrétion comme c’est le cas du syndrome de Gougerot-Sjögren [62]. Elle peut à l’inverse être réduite dans les kératites neurotrophiques [6], ce qui ne fait qu’aggraver la situation.
Le blépharospasme est une forme particulière d’anomalie de fréquence des clignements. Il correspond à la fermeture des paupières de façon répétitive et incontrôlée. Les causes les plus classiques, mais aussi les plus rares, sont le syndrome de Meige (apparition d’une dystonie faciale, autour de la soixantaine, avec spasmes du muscle orbiculaire et atteinte des muscles mandibulaires et cervicaux), le syndrome de Gilles de la Tourette, la maladie de Wilson, les dystonies liées aux antiparkinsoniens et les névralgies du trijumeau [63]. Il est en réalité souvent essentiel et souvent associé à un syndrome de sécheresse oculaire rebelle aux traitements habituels. Dans ce cadre, il n’est pas permanent et peut n’apparaître qu’au bout de plusieurs minutes d’examen (profiter de l’interrogatoire à cet effet) [64]. Un pseudo-blépharospasme est aussi un élément classique dans le cadre des kératites aiguës. Il correspond à un réflexe normal devant une situation pathologique, mais il n’y a pas à proprement parler de dérèglement neuromusculaire comme dans le blépharospasme essentiel.
Les outils modernes d’analyse de la surface oculaire ont permis de confirmer une notion déjà connue des cliniciens de longue date, mais difficilement mesurable : celle de la qualité de l’occlusion palpébrale. Outre les situations évidentes de malocclusion nocturne dans les suites d’une paralysie faciale (signe de Charles Bell) ou d’une plaie palpébrale, ou encore d’une chirurgie délabrante sur une maladie cancéreuse de la face, il existe chez certains patients des clignements plus ou moins abortifs qui peuvent générer ou aggraver des anomalies de la surface oculaire et/ou une intolérance aux lentilles. Cette malocclusion partielle peut toucher tous les clignements ou seulement une partie. Les anomalies cornéoconjonctivales qui en résultent (kératoconjonctivite sèche inférieure) sont d’autant plus marquées que la malocclusion est fréquente et importante. Dans les cas les plus sévères, elle peut être examinée directement en observant le patient pendant la période d’interrogatoire. La confirmation est apportée après instillation de fluorescéine (le film n’est pas entièrement renouvelé à chaque clignement), voire après enregistrement vidéographique [65].
Enfin, il peut être utile dans certains syndromes secs mal expliqués de rechercher un syndrome de laxité palpébrale ou floppy eyelid syndrome, c’est-à-dire une éversion trop facile, voire spontanée lors de l’occlusion oculaire, de la paupière supérieure. Cette éversion est en réalité maximale en période nocturne, ce qui explique le caractère rebelle des yeux secs qui en résultent.
Une observation, même rapide, de la peau du visage permet de détecter des pathologies dermatologiques pouvant générer ou s’associer à des anomalies de la surface oculaire. Des pommettes très rouges, a fortiori si elle s’aggrave en cas d’exposition à la chaleur, de prise d’aliments pimentés ou d’alcool, évoquent une rosacée. Le diagnostic peut être confirmé si on y trouve des télangiectasies et, plus encore, si on détecte un rhinophyma. La dépigmentation de la peau en regard des paupières et/ou la présence de plis supplémentaires en dessous du bord libre de la paupière inférieure (signe de Dennie Morgan) suggèrent un terrain allergique. La présence de croûtes et de squames entre les sourcils est évocatrice de dermatite séborrhéique.
Cette mesure fait aussi partie de l’examen standard de toute pathologie de la surface oculaire, car elle en indique les conséquences et permet d’en évaluer l’évolution.
En pratique courante, la mesure est réalisée, dans les conditions habituelles pour un cabinet d’ophtalmologie, sur une échelle de Monnoyer ou de Snellen. En recherche clinique, des échelles de vision des contrastes peuvent être utilisées pour augmenter la sensibilité des évaluations, et les mesures de la diffusion de la lumière ou des aberrations complètent ces données (voir chapitre 2-III). En revanche, les échelles logarithmiques, type EDTRS (early treatment diabetic retinopathy study), n’ont pas d’intérêt majeur dans les PSO, car elles sont plutôt peu informatives pour faire la différence entre des niveaux élevés d’acuité visuelle, ce qui est généralement le cas des maladies de surface, contrairement aux maladies rétiniennes.
Il est complémentaire de la mesure de l’acuité visuelle et peut être utile dans les situations chroniques ne répondant qu’incomplètement au traitement théoriquement adapté. On sait que les troubles orthoptiques, au même titre qu’un trouble réfractif non corrigé, peuvent décompenser une anomalie de la surface oculaire, notamment lors des efforts visuels prolongés (travail sur écran, conduite automobile). La fatigabilité oculaire et les autres signes fonctionnels voire physiques de la surface oculaire peuvent ressembler en tout point à une pathologie environnementale ou à une sécheresse oculaire.
Le principe général est de commencer par les observations les moins invasives et les moins pénibles pour le patient, afin que chaque étape de l’examen ne perturbe qu’au minimum les étapes suivantes. Ainsi, on commence généralement par analyser toutes les structures sans colorants puis avec (les informations fournies par l’instillation de colorants sont décrites plus loin dans le paragraphe « Explorations microbiologiques de la surface oculaire »).
La sclère est une tunique avasculaire comme la cornée et qui, comme elle, peut être infiltrée par des éléments figurés du sang dans le cadre de certains syndromes inflammatoires. Outre la douleur, toujours intense dans les atteintes de la sclère, le principal signe évoquant un processus pathologique scléral est la rougeur, qui correspond en réalité à une dilatation du plexus vasculaire profond de l’épisclère. Selon la localisation de la rougeur d’origine inflammatoire par rapport à la ligne d’insertion des muscles droits, on parle de sclérite antérieure ou postérieure. Elle se traduit par une rougeur profonde, avec des gros vaisseaux violacés répartis de façon perpendiculaire au limbe, qui persiste une minute après instillation d’un collyre vasoconstricteur (néosynéphrine à 10 %, test à ne pas pratiquer chez l’enfant), à la différence de la rougeur d’origine épisclérale (blanchiment très rapide). La rougeur peut être segmentaire ou diffuse associée ou non à un gonflement localisé (sclérite nodulaire) et, souvent, à des douleurs oculaires. Certaines formes de sclérite évoluent vers la nécrose, avec amincissement scléral, laissant apercevoir par transparence le pigment des tissus uvéaux.
Une atrophie de la sclère peut aussi apparaître progressivement en l’absence d’inflammation aiguë, dans le cadre d’une scléromalacie, typique de la polyarthrite rhumatoïde. Une pigmentation mélanique diffuse se traduit par la présence de plaques brunes plates, correspondant histologiquement à des mélanocytes ; elle peut être isolée ou associée à des lésions cutanées pigmentées dans le cadre de nævus d’Ota ou melanosis oculi. En revanche, une pigmentation mélanique localisée et/ou la présence d’un gros tronc vasculaire apparemment isolé doivent faire rechercher des anomalies tumorales sous-jacentes, en particulier un mélanome uvéal. La présence de lésions pigmentées sclérales, associées à des macules pigmentées du cartilage de l’oreille et parfois à des arthropathies, évoque l’alcaptonurie, une maladie génétique rare.
L’épisclère est une couche du tissu conjonctif tapissant le sclère, sous la conjonctive. Pour elle aussi, les douleurs (moins importantes que celles liées aux sclérites) et la rougeur sont les deux principaux signes d’appel. La rougeur peut être segmentaire ou diffuse. Elle se distingue de celle des sclérites par l’organisation concentrique au limbe des vaisseaux trop bien visibles et sa disparition très rapide après l’instillation d’un collyre vasoconstricteur.
L’aspect normal d’une conjonctive est uniformément lisse et transparent, laissant un vernissé : rose en regard de la face interne des paupières et du canthus interne ; blanc en regard de la sclère.
L’hyperémie conjonctivale est l’anomalie conjonctivale la plus commune. Elle traduit une situation inflammatoire, aiguë ou chronique. On note son intensité et sa répartition, qui peuvent être enregistrées en s’appuyant sur l’échelle de McMonnies, en quatre quadrants, souvent utilisée d’ailleurs dans les protocoles de recherche clinique.
Un chémosis, associé ou non à des sécrétions mucopurulentes, évoque plutôt une conjonctivite infectieuse aiguë, mais il peut aussi survenir en contexte allergique.
Les papilles conjonctivales correspondent à des bourgeons charnus irréguliers, polyédriques, centrés par un bouquet vasculaire (« blanc centré par du rouge »). Elles peuvent être groupées, donnant un aspect velouté quand elles sont petites et en pavé lorsqu’elles sont plus grandes. Les papilles conjonctivales sont d’ailleurs classées en fonction de leurs tailles : petites (< 0,3 mm de diamètre), intermédiaires (0,3 à 1 mm) et géantes (> 1 mm). Les conjonctivites papillaires sont très évocatrices d’allergie, mais d’autres phénomènes peuvent les générer, comme des aspects mécaniques couplés à l’hypersensibilité dans les conjonctivites gigantopapillaires des porteurs de lentilles [66].
Les follicules conjonctivaux correspondent à une hyperplasie des éléments lymphoïdes de la conjonctive. Ils se reconnaissent sous la forme de nodules translucides, opalescents, saillants, avasculaires (« blanc entouré de rouge »). Une conjonctivite folliculaire diffuse évoque volontiers une conjonctivite virale, tandis qu’une conjonctivite folliculaire inférieure évoque plutôt une toxicité des collyres. La présence de nodules conjonctivaux périlimbiques, aussi appelés nodules de Trantas, évoque une conjonctivite allergique avancée, dans ses formes vernales ou atopiques.
Des phlyctènes, petites bulles de l’épithélium conjonctival, plus visibles en lumière rasante (mais parfois difficiles à dépister), sont très évocatrices d’une rosacée, notamment en contexte pédiatrique [67]. Mais ces anomalies peuvent aussi se voir dans d’autres contextes : conjonctivite phlycténulaire staphyloccoccique ou tuberculosique [68], allergie oculaire, ptérygion inflammatoire, abcès de cornée et pemphigoïdes des muqueuses [68]. Elles ne doivent être confondues ni avec des follicules, ni avec des dilatations lymphatiques localisées, ni encore avec les nodules conjonctivaux, souvent retrouvés dans la conjonctive bulbaire inférieure et particulièrement évocateurs d’une sarcoïdose (ils sont d’ailleurs facilement accessibles à la biopsie).
Les plis conjonctivaux, parallèles au bord palpébral inférieur, peuvent être observés dans le cas de sécheresse oculaire. Ce conjonctivochalasis inférieur peut être côté en quatre grades (tableau 2-2), dont la gravité est corrélée au risque de sécheresse oculaire [9].
Une fibrose conjonctivale modérée est fréquente en cas de réaction du greffon contre l’hôte (GVH). Elle est plus rare, mais possible, dans les formes avancées d’œil sec par syndrome de Gougerot-Sjögren, dans l’acné rosacée ou encore dans le trachome. En l’absence de ces contextes, il faut savoir évoquer une maladie auto-immune fibrosante, de type pemphigoïde des muqueuses. La recherche d’autres anomalies des muqueuses, notamment dans la bouche, peut apporter des arguments majeurs dans l’enquête étiologique. Des adhérences en pont dans les culs-de-sac (symblépharons) peuvent aussi être notées dans ce contexte, comme dans les suites d’une brûlure caustique.
Tableau 2-2 Notation des plis conjonctivaux parallèles au bord palpébral, d’après Schiffman et al. [9].
L’examen biomicroscopique doit combiner différentes méthodes d’éclairage (diffus ou focal, direct ou incliné voire rasant, à petit puis à fort grossissement) pour observer les anomalies potentielles en fonction de leur nature, de leur étendue et profondeur. Les processus pathologiques peuvent être classés en pertes de la transparence, pertes de substance, anomalies de la vascularisation, déformations et dépôts (dont les corps étrangers).
Les opacités cornéennes peuvent aussi être décrites selon leur caractère diffus ou localisé et selon la profondeur. Les causes les plus fréquentes sont infectieuses et/ou immunologiques, ou encore traumatiques. Les déficits localisés de la fonction endothéliale (traumatique en période postopératoire ou infectieuse) peuvent aussi induire des pertes de transparence locale. Cependant, les atteintes endothéliales sont le plus souvent diffuses (dystrophie endothéliale de Fuchs, par exemple, et la plupart des dystrophies cornéennes et épithéliales génétiquement liées) et induisent donc une perte globale de la transparence cornéenne. Ce peut être aussi le cas des processus immunitaires et infectieux, dans les formes sévères.
Les pertes de substance peuvent toucher tout ou partie de la cornée. La forme la plus commune est l’atteinte épithéliale, qui peut être diffuse ou localisée. Les ulcérations épithéliales localisées prennent différentes formes en fonction du contexte : dendritiques dans les causes virales (herpès, zona) ; pseudo-dendritiques dans les atteintes neurotrophiques ou toxiques (penser aussi aux atteintes amibiennes) ; géographiques dans les atteintes virales ou bactériennes sévères ; marginales dans les atteintes liées à la rosacée (penser aussi à l’herpès). Les atteintes épithéliales diffuses sont en général de type ponctué (kératite ponctuée superficielle ou KPS). Il s’agit probablement de l’atteinte cornéenne la plus fréquente, mais aussi la moins spécifique puisqu’elle peut être liée à des causes aussi diverses qu’une sécheresse oculaire, une atteinte virale (type adénovirus), une toxicité par un collyre. Il existe aussi des pertes épithéliales totales, diffuses sur l’ensemble de la cornée, surtout post-traumatiques (brûlures chimiques), mais aussi parfois infectieuses.
La perte de substance peut être plus profonde, c’est-à-dire toucher l’étage épithélial et le stroma. Un descemétocèle et une perforation cornéenne peuvent en être l’expression finale. Souvent ces pertes de substance sévères sont associées à des pertes de transparence aux bords de l’ulcère, ce qui est très évocateur d’un abcès d’origine infectieuse ou immunitaire. Il existe toutefois des causes immunitaires à des ulcères sans abcès associé telles que : les nécroses cornéennes aseptiques centrales rencontrées dans la polyarthrite rhumatoïde ou le syndrome de Gougerot-Sjögren ; les formes marginales comme la maladie de Mooren et les kératites ulcérantes périphériques (voir chapitre 7). Bien entendu, les pertes de substance profondes post-traumatiques ne s’accompagnent pas initialement d’une opacité stromale adjacente, mais celle-ci peut survenir par agent infectieux ou atteinte endothéliale (en cas de perforation associée).
Les ulcères trophiques (ou neurotrophiques) constituent une forme particulière de perte de substance cornéenne suite à une perte de la sensibilité cornéenne par kératite infectieuse (zostériennes ou herpétiques), traumatique (brûlure, chirurgie oculaire ou trigéminale), et plus rarement par compression nerveuse tumorale, ou dans le cadre de certaines dystrophies stromales [69]. On distingue classiquement trois stades (tableau 2-3) [62, 69] qui règlent la prise en charge thérapeutique.
Les anomalies de la vascularisation cornéenne sont essentiellement le fait de processus de néovascularisation, puisque la cornée est un tissu avasculaire à l’état sain.
Les insuffisances limbiques (post-traumatiques, ischémiques, congénitales, etc.) impactent rapidement la transparence cornéenne et la qualité du revêtement épithélial et sont suivies d’un envahissement conjonctival de la surface cornéenne (conjonctivalisation) accompagné d’une néovascularisation. La plupart des autres causes de néovascularisation sont dues à des processus immunitaires, éventuellement post-infectieux. L’examen biomicroscopique précise l’étendue des néovaisseaux, à la fois sur la surface de la cornée et en nombre de secteurs horaires au limbe (notamment la position par rapport aux zones de contact avec le bord libre des paupières). La profondeur est aussi importante à préciser de même que la sévérité (grosseur des néovaisseaux, qualité du flux sanguin au travers). La valeur sémiologique dépend largement du contexte. Chez un porteur de lentilles de contact, un certain degré de néovascuralisation circonférentielle peut être observé dans 20 % des cas [70], témoin d’une hypoxie cornéenne chronique. Chez les patients sujets aux récidives d’herpès cornéen, les néovaisseaux témoignent de périodes inflammatoires subintrantes, liées à un blocage insuffisant de la réplication virale. Chez un patient atteint de rosacée, elles sont typiquement localisées en regard du bord libre palpébral et sont le reflet de l’activité de la maladie.
Les déformations de la cornée les plus fréquentes sont le kératocône et la dégénérescence marginale pellucide, si l’on exclut évidemment les astigmatismes réguliers primitifs ou postopératoires. Ces deux pathologiques deviennent cliniquement visibles à la lampe à fente lorsqu’elles sont avancées (voir chapitre 8). Citons également le kératoglobe, plus rare.
Les dépôts intracornéens peuvent toucher toutes les couches de la cornée et prendre divers aspects selon la couleur (bruns, noirs, blancs, gris, bleus) et la répartition (diffus ou focaux, en tourbillon, circulaires, etc.). Il peut s’agir de dépôts d’origine médicamenteuse, suite à des traitements topiques ou généraux (amiodarone par exemple, voir chapitre 12-II). Il peut également s’agir de dépôts dans le cadre de maladies métaboliques ou de surcharge systémique (anneau descemétique de Kayser-Fleischer dans la maladie de Wilson, dépôts stromaux de la cystinose, dépôts épithéliaux verticiliés de la maladie de Fabry ou encore dépôts stromaux diffus de la maladie de Hurler, etc.). Certaines maladies hématologiques compliquées d’amylose AL peuvent s’accompagner de dépôts cornéens.
Dans le cadre des dystrophies cornéennes, l’examen sémiologique de la cornée doit aussi passer par l’évaluation de la sensibilité. Cette partie de l’examen est en général réalisée après les autres temps de l’analyse sémiologique (mais avant l’instillation de collyre anesthésique), car elle peut modifier les résultats des tests de coloration et de production des larmes. Elle est donc logiquement décrite à la fin de ce sous-chapitre.
Tableau 2-3 Classification des kératites neurotrophiques [62].
L’analyse qualitative des larmes débute avant toute instillation de colorants, en observant le reflet de la lampe à fente sur le sommet de la cornée. En cas d’altération du film lacrymal, le reflet n’est pas lisse, voire manque totalement. À ce stade de l’examen, on peut aussi observer d’éventuels débris ou filaments, libres ou accrochés à la surface de la cornée.
L’efficacité du film lacrymal peut être appréciée par la mesure dite non invasive du temps de rupture du film lacrymal (non-invasive tear break-up time ou NIBUT) (fig. 2-3). Comme pour la mesure classique du temps de rupture du film lacrymal (BUT ou break-up time, voir ci-dessous), le NIBUT correspond au temps qui s’écoule entre un clignement et le premier signe de distorsion ou de rupture des mires émises par certains appareils ophtalmologiques (kératomètre, topographe cornéen, aberromètre, interféromètre de type Tearscope®). Sa mesure demande donc des instruments plus complexes qu’une simple lampe à fente. Cependant, il présente l’avantage d’être moins variable que le BUT mesuré après instillation de fluorescéine (dont la concentration dans les larmes peut faire varier les mesures), surtout s’il est couplé à des enregistrements vidéographiques qui permettent en outre d’analyser la dynamique des relations entre composants lipidiques et aqueux du film [71]. Chez le sujet sain, on observe une stabilisation complète des mouvements du film en moins d’une seconde après une propagation d’aspect horizontal, tandis qu’en cas de dysfonctionnement meibomien, la stabilisation du film lacrymal est beaucoup plus longue (plusieurs secondes) avec une propagation d’aspect vertical ou inégal et une couche lipidique plus épaisse en cornée inférieure et déficiente en cornée supérieure [72]. Le NIBUT d’un œil sain est supérieur à 16 secondes, et les valeurs sont considérées comme pathologiques en deçà de 7 secondes [73].

Fig. 2-3 Mesure non invasive du temps de rupture du film lacrymal. Interférométrie lacrymale.
(Coll. Pr C. Baudouin.)
L’instillation de colorants permet d’augmenter la sensibilité de l’examen de la surface oculaire. Tous les creux et reliefs sont plus facilement observables, notamment les follicules, papilles, phlyctènes et plis conjonctivaux, ainsi que les anomalies de qualité du film lacrymal (débris, filaments, anomalies dynamiques) et les pertes de substance cornéennes. Pour ces dernières, il convient d’attendre quelques dizaines de secondes après l’instillation pour détecter une éventuelle diffusion du colorant (pour la fluorescéine), témoin d’une altération plus profonde des structures cornéennes.
Les colorants disponibles actuellement en France sont la fluorescéine et le vert de lissamine. La fluorescéine est disponible en collyre à 2 % et sous forme anhydre, imbibée dans des bandelettes de papier stériles (à mouiller avec les propres larmes du patient). La fluorescéine n’est pas un colorant vital car elle se distribue dans les espaces intercellulaires sans pénétrer dans les cellules. Après instillation d’une goutte de fluorescéine dans le cul-de-sac conjonctival, l’application de lumière bleue induit une fluorescence du produit en vert. Le test peut encore être optimisé par l’observation de cette fluorescence au travers d’un filtre jaune (de type Kodak Wratten 12 ou Hoya). L’analyse de la répartition du colorant se fait en deux temps, pour juger à la fois du marquage immédiat des lésions et de la diffusion potentielle autour de ces dernières. L’imprégnation par la fluorescéine témoigne d’une altération des jonctions intercellulaires [74] ou d’une anomalie de la couche muqueuse [75]. Elle colore également les filaments muqueux et les sécrétions. Les avantages majeurs de la fluorescéine sont sa très bonne tolérance (pas de toxicité intrinsèque), sa facilité d’utilisation et l’absence d’interaction avec la qualité du film lacrymal.
Le vert de lissamine est l’autre colorant le plus utilisé pour les maladies de la surface oculaire, en remplacement du rose Bengale, car il donne des résultats similaires [76], tout en étant nettement mieux toléré (moins de douleurs à l’instillation) et moins toxique [77]. Le vert de lissamine est disponible sous forme de collyre à 1 % (à conserver au réfrigérateur) [78] et sous forme anhydre, imbibé dans des bandelettes de papier stériles (à mouiller avec les propres larmes du patient ou du sérum physiologique). Le vert de lissamine colore les cellules mortes et/ou en cours de desquamation [79]. La coloration des lésions épithéliales est assez facilement visible sur la conjonctive, moins évidente sur la cornée. Elle peut être optimisée par l’emploi d’un filtre rouge (de type Hoya 25A ou Kodak Wratten 92), qui fait apparaître les lésions en vert-noir sur fond rouge.
Le rose Bengale n’est plus actuellement disponible en France, mais il reste utilisé dans plusieurs pays européens. Il s’agit d’une teinture fluorée dérivée de la fluorescéine synthétique [80], largement utilisée pour le diagnostic de la sécheresse oculaire [81], avec une bonne corrélation entre le marquage observé et le niveau d’inconfort du patient. L’observation s’effectue en lumière verte ou après interposition d’un filtre vert (type Kodak Wratten 58) : les zones colorées apparaissent alors en noir sur fond vert. Le rose Bengale imprègne la couche de mucus plutôt que les cellules altérées. Cependant, le rose Bengale est progressivement abandonné, du fait des douleurs induites par l’instillation qui nécessitent une préparation par collyre anesthésique ajoutant une toxicité sur des épithéliums le plus souvent déjà altérés.
D’autres colorants ont été utilisés dans diverses études [82] mais ne le sont pas en routine : le bleu alcian (colorant spécifique du mucus, présentant un risque de tatouage indélébile du tissu conjonctif ; le tétrazolium (coloration en rouge des cellules inflammatoires : elle est captée par les cellules vivantes et colore les enzymes spécifiques intracytoplasmiques) ; le bleu trypan (colore les cellules mortes) ; le rouge Soudan (colore les lipides, mais la couche lipidique lacrymale superficielle est trop fine pour être directement visible). De même, des mélanges tinctoriaux ont été proposés, tels que du rose Bengale à 1 % et de la fluorescéine à 1 %, qui permettraient d’apprécier en une seule instillation la qualité des larmes et les lésions cornéoconjonctivales [82].
L’évaluation du temps de rupture du film lacrymal (break-up time ou BUT) (fig. 2-4) est classiquement réalisée après instillation de fluorescéine (voir plus haut pour les conditions techniques). Par définition, le BUT correspond au temps passé entre l’instillation et la première apparition de zones sombres non colorées (dry spot ou taches sèches), que l’on détecte en balayant la totalité de la cornée avec une fente lumineuse de 0,5 à 2 mm de large. On mesure en général 3 fois le BUT et la valeur retenue correspond à la moyenne. D’autres ont proposé de ne tenir compte que des deuxièmes et troisièmes mesures, car la première mesure est significativement différente des suivantes [83]. Cette précaution ne fait en réalité que souligner l’importance d’attendre quelques instants (et quelques clignements) après l’instillation de fluorescéine car une grande quantité de colorant induit une surestimation majeure du BUT [1]. Les valeurs considérées comme normales et pathologiques sont toujours l’objet de discussion. On admet généralement qu’un BUT de plus de 15 secondes est normal. Selon les études, les valeurs de 5 ou 10 secondes sont classiquement considérées comme pathologiques. Il est par ailleurs établi que le BUT diminue avec l’âge [84] selon une équation : BUT = 10,7 – 0,081 × âge chez les patients normaux. Chez des patients asymptomatiques de Hong Kong, il peut être influencé par certains facteurs environnementaux comme l’humidité ou la température de la pièce [85]. Il n’existe pas, pour autant, d’abaques validés du BUT en fonction de l’âge. La mesure du BUT est le plus souvent bien corrélée à la fréquence de clignement [86]. Il peut cependant exister des situations où l’inconfort est tel que les clignements réflexes sont nettement plus rapides que la rupture du film lacrymal. À l’inverse, toutes les situations entraînant une perte importante de la sensibilité cornéenne peuvent induire un clignement moins fréquent que ne le voudrait la qualité du film lacrymal, ce qui ne fait qu’aggraver la situation. Pour tenir compte de ces situations très différentes, il a été préconisé par certains auteurs de prendre en compte l’intervalle entre deux clignements de paupière (ICP) pour calculer l’index de protection oculaire, défini comme le rapport BUT/ICP, dont une valeur inférieure à 1 témoignerait d’une instabilité cliniquement significative [87].
L’évaluation de la qualité du clignement peut être réalisée de façon parallèle à la mesure du BUT. Il suffit de vérifier que chaque clignement est bien complet, c’est-à-dire que l’ensemble du film lacrymal est bien renouvelé. Dans le cas contraire, on observe facilement la limite inférieure du clignement (différence d’intensité de fluorescence entre le film récemment renouvelé, en haut, et celui non renouvelé, en bas). Il convient cependant d’être patient pour obtenir ce type d’informations, car il est rare que tous les clignements soient abortifs, et c’est le pourcentage de film non renouvelé et la fréquence des clignements incomplets qui donnent une idée du rôle potentiel de cette anomalie dans la genèse de la pathologie de surface.
La hauteur du ménisque lacrymal (fig. 2-5) est aussi facilement observable après instillation de colorants, et cette évaluation est souvent réalisée dans la foulée de la mesure du BUT. L’analyse qualitative permet de détecter une réelle insuffisance lacrymale (rivière lacrymale de très faible volume) ou, à l’inverse, une quantité suffisante, voire trop importante, évocatrice d’une sécrétion réflexe en réponse à une agression ou un défaut de drainage dans les voies lacrymales. En pratique quotidienne, on peut utiliser la vis micrométrique de la lampe à fente pour estimer la hauteur du ménisque lacrymal. Les valeurs considérées comme normales sont supérieures à 0,2 mm [88], mais cette mesure est difficile à standardiser. L’observation du profil du ménisque est également utile : un profil de ménisque régulier est caractéristique d’un œil sain, alors qu’un ménisque présentant un bord dentelé est souvent associé à une sécheresse oculaire. Des techniques de mesure plus précises que l’utilisation d’une simple lampe à fente (méniscométrie), basées sur l’utilisation de machines d’imageries de la surface oculaire (photographies, topographies, interférométrie, tomographie par cohérence optique, etc.), sont désormais disponibles. Elles relèvent encore de la recherche clinique, mais même ces techniques complexes ne permettent toujours pas de définir des valeurs consensuelles pour dépister ou affirmer une insuffisance (voir chapitre 2-II). D’ailleurs, plusieurs paramètres peuvent modifier l’évaluation de ménisque des larmes : le volume des larmes bien entendu, mais aussi la localisation du point lacrymal et la longueur de la paupière [89], la rapidité du drainage lacrymal [74], la qualité et la tonicité de l’ouverture palpébrale [88], la présence d’un blépharochalasis ou de sécrétions anormales à la surface de l’œil [90], et même enfin l’instillation trop volumineuse de fluorescéine en début d’examen [90].
L’évaluation du degré d’altération des épithéliums cornéen et conjonctival est largement optimisée par l’utilisation des colorants. On considère que la fluorescéine est plus efficace pour l’analyse de la surface cornéenne tandis que le vert de lissamine est supérieur pour la surface conjonctivale. Cela est mis en œuvre dans le cadre des protocoles de recherche clinique, mais en routine, la fluorescéine peut suffire si l’on prend soin de respecter un temps d’attente pour que les zones de coloration se démarquent de l’imprégnation globale de la surface. Le filtre bleu cobalt peut être complété d’un filtre jaune qui améliore le contraste de la fluorescéine (fig. 2-6). Pour les pertes de substance importantes, les colorants permettent une analyse sémiologique précise (taille, profondeur, diffusion éventuelle du colorant). Ils permettent aussi de détecter les anomalies de surface plus discrètes, comme les débris et petits filaments, mais aussi les épithéliopathies ponctuées, cornéennes et conjonctivales. Dans le cadre de la sécheresse oculaire, les images observées servent à grader la sévérité de l’atteinte. Il existe plusieurs échelles dans la littérature, la première d’entre elles étant historiquement celle de Van Bijsterveld, décrite avec le rose Bengale [91]. Elle a été ensuite largement reprise et améliorée grâce au développement d’autres échelles décrites ci-dessous.
Plusieurs échelles de coloration de l’épithélium cornéoconjonctival ont été développées, en comparant les données du patient à des images de référence. Ces images de référence peuvent être des dessins en noir et blanc avec une description textuelle comme le score de Van Bijsterveld [91], le schéma d’Oxford [79] ou encore l’échelle du National Eye Institute (NEI). Il peut aussi s’agir d’images en couleur, comme c’est le cas pour le score d’Efron [92]. Elles peuvent être aussi une combinaison d’un texte descriptif et d’une image, comme pour le score CCLR (cornea and contact lens research unit ou CCLR scale) [93]. Certains auteurs ont utilisé des échelles descriptives de la superficie et de la densité de coloration cornéenne sans image de référence [94]. D’autres systèmes combinent le score d’Oxford et celui du NEI : c’est le cas de l’ocular staining score (OSS). Ce score composite a été développé pour évaluer la gravité de la kératoconjonctivite sèche dans le syndrome de Gougerot-Sjögren [95].
Il est dorénavant fréquent d’utiliser des échelles composites, empruntant à l’une l’aspect cornéen analysé en fluorescéine et à l’autre l’aspect conjonctival analysé en vert de lissamine (fig. 2-7). Force est de reconnaître que malgré l’importance de la littérature sur le sujet, il n’y a toujours pas de consensus sur la meilleure échelle, et l’une ou l’autre doit être utilisée en fonction des objectifs de chaque étude clinique. Pour la pratique quotidienne, l’échelle d’Oxford ou l’OSS (combinant marquage conjonctival par le vert de lissamine et cornéen par la fluorescéine) sont très largement suffisants pour un suivi précis des patients.
Le tableau 2-4 reprend les principales caractéristiques de ces échelles.

Fig. 2-4 Évaluation du temps de rupture du film lacrymal.

Fig. 2-5 Hauteur du ménisque lacrymal.

Fig. 2-6 Filtre bleu cobalt complété d’un filtre jaune améliorant le contraste de la fluorescéine.
(Coll. Pr C. Baudouin.)

Fig. 2-7 Analyse au vert de lissamine.
Tableau 2-4 Caractéristiques des échelles.
En pratique, on commence généralement par inspecter les paupières et les cils à la lampe à fente et le reste des annexes (qualité de la peau autour des paupières, sourcils, système lacrymal) est examiné en fonction de la pathologie présentée.
Il fait logiquement suite à l’analyse du film lacrymal, surtout après l’instillation du film lacrymal. On détecte alors facilement s’il existe une sténose ou à l’inverse une béance avec ou sans stricturotomie (le plus souvent sur des sondes lacrymales trop serrées) et enfin un ectropion du point lacrymal inférieur. Un point lacrymal normal est ouvert et vide du fait de l’activité de la pompe lacrymale. Un point lacrymal inférieur engorgé, surtout si le liquide qu’il contient présente des débris, évoque une stase en aval, dans le sac lacrymal.
Les glandes de Meibomius sont localisées dans le tarse palpébral, perpendiculairement au bord de la paupière auquel elles s’abouchent dans sa partie muqueuse ou à la jonction cutanéomuqueuse. Elles sont au nombre de 15 à 25 environ par paupière [45]. L’évaluation des sécrétions meibomiennes revêt une grande importance dans l’analyse sémiologique des anomalies chroniques de la surface oculaire. L’aspect des sécrétions meibomiennes (communément appelées « meibum ») est huileux, mais fluide et clair à l’état normal. Le meibum doit donc sourdre facilement lors de la pression des glandes au travers de la paupière. En cas de dysfonctionnement meibomien, le meibum sort difficilement, prend un aspect visqueux, jaunâtre, voire blanchâtre (« en pâte de dentifrice »). Les orifices des glandes apparaissent volontiers inflammatoires, entourés de télangiectasies. Dans les formes les plus avancées, les orifices sont bouchés, voire atrophiques (fig. 2-8). Les glandes peuvent être directement analysées par transillumination, pour mettre en évidence une perte partielle ou totale des structures. Cet examen clinique est dorénavant complété par les techniques meibographiques.
Tableau 2-5 Stades des maladies des glandes meibomiennes d’après Tomlinson et al. [96].

Fig. 2-8 Orifices des glandes de Meibomius atrophiées.
L’appareil ciliaire est composé d’une centaine de cils en paupière supérieure et d’une cinquantaine en paupière inférieure. Son analyse peut donner des informations précieuses sur certaines causes d’anomalies de la surface oculaire.
Le trichiasis est une inflexion des cils vers l’œil qui entraîne une irritation cornéenne avec un risque d’ulcère, d’opacité et de néovascularisation cornéenne. Le distichiasis décrit la présence d’une seconde rangée de cils, positionnée en arrière des cils naturels, en contact avec le globe. Il est souvent d’origine congénitale ; rarement, il peut compliquer certaines brûlures chimiques ou physiques.
Les anomalies de croissance des cils (hypotrichose plus souvent qu’hypertrichose), voire leur disparition (madarose) peuvent compliquer certaines dermatoses atopiques. Les anomalies de pigmentation ciliaire ou des sourcils (poliose) sont associées à certaines inflammations oculaires mettant en jeu les mélanocytes (maladie de Vogt-Koyanagi-Harada et uvéite sympathique). Les autres causes de la poliose, en plus de l’origine génétique, sont médicamenteuses et liées aux tumeurs générales malignes ou bénignes, surtout mélanocytaire [97].
Enfin, la propreté des cils et des sourcils est importante à vérifier. On peut retrouver des croûtes, plus ou moins grasses, dans les blépharites antérieures et les dermatoses séborrhéiques. L’examen à la lampe à fente permet aussi d’observer la peau en regard des paupières et entre les sourcils. Des squames sont aussi évocatrices de dermatoses séborrhéiques, tandis qu’une peau rouge, sèche, cartonnée, voire dépigmentée est évocatrice d’une dermatite atopique.
La présence des squames palpébrales, associées souvent à des squames du cuir chevelu, évoque une dermatite séborrhéique qui peut se manifester sur le plan oculaire par une meibomite, une blépharite, une hyperhémie conjonctivale et une sécheresse oculaire [98]. Un eczéma des paupières et de la région péri-orbitaire évoque une dermatite atopique, dans le cadre d’une kératoconjonctivite atopique, dont le pronostic oculaire est plus engagé que celui des autres formes de conjonctivite allergique.
Il peut être utile d’avoir une idée de la qualité du contenu du sac lacrymal dans certaines pathologies de surface, par exemple en cas de conjonctivites à répétition du nourrisson. On recherche une voussure en regard du sac lacrymal ainsi qu’un reflux mucopurulent à la pression du sac lacrymal qui signent l’existence d’une stase anormale. Une déviation du globe ou une voussure dépassant en hauteur le niveau du tendon canthal interne sont en faveur d’une tumeur du sac ou du contenu orbitaire ou d’une pathologie sinusienne. Le sondage des voies lacrymales ne doit être entrepris, en cas de larmoiement ou de suspicion de stase, qu’à la fin de l’examen de l’œil.
Les glandes lacrymales sont peu accessibles à l’examen clinique en conditions normales, mais elles augmentent de volume et deviennent douloureuses à la palpation en cas de dacryoadénite. Une atteinte de la portion la plus postérieure peut se manifester par une exophtalmie avec diplopie, alors qu’une atteinte de la partie antérieure se traduit par une tuméfaction de la partie supéro-externe de la paupière supérieure, directement visible sous la conjonctive après éversion palpébrale donnant une déformation caractéristique de la paupière supérieure en S allongé.
L’examen clinique des autres structures de l’orbite est à la fois riche et difficile mais peut être utile dans le cadre de certaines PSO. Le cadre osseux peut être observé et palpé pour détecter une déformation. L’exophtalmomètre de Hertel permet de mesurer l’exophtalmie éventuelle (normale inférieure à 25 mm de débord entre la ligne tangentielle à l’apex cornéen et la ligne bicanthale).
Le groupe de travail international sur la sécheresse oculaire conseille de tester le niveau de production des larmes à la fin de l’examen clinique, et à distance des autres temps de l’examen, à la fois pour ne pas être influencé (par l’instillation de collyre) et aussi pour ne pas en fausser les résultats (faux positifs avec les colorants après un test de Schirmer, par exemple) [45]. Parmi les tests dynamiques de la production de larmes, le plus représentatif est le test de Schirmer, décrit pour la première fois par Otto Schirmer en 1903 [99] et dont plusieurs variétés ont été développées.
Il s’agit d’un test quantitatif de la sécrétion lacrymale globale, à la fois basale et réflexe [100]. Il utilise une bandelette de papier-filtre Whatman no 41 mesurant 35 mm de long et 5 mm de large, qui doit être placée délicatement (sans toucher la cornée, pour ne pas fausser les résultats) à la jonction du 1/3 externe et des 2/3 internes du cul-de-sac conjonctival inférieur. Selon les auteurs, le test doit être réalisé les yeux ouverts [85, 101] ou fermés [102], ou encore indifféremment entre les deux positions [91]. Des études suggèrent que les valeurs obtenues les yeux fermés sont plus basses [103] et cette solution est d’ailleurs plus confortable pour le patient. Par ailleurs, cela évite d’avoir à définir la position du regard à maintenir, dont on sait qu’elle peut aussi influencer les résultats par le biais de l’évaporation plus ou moins grande selon l’ouverture de la fente palpébrale [104].
Par définition, le test de Schirmer I est pratiqué sans anesthésie locale, et le test doit durer 5 minutes. La valeur de 5 mm à 5 minutes est la valeur pathologique la plus souvent retenue. Le Dry Eye WorkShop (DEWS) [45], en 2007, considère aussi qu’une valeur inférieure ou égale à 5 mm est un bon indice de sécheresse oculaire. D’autres publications ont retenu la valeur de 10 mm, par essence plus sensible mais moins spécifique. Quoi qu’il en soit, le réel intérêt clinique reste discuté par certains auteurs [1, 91], car même le seuil à 5 mm, pourtant apparemment bas, n’a qu’une sensibilité médiocre (de 25 à 83 % selon les auteurs) pour une spécificité somme toute satisfaisante (environ 90 %). Le réel souci posé par le test de Schirmer I tient aux conditions techniques, puisque la bandelette peut être plus ou moins imbibée d’emblée selon le volume de la rivière lacrymale et la qualité de la sensibilité cornéenne, quand il ne s’agit pas tout simplement d’une imbibition par des larmes artificielles, voire des collyres utilisés pour l’examen précédent. Toutes ces données expliquent le manque de reproductibilité de ce test [105], certes moindre dans les sécheresses oculaires par insuffisance aqueuse, de grade modéré à sévère [102]. Une des astuces pour optimiser l’apport clinique de ce test est de le réaliser à distance du reste de l’examen, en ayant pris le soin d’expliquer le principe au patient pour éviter toute réaction de surprise qui fausserait les résultats. Dans ces conditions, le Schirmer reste un test qu’il convient de pratiquer au mois une fois dans la prise en charge d’un patient souffrant de sécheresse oculaire. Afin d’améliorer son intérêt clinique, certains auteurs combinent le test de Schirmer avec d’autres tests : test de rose Bengale et de BUT pour Farris [106] ; test de fil rouge de phénol pour de Monchy [107].

Fig. 2-9 Test de Schirmer I.
Le test de Jones suit la même méthode que le test de Schirmer I, mais est précédé d’une anesthésie topique, censée supprimer la sécrétion lacrymale réflexe pour ne mesurer que la sécrétion lacrymale basale, reflet du flux physiologique. Il s’agit malheureusement d’une vue trop simpliste, car malgré l’instillation de collyre anesthésique, la stimulation des cils et du bord palpébral persiste et induit une sécrétion réflexe [108]. Le test est en outre peu discriminant et souffre d’une mauvaise spécificité [108]. On retrouve d’ailleurs des valeurs inférieures à 3 mm chez 15 % des sujets normaux [101] et seulement 17 % des patients souffrant de syndrome sec [109]. De plus, les anesthésiques topiques peuvent induire une rupture des jonctions serrées de l’épithélium cornéen, faussant alors les éventuels tests ultérieurs avec colorants [110]. Le test de Jones a donc peu d’intérêt en pratique quotidienne.
Ce test combine la méthode du Schirmer I associée à une stimulation nasale, dont le but est d’augmenter la part du résultat liée à la sécrétion réflexe. Dans ce test, qui n’est plus utilisé de nos jours, la muqueuse nasale est stimulée avec un écouvillon, et une valeur de moins de 15 mm après 2 minutes de stimulation est considérée comme un témoin de déficit de sécrétion réflexe. Le caractère invasif, et même pénible, associé aux difficultés de standardisation, explique son abandon.
Le test au fil rouge phénol (phenol red thread ou PRT) a été introduit pour la première fois en 1982 [105] pour pallier les différents inconvénients du test de Schirmer I. Il utilise un fil de coton stérile, imbibé de rouge phénol, dont la couleur varie en fonction du pH. Le fil est placé dans le cul-de-sac conjonctival inférieur, à la manière de la bandelette de papier du test de Schirmer. Sa couleur passe de l’orange pâle quand il est sec au rouge quand il est imbibé de larmes. Dans sa description princeps, la longueur de fil imprégné de larmes doit être lue 15 secondes après la pose. Ses avantages majeurs sont ses caractères peu invasifs et indolores, et la rapidité de réalisation, et donc une meilleure tolérance que le test de Schirmer I [105, 111]. Il serait en outre plus reproductible et plus sensible que le test de Schirmer I [105].
Les premières études réalisées sur des volontaires sains avec le test commercialisé (Zone-Quick®, Menicon) ont retrouvé une valeur moyenne de 17,3 mm (± 6,7). D’autres études chez des patients atteints de sécheresse oculaire ont défini les valeurs pathologiques comme inférieures à 9 mm ou 12 mm [112], cette dernière valeur permettant de combiner une sensibilité de 56 %, une spécificité de 69 % et une bonne concordance avec le test de Schirmer I. Cependant, des études plus poussées ont montré que l’utilisation du test tel qu’il a été conçu ne fait pas mieux (ni moins bien) que le classique test de Schirmer I [107]. Ceci pourrait être dû aux facteurs pouvant influencer les résultats, dont le volume et la profondeur de la rivière lacrymale, les anomalies de la couche lipidique du film lacrymal, ainsi que la température de la pièce [113]. Cependant, ce test peut être combiné à la procédure du test de Schirmer I, il en résulte une meilleure sensibilité discriminante entre les patients atteints de sécheresse par syndrome de Gougerot-Sjögren et des patients témoins [107]. Ce test, pourtant pratique et totalement indolore, n’est malheureusement plus disponible actuellement en France, mais il le reste dans un certain nombre de pays, dont les États-Unis.

Fig. 2-10 Test au fil rouge phénol.
Ils ont été décrits pour évaluer la clairance de la surface oculaire par les larmes. Historiquement, du rose Bengale ou de la fluorescéine était instillé simultanément dans les deux culs-de-sac conjonctivaux inférieurs et le degré de dilution était observé après 5 minutes. La coloration jaune du ménisque indique un renouvellement correct des larmes, alors qu’une coloration rouge (inchangée) indique un renouvellement insuffisant [114]. De façon complémentaire, McCan et al. ont utilisé des bandelettes de papier imprégnées de fluorescéine, mises en place pendant 3 minutes dans le cul-de-sac conjonctival inférieur, et ont mesuré l’intensité de la coloration restante. La sensibilité, dans leurs mains, était de 83 % pour le diagnostic de la sécheresse oculaire, mais au prix d’une spécificité de seulement 40 % [115]. La complexité de standardisation des tests de dilution les rend peu pratique pour une utilisation en routine (tableaux 2-6 et 2-7).
Tableau 2-6 Comparaison des différents tests cliniques pour le diagnostic de sécheresse oculaire modifié d’après DEWS [1].
Tableau 2-7 Sensibilité des combinaisons des tests cliniques modifiée d’après DEWS [1].
En consultation quotidienne, la sensibilité cornéenne peut être facilement testée avec l’embout propre d’un écouvillon, d’une éponge triangulaire en ouate de cellulose ou d’une compresse stérile. Le stimulus doit être présenté par le côté (pour ne pas être vu) et le clignement doit être très rapide après le contact avec la cornée.
L’esthésiomètre de Cochet-Bonnet peut aussi être utilisé en clinique courante car le test est rapide et aisé. Il utilise un fil de Nylon standardisé, dont on règle la longueur avant d’en appuyer l’extrémité sur la cornée, le patient regardant en face de lui. Plus la longueur est grande, plus le fil est souple, et plus la sensibilité doit être préservée pour détecter le contact. La dureté du fil et donc la pression exercée sur la cornée croissent de façon exponentielle au fur et à mesure que le fil est raccourci. L’humidité dans la pièce, l’ancienneté du fil de Nylon lui-même peuvent modifier les réponses [123], de même que le niveau d’anxiété du patient [124]. Il s’agit toutefois d’un très bon outil pour l’ophtalmologiste clinicien, car il permet d’avoir une idée précise du niveau éventuel de perte de sensibilité et même de réaliser une carte de sensibilité en testant plusieurs secteurs de la cornée. Rappelons à cet égard que certaines pathologies comme la sécheresse ou les infections herpétiques et zostériennes induisent des pertes globales de la sensibilité cornéenne, alors que le déficit sensitif est surtout localisé en regard du site d’infection après abcès à germe bactérien.
Dans le cadre de la recherche clinique, des esthésiomètres plus performants peuvent être utilisés, comme l’esthésiomètre de Draeger [124] ou celui de Belmonte, ce dernier permettant en plus de faire la différence entre des stimuli mécaniques, chimiques et thermiques [125]. Ces appareils sont encore largement réservés à des applications de recherche.

Fig. 2-11 Test de sensibilité cornéenne.
L’examen clinique de la surface oculaire apparaît finalement comme un temps facilement standardisable en pratique quotidienne, ce qui permet d’être plus efficace, à la fois pour le temps consacré et la quantité d’informations recueillies. Cependant, tout n’est pas idéal et une pathologie aussi fréquente que la sécheresse oculaire est justement caractérisée par une certaine discordance entre l’intensité des signes fonctionnels et celle des signes physiques. C’est une raison de plus pour être rigoureux dans l’interrogatoire et l’observation des lésions, avant de se lancer dans la demande d’examens complémentaires coûteux, dont l’efficacité sera d’autant meilleure qu’ils sont guidés par une bonne analyse sémiologique en amont.
[1] DEWS. Methodologies to diagnose and monitor dry eye disease : report of the diagnostic methodology subcommittee of the International Dry Eye WorkShop (2007). The Ocular Surface 2007 ; 5 : 108-52.
[2] Cronau H, Kankanala RR, Mauger T. Diagnosis and management of red eye in primary care. American Family Physician 2010 ; 81 : 137-44.
[3] Kaswin G, Rousseau A, M’Garrech M, et al. Optical aberrations in patients with recurrent herpes simplex keratitis and apparently normal vision. The British Journal of Ophthalmology 2013 ; 97 : 1113-7.
[4] Denoyer A, Rabut G, Baudouin C. Tear film aberration dynamics and vision-related quality of life in patients with dry eye disease. Ophthalmology 2012 ; 119 : 1811-8.
[5] Begley CG, Chalmers RL, Abetz L, et al. The relationship between habitual patient-reported symptoms and clinical signs among patients with dry eye of varying severity. Investigative Ophthalmology & Visual Science 2003 ; 11 : 4753-61.
[6] Kaufman SC. Anterior segment complications of herpes zoster ophthalmicus. Ophthalmology 2008 ; 115 : S24-32.
[7] Goto E, Yagi Y, Matsumoto Y, et al. Impaired functional visual acuity of dry eye patients. American Journal of Ophthalmology ; 2002, 133 : 181-6.
[8] Labbé A, Wang YX, Jie Y, et al. Dry eye disease, dry eye symptoms and depression : the Beijing Eye Study. The British Journal of Ophthalmology 2013 ; 97 : 1399-403.
[9] Schiffman RM, Christianson MD, Jacobsen G, et al. Reliability and validity of the Ocular Surface Disease Index. Archives of Ophthalmology 2000 ; 118 : 615-21.
[10] Lemp MA. Clinical trials in dry eye in surgery for dry eye ? Developments in Ophthalmology 2008 ; 41 : 283-97.
[11] Miller KL, Walt JG, Mink DR, et al. Minimal clinically important difference for the ocular surface disease index. Archives of Ophthalmology 2010 ; 128 : 94-101.
[12] Schaumberg DA, Sullivan DA, Buring JE, et al. Prevalence of dry eye syndrome among US women. American Journal of Ophthalmology 2003 ; 136 : 318-26.
[13] Schein OD, Tielsch JM, Munoz B, et al. Relation between signs and symptoms of dry eye in the elderly. A population-based perspective. Ophthalmology 1997 ; 104 : 1395-401.
[14] Rajagopalan K, Abetz L, Mertzanis P, et al. Comparing the discriminative validity of two generic and one disease-specific health-related quality of life measures in a sample of patients with dry eye. Value In Health 2005 ; 2 : 168-74.
[15] Walt JG, Rowe MM, Stern KL. Evaluating the functional impact of dry eye : the ocular surface disease index. Drug Information Journal 1997 ; 31 : 1436.
[16] McMonnies CW. Key questions in a dry eye history. Journal of the American Optometric Association 1986 ; 57 : 512-7.
[17] McMonnies C, Ho A, Wakefield D. Optimum dry eye classification using questionnaire responses. Advances in Experimental Medicine and Biology 1998 ; 438 : 835-8.
[18] Mangione CM, Lee PP, Pitts J, et al. Psychometric properties of the National Eye Institute visual function questionnaire (NEI-VFQ). NEI-VFQ field test investigators. Archives of Ophthalmology 1998 ; 116 : 1496-504.
[19] Begley CG, Caffery B, Nichols KK, et al. Responses of contact lens wearers to a dry eye survey. Optometry and Vision Science 2000 ; 77 : 40-6.
[20] Baudouin C, Creuzot-Garcher C, Hoang-Xuan T, et al. Création d’un questionnaire spécifique d’aide au diagnostic et d’évaluation de la qualité de vie chez les patients souffrant de pathologie de la surface oculaire. Journal Français d’Ophtalmologie 2003 ; 26 : 119-30.
[21] Resnikoff S, Cornand G, Filliard G, et al. Limbal vernal keratoconjunctivitis in the tropics. Rev Int Trach Pathol Ocul Trop Subtrop Sante publique 1988 ; 65 : 21-72.
[22] Eksarenko OV, Kharlap SI, Safonova TN. Sarcoidosis : etiology, pathogenesis, epidemiology, risk factors, clinical presentation. Vestnik Oftalmologii 2012 ; 128 : 42-8.
[23] Abe S, Sotoyama M, Taptagaporn S, Saito S. Relationship between vertical gaze direction and tear volume. 4th International scientific conference WWDU’94 : work with display units. 1994 : B6-B7.
[24] Deschamps N, Ricaud X, Rabut G, et al. The impact of dry eye disease on visual performance while driving. American Journal of Ophthalmology 2013 ; 156 : 184-9.e3.
[25] Sommer HJ, Johnen J, Schongen P, et al. Adaptation of the tear film to work in air-conditioned rooms (office-eye syndrome). German Journal of Ophthalmology 1994 ; 3 : 406-8.
[26] Bourcier T, Sauer A, Letscher-Bru V, et al. Fungal keratitis. Journal Français d’Ophtalmologie 2011 ; 34 : 563-7.
[27] Bourcier T, Viboud C, Cohen JC, et al. Effects of air pollution and climatic conditions on the frequency of ophthalmological emergency examinations. The British Journal of Ophthalmology 2003 ; 87 : 809-11.
[28] Trethowan WN, Burge PS, Rossiter CE, et al. Study of the respiratory health of employees in seven European plants that manufacture ceramic fibres. Occupational and Environmental Medicine 1995 ; 52 : 97-104.
[29] Torricelli AA, Novaes P, Matsuda M, et al. Correlation between signs and symptoms of ocular surface dysfunction and tear osmolarity with ambient levels of air pollution in a large metropolitan area. Cornea 2013 ; 32 : e11-5.
[30] Pisella PJ, Debbasch C, Hamard P, et al. Conjunctival proinflammatory and proapoptotic effects of latanoprost and preserved and unpreserved timolol : an ex vivo and in vitro study. Invest Ophthalmol Vis Sci 2004 ; 45 : 1360-8.
[31] Rios JL, Boechat JL, Gioda A, et al. Symptoms prevalence among office workers of a sealed versus a non-sealed building : associations to indoor air quality. Environment International 2009 ; 35 : 1136-41.
[32] Kimata H. Passive smoking elevates neurotrophin levels in tears. Human & Experimental Toxicology 2004 ; 23 : 215-7.
[33] Godish T. Indoor environmental quality. Lewis Publishers ; 2001.
[34] Jaenen N, Baudouin C, Pouliquen P, et al. Ocular symptoms and signs with preserved and preservative-free glaucoma medications. European Journal of Ophthalmology 2007 ; 17 : 341-9.
[35] Van Went C, Brasnu E, Hamard P, et al. The influence of ocular surface diseases in the management of glaucoma. Journal Français d’Ophtalmologie 2011 ; 34 : 230-7.
[36] Anders N, Wollensak J. Ocular pseudopemphigoid after topical drug administration. Klinische Monatsblatter fur Augenheilkunde 1994 ; 205 : 61-4.
[37] Tabbara Kf, Al Balushi N. Topical ganciclovir in the treatment of acute herpetic keratitis. Clinical Ophthalmology 2010 ; 4 : 905-12.
[38] Chiquet C, Romanet JP. Prescribing fortified eye drops. Journal français d’ophtalmologie 2007 ; 4 : 423-30.
[39] Dart J. Corneal toxicity : the epithelium and stroma in iatrogenic and factitious disease. Eye (Lond) 2003 ; 17 : 886-92.
[40] Baudouin C, Labbé A, Liang H, et al. Preservatives in eyedrops : the good, the bad and the ugly. Progress in Retinal and Eye Research 2010 ; 29 : 312-34.
[41] Krasny J, Hruba D, Netukova M, et al. Chlamydia pneumoniae in the etiology of the keratoconjunctivitis sicca in adult patients (a pilot study). Cesk Slov Oftalmol 2009 ; 65 : 102-6.
[42] Meyer-Rusenberg B, Loderstadt U, Richard G, et al. Epidemic keratoconjunctivitis : the current situation and recommendations for prevention and treatment. Deutsches Arzteblatt International 2011 ; 108 : 475-80.
[43] M’Garrech M, Rousseau A, Kaswin G, et al. Impairment of lacrimal secretion in the unaffected fellow eye of patients with recurrent unilateral herpetic keratitis. Ophthalmology 2013 ; 120 : 1959-67.
[44] Lemp MA. Report of the National Eye Institute/Industry workshop on Clinical Trials in Dry Eyes. The CLAO Journal 1995 ; 21 : 221-32.
[45] DEWS. Research in dry eye : report of the Research Subcommittee of the International Dry Eye WorkShop (2007). The Ocular Surface 2007 ; 5 : 179-93.
[46] Gomes PJ, Ousler GW, Welch DL, et al. Exacerbation of signs and symptoms of allergic conjunctivitis by a controlled adverse environment challenge in subjects with a history of dry eye and ocular allergy. Clinical Ophthalmology 2013 ; 7 : 157-65.
[47] De Paiva CS, Chen Z, Koch DD, et al. The incidence and risk factors for developing dry eye after myopic LASIK. American Journal of Ophthalmology 2006 ; 141 : 438-45.
[48] Belmonte C, Acosta MC, Gallar J. Neural basis of sensation in intact and injured corneas. Experimental Eye Research 2004 ; 78 : 513-25.
[49] Pacella SJ, Codner MA. Minor complications after blepharoplasty : dry eyes, chemosis, granulomas, ptosis, and scleral show. Plastic and Reconstructive Surgery 2010 ; 125 : 709-18.
[50] Kasetsuwan N, Satitpitakul V, Changul T, et al. Incidence and pattern of dry eye after cataract surgery. PloS one 2013 ; 8 : e78657.
[51] Shoja MR, Besharati MR. Dry eye after LASIK for myopia : incidence and risk factors. European Journal of Ophthalmology 2007 ; 17 : 1-6.
[52] Brodrick JD. Anterior membrane dystrophy following cataract extraction. The British Journal of Ophthalmology 1979 ; 63 : 331-5.
[53] De Monchy I, Labbé A, Pogorzalek N, et al. Management of herpes zoster neurotrophic ulcer using a new matrix therapy agent (RGTA) : A case report. Journal Français d’Ophtalmologie 2012 ; 35 : 187.e1-6.
[54] Gabison EE, Chastang P, Menashi S, et al. Late corneal perforation after photorefractive keratectomy associated with topical diclofenac : involvement of matrix metalloproteinases. Ophthalmology 2003 ; 110 : 1626-31.
[55] Bourcier T, Saleh M, Dory A, Prévost G, Labetoulle M. Bacterial keratitis. Encycl Méd Chir (Elsevier, Paris). Ophtalmologie, 21200-D22. 2013.
[56] Ilhan N, Ilhan O, Ayhan Tuzcu E, et al. Is there a relationship between pathologic myopia and dry eye syndrome ? Cornea 2014 ; 33 : 169-71.
[57] Nassar A, Tabbara KF, Aljurf M. Ocular manifestations of graft-versus-host disease. Saudi Journal of Ophthalmology 2013 ; 27 : 215-22.
[58] Moss SE, Klein R, Klein BE. Incidence of dry eye in an older population. Archives of Ophthalmology 2004 ; 122 : 369-73.
[59] Rousseau A. Sclérites infectieuses. Rapport annuel des sociétés ophtalmologiques de France ; 2010.
[60] Ben Ayed CH, Hamédani M, Morax S. Ectropions. Encycl Méd Chir (Elsevier, Paris). Ophtalmologie. 2005.
[61] Bentivoglio AR, Bressman SB, Cassetta E, et al. Analysis of blink rate patterns in normal subjects. Movement Disorders 1997 ; 12 : 1028-34.
[62] Bonini S, Rama P, Olzi D, et al. Neurotrophic keratitis. Eye (Lond) 2003 ; 17 : 989-95.
[63] Adams WH, Digre KB, Patel BC, et al. The evaluation of light sensitivity in benign essential blepharospasm. American Journal of Ophthalmology 2006 ; 142 : 82-7.
[64] Girard B. Œil sec et blépharospasme essentiel : un élément de diagnostic positif, une clé du traitement. SOP 19 octobre 2009.
[65] Ounnoughene Y, Benhatchi N, Agboke J, et al. The Video Tearscope : a new method for evaluating lacrimal film in vivo. Journal Français d’Ophtalmologie 2006 ; 29 : 476-84.
[66] Lemp MA. Contact lenses and allergy. Current Opinion in Allergy and Clinical Immunology 2008 ; 8 : 457-60.
[67] Doan S, Gabison EE, Nghiem-Buffet S, et al. Long-term visual outcome of childhood blepharokeratoconjunctivitis. American Journal of Ophthalmology 2007 ; 143 : 528-9.
[68] Neiberg MN, Sowka J. Phlyctenular keratoconjunctivitis in a patient with Staphylococcal blepharitis and ocular rosacea. Optometry 2008 ; 79 : 133-7.
[69] Chang BH. Neurotrophic keratitis. In : Krachmer JH, Mannis MJ, Holland EJ. Eds. Cornea. St-Louis : Mosby ; 2010.
[70] Chopra SK, George S, Daniel R. Tear film break up time (B.U.T.) in non-contact lens wearers and contact lens wearers in normal Indian population. Indian Journal of Ophthalmology 1985 ; 33 : 213-6.
[71] Sweeney DF, Millar TJ, Raju SR. Tear film stability : a review. Experimental Eye Research 2013 ; 117 : 28-38.
[72] Labbé A, Brignole-Baudouin F, Baudouin C. Ocular surface investigations in dry eye. Journal Français d’Ophtalmologie 2007 ; 30 : 76-97.
[73] Farrell J, Grierson DJ, Patel S, et al. A classification for dry eyes following comparison of tear thinning time with Schirmer tear test. Acta ophthalmologica 1992 ; 70 : 357-60.
[74] Tabery HM. Dual appearance of fluorescein staining in vivo of diseased human corneal epithelium. A non-contact photomicrographic study. The British Journal of Ophthalmology 1992 ; 76 : 43-4.
[75] Mokhtarzadeh M, Casey R, Glasgow BJ. Fluorescein punctate staining traced to superficial corneal epithelial cells by impression cytology and confocal microscopy. Investigative Ophthalmology & Visual Science 2011 ; 52 : 2127-35.
[76] Machado LM, Castro RS, Fontes BM. Staining patterns in dry eye syndrome : rose bengal versus lissamine green. Cornea 2009 ; 28 : 732-4.
[77] Kim J, Foulks GN. Evaluation of the effect of lissamine green and rose bengal on human corneal epithelial cells. Cornea 1999 ; 18 : 328-32.
[78] Korb DR, Herman JP, Finnemore VM, et al. An evaluation of the efficacy of fluorescein, rose bengal, lissamine green, and a new dye mixture for ocular surface staining. Eye & Contact Lens 2008 ; 34 : 61-4.
[79] Bron AJ, Evans VE, Smith JA. Grading of corneal and conjunctival staining in the context of other dry eye tests. Cornea 2003 ; 22 : 640-50.
[80] Marshall PN. The composition of erythrosins, fluorescein, phloxine and rose Bengal : a study using thin-layer chromatography and solvent extraction. The Histochemical Journal 1976 ; 8 : 487-99.
[81] Doughty MJ, Hagan S. On the staining of human tissue-cultured (Chang) conjunctival cells with rose bengal and lissamine green. Contact Lens & Anterior Eye 2013 ; 36 : 32-40.
[82] Liotet S. Examen de la sécrétion lacrymale. Encycl Méd Chir (Elsevier, Paris). Ophtalmologie. 1197.
[83] Cho P, Leung L, Lam A, et al. Tear break-up time : clinical procedures and their effects. Ophthalmic & Physiological Optics 1998 ; 18 : 319-24.
[84] Cho P, Yap M. Age, gender, and tear break-up time. Optometry and Vision Science 1993 ; 70 : 828-31.
[85] Shapiro A, Merin S. Schirmer test and break-up time of tear film in normal subjects. American Journal of Ophthalmology 1979 ; 88 : 752-7.
[86] Yap M. Tear break-up time is related to blink frequency. Acta Ophthalmologica 1991 ; 69 : 92-4.
[87] Ousler GW ET, Welch D, Abelson MB. Facteurs qui influencent l’intervalle entre les clignements, tel que mesuré par l’indice de protection oculaire (IPO). The Association of Research in Vision and Ophthalmology (ARVO) ; 2002.
[88] Shen M, Li J, Wang J, et al. Upper and lower tear menisci in the diagnosis of dry eye. Investigative Ophthalmology & Visual Science 2009 ; 50 : 2722-6.
[89] Wang J, Palakuru JR, Aquavella JV. Correlations among upper and lower tear menisci, noninvasive tear break-up time, and the Schirmer test. American Journal of Ophthalmology 2008 ; 145 : 795-800.
[90] Zhou S, Li Y, Lu AT, et al. Reproducibility of tear meniscus measurement by Fourier-domain optical coherence tomography : a pilot study. Ophthalmic Surgery, Lasers & Imaging 2009 ; 40 : 442-7.
[91] Van Bijsterveld OP. Diagnostic tests in the Sicca syndrome. Archives of Ophthalmology 1969 ; 82 : 10-4.
[92] Efron N. Grading scales for contact lens complications. Ophthalmic & Physiological Optics 1998 ; 18 : 182-6.
[93] Terry RL, Schnider CM, Holden BA, et al. CCLRU standards for success of daily and extended wear contact lenses. Optometry and Vision Science 1993 ; 70 : 234-43.
[94] Miyata K, Amano S, Sawa M, et al. A novel grading method for superficial punctate keratopathy magnitude and its correlation with corneal epithelial permeability. Archives of Ophthalmology 2003 ; 121 : 1537-9.
[95] Whitcher JP, Shiboski CH, Shiboski SC, et al. A simplified quantitative method for assessing keratoconjunctivitis sicca from the Sjogren’s Syndrome International Registry. American Journal of Ophthalmology 2010 ; 149 : 405-15.
[96] Tomlinson A, Bron AJ, Korb DR, et al. The international workshop on meibomian gland dysfunction : report of the diagnosis subcommittee. Investigative Ophthalmology & Visual Science 2011 ; 52 : 2006-49.
[97] Sleiman R, Kurban M, Succaria F, et al. Poliosis circumscripta : overview and underlying causes. Journal of the American Academy of Dermatology 2013 ; 69 : 625-33.
[98] Karalezli A, Borazan M, Dursun R, et al. Impression cytology and ocular surface characteristics in patients with seborrhoeic dermatitis. Acta Ophthalmol 2011 ; 89 : e137-41.
[99] Schirmer O. Studies on the physiology and pathology of the secretion and drainage of tears. Albrecht von Graefes Arch Klin Ophthalmol 1903 ; 56 : 197-291.
[100] Jones LT, Wobig JL. The Wendell L. Hughes lecture. Newer concepts of tear duct and eyelid anatomy and treatment. Transactions Section on Ophthalmology American Academy of Ophthalmology and Otolaryngology 1977 ; 831 : 603-16.
[101] Lamberts DW, Foster CS, Perry HD. Schirmer test after topical anesthesia and the tear meniscus height in normal eyes. Archives of Ophthalmology 1979 ; 97 : 1082-5.
[102] Nichols KK, Mitchell GL, Zadnik K. The repeatability of clinical measurements of dry eye. Cornea 2004 ; 23 : 272-85.
[103] Serin D, Karsloglu S, Kyan A, et al. A simple approach to the repeatability of the Schirmer test without anesthesia : eyes open or closed ? Cornea 2007 ; 26 : 903-6.
[104] Bitton E, Wittich W. Influence of eye position on the Schirmer tear test. Contact Lens & Anterior 2014 ; 37 : 257-61.
[105] Sakamoto R, Bennett ES, Henry VA, et al. The phenol red thread tear test : a cross-cultural study. Investigative Ophthalmology & Visual Science 1993 ; 34 : 3510-4.
[106] Farris RL. Tear osmolarity--a new gold standard ? Advances in experimental medicine and biology. 1994 ; 350 : 495-503.
[107] De Monchy I, Gendron G, Miceli C, et al. Combination of the Schirmer I and phenol red thread tests as a rescue strategy for diagnosis of ocular dryness associated with Sjogren’s syndrome. Investigative Ophthalmology & Visual Science 2011 ; 52 : 5167-73.
[108] Afonso AA, Monroy D, Stern ME, et al. Correlation of tear fluorescein clearance and Schirmer test scores with ocular irritation symptoms. Ophthalmology 1999 ; 106 : 803-10.
[109] Gilbard JP, Farris RL. Tear osmolarity and ocular surface disease in keratoconjunctivitis sicca. Archives of Ophthalmology 1979 ; 97 : 1642-6.
[110] Josephson JE, Caffery BE. Corneal staining after instillation of topical anesthetic (SSII). Investigative Ophthalmology & Visual Science 1988 ; 29 : 1096-9.
[111] Patel S, Farrell J, Blades KJ, et al. The value of a phenol red impregnated thread for differentiating between the aqueous and non-aqueous deficient dry eye. Ophthalmic & Physiological Optics 1998 ; 18 : 471-6.
[112] Labetoulle M, Mariette X, Joyeau L, et al. The phenol red thread first results for the assessment of the cut-off value in ocular sicca syndrome. Journal Français d’Ophtalmologie 2002 ; 25 : 674-80.
[113] Doughty MJ, Whyte J, Li W. The phenol red thread test for lacrimal volume--does it matter if the eyes are open or closed ? Ophthalmic & Physiological Optics 2007 ; 27 : 482-9.
[114] Norn MS. Lacrimal apparatus tests. A new method (lacrimal streak dilution test) compared with previous methods. Acta Ophthalmologica 1965 ; 43 : 557-66.
[115] McCann LC, Tomlinson A, Pearce EI, et al. A clinical alternative to fluorophotometry for measuring tear production in the diagnosis of dry eye. Cornea 2010 ; 29 : 745-50.
[116] Lucca JA, Nunez JN, Farris RL. A comparison of diagnostic tests for keratoconjunctivitis sicca : lactoplate, Schirmer, and tear osmolarity. The CLAO Journal 1990 ; 16 : 109-12.
[117] Farris RL, Stuchell RN, Mandel ID. Basal and reflex human tear analysis. I. Physical measurements : osmolarity, basal volumes, and reflex flow rate. Ophthalmology 1981 ; 88 : 852-7.
[118] Mainstone JC, Bruce AS, Golding TR. Tear meniscus measurement in the diagnosis of dry eye. Current Eye Research 1996 ; 15 : 653-61.
[119] Yokoi N, Komuro A. Non-invasive methods of assessing the tear film. Experimental Eye Research 2004 ; 78 : 399-407.
[120] Vitali C, Moutsopoulos HM, Bombardieri S. The European Community Study Group on diagnostic criteria for Sjogren’s syndrome. Sensitivity and specificity of tests for ocular and oral involvement in Sjogren’s syndrome. Annals of the Rheumatic Diseases 1994 ; 53 : 637-47.
[121] Mengher LS, Bron AJ, Tonge SR, et al. A non-invasive instrument for clinical assessment of the pre-corneal tear film stability. Current Eye Research 1985 ; 4 : 1-7.
[122] Goren MB, Goren SB. Diagnostic tests in patients with symptoms of keratoconjunctivitis sicca. American Journal of Ophthalmology 1988 ; 106 : 570-4.
[123] Murphy PJ, Lawrenson JG, Patel S, et al. Reliability of the non-contact corneal aesthesiometer and its comparison with the Cochet-Bonnet aesthesiometer. Ophthalmic & Physiological Optics 1998 ; 18 : 532-9.
[124] Draeger J. Corneal sensitivity. Measurement and clinical importance. Springer-Verlag ; 1984.
[125] Bourcier T, Acosta MC, Borderie V, et al. Decreased corneal sensitivity in patients with dry eye. Investigative Ophthalmology & Visual Science 2005 ; 46 : 2341-5.
A. Labbé, S. Kallel, B. Dupas, H. Liang, E. Brasnu, R. Tahiri Joutei Hassani, A. Denoyer, C. Baudouin
Plusieurs techniques d’imagerie morphologique de la surface oculaire sont désormais accessibles aux cliniciens. Parmi celles-ci, la microscopie confocale in vivo (in vivo confocal microscopy ou IVCM) et la tomographie par cohérence optique (optical coherence tomography ou OCT) offrent des approches nouvelles, respectivement microscopique et macroscopique.
La microscopie confocale in vivo est une technique non invasive permettant d’obtenir des images de haute résolution de l’ensemble des tissus qui composent la surface oculaire. Elle est principalement utilisée dans les kératites infectieuses, les dystrophies de la cornée et la chirurgie cornéenne. Elle nécessite un apprentissage pour obtenir des images de bonne qualité et savoir les interpréter.
La tomographie par cohérence optique est une technique d’imagerie non-contact qui permet d’obtenir des coupes anatomiques de résolution tissulaire de la surface oculaire et du segment antérieur. En pratique clinique, elle est principalement utilisée pour obtenir des mesures quantitatives des structures cornéennes.
En pratique clinique, l’analyse morphologique des tissus qui composent la surface oculaire est largement dominée par la biomicroscopie, l’examen à la lampe à fente restant limité par sa résolution qui ne permet pas toujours d’appréhender les modifications tissulaires pathologiques mais aussi physiologiques. Initialement réservée au domaine de la recherche, la microscopie confocale in vivo ou in vivo confocal microscopy (IVCM) est devenue aujourd’hui un outil d’imagerie de résolution quasi histologique directement accessible aux cliniciens. Cette technique est utilisée pour analyser les modifications cellulaires et tissulaires impliquées dans de nombreuses pathologies de la surface oculaire comme les kératites infectieuses, les dystrophies cornéennes ou encore la sécheresse oculaire, mais aussi après chirurgie cornéenne et réfractive ou encore dans le glaucome. Plus récemment encore, les techniques d’imagerie par tomographie par cohérence optique ou optical coherence tomography (OCT) se sont également développées pour l’évaluation du segment antérieur (anterior segment optical coherence tomography ou AS-OCT). Elles permettent d’obtenir, sans contact avec l’œil du patient, des coupes des tissus qui composent la surface oculaire. Cette nouvelle imagerie du segment antérieur a ainsi trouvé de nombreuses applications dans le domaine de la surface oculaire en particulier dans les greffes de la cornée ou les dystrophies cornéennes. Les développements récents et rapides de ces deux techniques d’imagerie morphologique de la surface oculaire laissent entrevoir pour le futur des applications de plus en plus nombreuses et bientôt incontournables en pratique clinique.
Le principe de la microscopie optique conventionnelle et de la biomicroscopie est l’observation d’une image réfléchie au travers d’un objectif contenant une ou plusieurs lentilles, après illumination de l’objet étudié par un faisceau lumineux focalisé. Le principal facteur limitant de cette technique est que la lumière réfléchie sur les structures adjacentes au point d’observation brouille l’image observée, réduisant ainsi la résolution et le contraste. Le principe de microscopie confocale a été décrit pour la première fois par Minsky en 1955 pour l’étude du parenchyme cérébral [1]. Il a ainsi proposé que les systèmes d’observation et d’illumination soient focalisés en un même point, d’où le nom de microscopie confocale. La lumière réfléchie par les éléments situés en dehors du point focal est alors exclue de l’image finale ce qui réduit les interférences lumineuses (diffusion, réflexion et diffraction) et augmente considérablement la résolution ainsi que le contraste des images obtenues. Ainsi, la microscopie confocale in vivo permet des résolutions axiales et latérales de l’ordre de quelques microns. Cette amélioration de la résolution spatiale se fait cependant au prix d’une réduction importante du champ d’observation ainsi obtenu (point focal). Il est donc nécessaire de rapidement observer le point adjacent et de reconstruire l’image pour permettre l’observation en direct de la structure examinée dans son ensemble [1].
Trois grands types de microscopes confocaux in vivo utilisables en pratique clinique ont été développés, la différence portant essentiellement sur la technique utilisée pour analyser rapidement l’ensemble des points qui constituent l’image et sur la source lumineuse utilisée : les microscopes confocaux tandem scanning confocal microscopy (TSCM) et slit-scanning confocal microscopy (SSCM), et le microscope confocal à balayage laser ou confocal laser scanning microscopy (CLSM) [1, 2]. Grâce à des systèmes numériques performants, l’IVCM offre aujourd’hui une résolution de l’ordre du micron et ceci malgré les mouvements souvent involontaires du patient. L’utilisateur d’un microscope confocal doit néanmoins se familiariser avec l’aspect des tissus, vus sans préparation et dans un plan coronal, l’image étant parallèle à la surface examinée.
À l’exception de la membrane de Descemet normale, l’IVCM permet d’obtenir des images de l’ensemble des couches de la cornée. La plupart de ces images sont parallèles à la surface cornéenne (ou coronales) mais parfois des images transversales, similaires aux coupes histologiques, peuvent être obtenues (fig. 2-12a).

Fig. 2-12 Image de microscopie confocale in vivo (HRT-RCM®, Heidelberg Engineering, Heidelberg, Allemagne) de la cornée normale (400 µm × 400 µm).
a. Image de la cornée en coupe montrant l’épithélium superficiel, la membrane de Bowman ainsi que les nerfs cornéens sous-épithéliaux. b. Cellules épithéliales superficielles. c. Cellules épithéliales intermédiaires. d. Cellules épithéliales basales. e, f. Plexus nerveux sous-épithéliaux. g. Couche de Bowman avec des nerfs cornéens visibles. h. Cellules hyperréflectives de formes dendritiques au niveau sous-épithélial.
Trois types de cellules épithéliales sont observés au niveau de l’épithélium : les cellules superficielles, intermédiaires et basales. Les cellules superficielles ont une forme polygonale, souvent hexagonale, et une réflectivité variable avec un noyau visible (fig. 2-12b) [1, 3]. Les cellules en voie de desquamation sont caractérisées par un cytoplasme hyperréflectif avec un noyau visible et parfois un halo noir périnucléaire. La densité moyenne des cellules de cette couche est comprise entre 759 et 1213 cellules/mm2 [1, 3].
Les cellules épithéliales intermédiaires ou wing cells sont de forme plus régulière avec un diamètre de 20 µm environ (fig. 2-12c). Elles sont caractérisées par des limites cellulaires hyperréflectives, un cytoplasme hyporéflectif et un noyau rarement visible [1, 3]. La densité moyenne des cellules de cette couche est de 5 000 à 5 500 cellules/mm2 [1, 3].
La couche des cellules épithéliales basales apparaît sous la forme d’une mosaïque de cellules plus petites (8–10 µm de diamètre) avec un cytoplasme hyporéflectif, des bords hyperréflectifs et l’absence de noyau visible (fig. 2-12d) [1, 3]. La densité de cette couche cellulaire varie entre 6 000 et 10 000 cellules/mm2 [1, 3].
Les plexus nerveux sous-épithéliaux sont situés entre le stroma antérieur et la couche basale de l’épithélium. Contrairement aux terminaisons nerveuses épithéliales qui ne sont pas visibles en IVCM, ils apparaissent comme de fines structures linéaires hyperréflectives de quelques microns d’épaisseur avec de nombreux branchements et bifurcations (fig. 2-12e et f) [1, 4]. La densité moyenne des plexus nerveux sous-épithéliaux au centre de la cornée chez les sujets normaux varie entre 0,58 et 25,9 mm/mm2 [4]. Cette variabilité de mesure est expliquée par les différentes méthodes de quantification et le type de microscope confocal utilisé [4, 5]. Par ailleurs, cette densité serait aussi corrélée à l’âge avec une diminution de la densité nerveuse associée au vieillissement.
La couche de Bowman apparaît comme une couche amorphe de 8 à 10 µm d’épaisseur, située entre les cellules basales de l’épithélium et le stroma (fig. 2-12g) [1, 3]. Elle est souvent reconnue par la présence des plexus nerveux sous-épithéliaux. Des cellules de forme dendritique sont également observées en IVCM entre l’épithélium basal et le stroma antérieur chez les sujets normaux (fig. 2-12h).
Au niveau du stroma cornéen, seuls les nerfs et les noyaux des kératocytes sont clairement observés en IVCM [1, 3]. Les noyaux des kératocytes sont visualisés sous la forme de structures hyperréflectives ovales ou rondes (fig. 2-13a). Le cytoplasme des kératocytes ainsi que les fibres de collagène ne sont pas visibles et apparaissent sous la forme d’un arrière-plan hyporéflectif. La densité des kératocytes varie en fonction de la localisation au sein du stroma, la densité la plus importante étant retrouvée au niveau du stroma antérieur juste en arrière de la couche de Bowman (entre 40 000 et 19 000 cellules/mm3), et diminue avec l’âge (fig. 2-13b) [1, 3].
Les nerfs du stroma apparaissent comme des structures linéaires hyperréflectives plus larges que les plexus nerveux sous-épithéliaux et qui présentent parfois des branches dichotomiques visibles (fig. 2-13c) [3].

Fig. 2-13 Images de microscopie confocale in vivo (HRT-RCM®) de la cornée normale (400 µm × 400 µm).
a. Noyaux de kératocytes hyperréflectifs au sein d’une matrice extracellulaire hyporéflective dans le stroma antérieur. b. Stroma postérieur. c. Stroma moyen avec un tronc nerveux. d. Endothélium normal.
La membrane de Descemet est visualisée sous la forme d’une fine couche (6–8 µm) amorphe et acellulaire située entre le stroma postérieur et l’endothélium. Cette couche n’est pas visible chez les sujets jeunes et sains [1, 3].
L’endothélium cornéen normal correspond à une monocouche de cellules hexagonales réflectives avec des limites hyporéflectives et sans noyau visible, disposées en nids d’abeilles (fig. 2-13d) [1, 3]. La densité des cellules endothéliales mesurées en IVCM varie chez le sujet normal entre 2 500 et 3 100 cellules/mm2, et diminue avec l’âge [1, 3].
Non seulement la cornée mais aussi le limbe et la conjonctive peuvent être analysés en IVCM. Au niveau superficiel, le limbe correspond à la jonction entre l’épithélium conjonctival hyperréflectif et l’épithélium cornéen bien structuré et hyporéflectif (fig. 2-14a). Au niveau limbique, les cellules épithéliales ont une taille et une réflectivité variables (fig. 2-14b) [3]. Plus en profondeur, cette zone de jonction est aussi caractérisée par la présence de palissades de Vogt qui apparaissent comme des palissades hyperréflectives et perpendiculaires au limbe, entourées de cellules hyperréflectives qui s’étendent de la conjonctive à l’épithélium cornéen (fig. 2-14c et d) [1, 3]. Cet aspect serait néanmoins très variable d’un individu à l’autre. Au niveau du limbe, des cellules de type dendritique sont également présentes à l’état normal (fig. 2-14e).

Fig. 2-14 Images de microscopie confocale in vivo (HRT-RCM®) du limbe normal (400 µm × 400 µm).
a. Épithélium superficiel du limbe avec les cellules cornéennes hyporéflectives et les cellules conjonctivales hyperréflectives. b. Couche plus profonde de l’épithélium limbique sur le versant conjonctival. c, d. Palissades de Vogt. e. Cellules hyperréflectives de type dendritique au limbe.
L’épithélium superficiel de la conjonctive bulbaire est hyperréflectif en IVCM avec des cellules épithéliales dont les limites sont parfois visibles (fig. 2-15a) et dont la taille serait approximativement de 10 µm [3]. Les noyaux des cellules épithéliales sont également hyperréflectifs et régulièrement espacés [3]. Dans les couches plus profondes de l’épithélium conjonctival, les cellules épithéliales apparaissent plus petites mais avec une forme et une taille variables (fig. 2-15b). Ces dernières sont hyperréflectives avec des limites bien définies et pas de noyau visible. Les cellules à mucus peuvent être observées au sein de l’épithélium conjonctival sous la forme de cellules rondes ou ovales, plus réflectives et plus larges que les cellules épithéliales (fig. 2-15c) [6]. Elles sont distribuées de manière aléatoire au sein de l’épithélium conjonctival et parfois groupées en amas. Des images rondes hyporéflectives de taille variable correspondant à des microkystes et des cellules hyperréflectives de type dendritique peuvent être aussi observées lors de l’examen en IVCM de l’épithélium conjonctival normal (fig. 2-15d) [6]. Dans les couches plus profondes, le stroma conjonctival apparaît sous la forme d’un réseau de fibres arrangées de manière anarchique (fig. 2-15e) [6]. Des vaisseaux sanguins sont également visualisés au sein du stroma conjonctival.
Les images obtenues lors de l’analyse de la conjonctive palpébrale sont comparables à celles de la conjonctive bulbaire avec des cellules épithéliales légèrement plus grandes (de 10 à 15 µm) et des cellules à mucus plus nombreuses [7]. Si l’examen est réalisé à proximité de la marge palpébrale et plus en profondeur, on observe des structures adénoïdes correspondant aux glandes de Meibomius. Certains auteurs ont également décrit en IVCM au niveau de la conjonctive palpébrale le CALT, ou conjunctiva-associated lymphoid tissue, qui correspond à des follicules lymphoïdes situés sous l’épithélium [3].

Fig. 2-15 Images de microscopie confocale in vivo (HRT-RCM®) de la conjonctive normale (400 µm × 400 µm).
a. Épithélium conjonctival superficiel. b. Couche plus profonde de l’épithélium conjonctival. c. Cellules à mucus (rondes, plus réflectives) au sein de l’épithélium conjonctival. d. Cellules hyperréflectives de type dendritique au sein de l’épithélium conjonctival. e. Stroma conjonctival.
Les couches cellulaires les plus superficielles des paupières peuvent être visualisées en IVCM. Les cellules épithéliales qui recouvrent le bord palpébral sont hyperréflectives avec une taille variable. Les orifices des glandes de Meibomius apparaissent sous la forme d’une zone hyporéflective ronde avec un contenu parfois inhomogène (fig. 2-16a) [8]. Plus profondément, l’épithélium glandulaire est très hyperréflectif et organisé en lobules ou acini entourés d’un tissu conjonctif hyporéflectif (fig. 2-16b). Les sécrétions meibomiennes peuvent également être visualisées au sein des acini et leur réflectivité analysée [8].
Grâce au développement d’objectifs non-contact, des images du film lacrymal peuvent être réalisées en IVCM, mais la place exacte de cette technique pour l’analyse du film lacrymal doit encore être précisée.

Fig. 2-16 Images de microscopie confocale in vivo (HRT-RCM®) des glandes de Meibomius (400 µm × 400 µm).
a. Orifice. b. Épithélium glandulaire.
Une kératite infectieuse est caractérisée par une inflammation cornéenne causée par un micro-organisme comme une bactérie, un virus, un champignon ou une amibe [9]. Les kératites infectieuses restent des pathologies sévères pouvant entraîner des complications irréversibles allant jusqu’à la cécité. Un diagnostic rapide, ou même la suspicion d’un organisme infectieux responsable permettant la mise en route d’un traitement efficace, serait un des facteurs pronostiques majeurs des kératites infectieuses. En permettant de visualiser directement certains micro-organismes, l’IVCM est ainsi utilisée en complément de l’examen clinique et microbiologique pour le diagnostic et le suivi des kératites infectieuses [2, 9]. Cependant, alors que sa valeur a été démontrée pour le diagnostic et la prise en charge des kératites amibiennes et fongiques, la résolution de cette technique d’imagerie limite encore son utilisation en cas de kératite bactérienne et virale.
Contrairement aux virus et aux bactéries, la taille des kystes d’Acanthamœba (forme quiescente) et des trophozoïtes (forme active) permet leur visualisation directement en IVCM. De nombreuses publications ont décrit son utilisation comme outil diagnostique mais aussi pour évaluer la réponse au traitement des kératites amibiennes [2, 9–11].
Les kystes sont les structures les plus communément observées en IVCM dans les kératites amibiennes. Ils apparaissent au sein de l’épithélium et/ou du stroma sous la forme de structures hyperréflectives, sphériques, rondes ou ovales, avec parfois une double paroi visible (fig. 2-17a à c), et dont le diamètre varie le plus souvent de 10 à 30 µm [9–11]. Cet aspect en double paroi n’est pas toujours présent et dépend du plan des images et de la réflectivité des tissus avoisinants. Lorsque cet aspect caractéristique n’est pas visible, la différenciation entre les kystes et d’autres structures hyperréflectives, comme les leucocytes, les lymphocytes ou encore les débris cellulaires, est difficile. Malgré une taille souvent similaire, l’hyperréflectivité et le contraste des kystes amibiens peuvent aider à les différencier des cellules avoisinantes [9]. L’IVCM permet aussi de visualiser les trophozoïtes. Ils sont hyperréflectifs avec des formes variables, le plus souvent ovales, et une taille allant de 15 à 100 µm (fig. 2-17d et e) [2, 9–11]. Compte tenu de leur forme moins typique que celle des kystes, ils sont plus difficiles à discerner des autres structures hyperréflectives adjacentes [2, 9]. La présence d’extensions de type pseudopodes serait un signe utile pour les différencier. Enfin, l’IVCM retrouve parfois des nerfs élargis évocateurs de kératonévrite radiaire, des modifications du stroma cornéen avec des cavités hyporéflectives, un œdème stromal, une infiltration par des cellules inflammatoires, des kératocytes activés hyperréflectifs ou encore des cicatrices extensives [2, 9].
Depuis plus de 10 ans maintenant, de nombreuses publications ont souligné l’intérêt diagnostic de l’IVCM dans les kératites amibiennes avec une sensibilité de 55,8 à 100 % et une spécificité de 77,3 à 100 % [2, 9–11]. Parce qu’il s’agit d’une technique non invasive, l’examen peut être répété facilement durant l’évolution de la maladie. L’IVCM a donc un potentiel non seulement pour le diagnostic mais aussi pour le suivi et l’évaluation de l’efficacité thérapeutique dans les kératites amibiennes. Ainsi, l’IVCM a été utilisée pour différencier une atteinte toxique de la progression de l’infection à Acanthamœba ou encore pour rechercher la persistance de kystes avant une greffe de la cornée [9–11].

Fig. 2-17 Images de microscopie confocale in vivo (HRT-RCM®) dans les kératites infectieuses (400 µm × 400 µm).
a, b, c. Les kystes amibiens apparaissent sous la forme de structures hyperréflectives, sphériques, rondes ou ovales, avec parfois une double paroi visible, et dont le diamètre varie le plus souvent de 10 à 30 µm. c. Parfois, les kystes amibiens apparaissent groupés en chaînettes. d, e. Les trophozoïtes sont hyperréflectifs avec des formes variables, le plus souvent ovales, et une taille allant de 15 à 100 µm. f–h. Les champignons filamenteux apparaissent comme un entrecroisement de lignes hyperréflectives d’approximativement 200 à 400 µm de long et de 3 à 6 µm de large. i. Infiltration majeure de cellules inflammatoires au sein de l’épithélium dans une kératite bactérienne. j. Modifications tissulaires avec infiltration diffuse de cellules dendritiques et destruction des nerfs sous-épithéliaux dans une kératite herpétique. k. Infiltration sous-épithéliale localisée de cellules de type dendritique dans une kératite à adénovirus.
Les kératites fongiques sont des kératites sévères avec une présentation clinique souvent non spécifique et un risque important de morbidité oculaire. L’IVCM a donc été utilisée non seulement pour le diagnostic, mais aussi pour évaluer l’efficacité du traitement lors du suivi [9–11]. Ce sont essentiellement les champignons filamenteux (Fusarium et Aspergillus) qui peuvent être visualisés en IVCM. Toutefois, quelques publications ont également décrit des levures ou encore Microsporidium [9].
Les champignons filamenteux apparaissent en IVCM comme un entrecroisement de lignes hyperréflectives d’approximativement 200 à 400 µm de long et de 3 à 6 µm de large au niveau du stroma antérieur ou de l’épithélium cornéen (fig. 2-17f à h) [9, 12]. Ces filaments hyperréflectifs peuvent être distingués des nerfs cornéens épithéliaux et sous-épithéliaux qui ont un nombre de branchements relativement plus faible comparé aux très nombreux branchements chaotiques observés avec les champignons filamenteux. Les nerfs du stroma sont plus larges en diamètre (25–50 µm) et situés plus profondément dans le stroma. Certains auteurs distingueraient également les champignons de type Fusarium dont les ramifications se feraient avec un angle de 90° et les champignons de type Aspergillus dont l’angle serait à 45° [12]. Les levures, comme Candida albicans, ont été décrites sous la forme de multiples particules réflectives allongées mesurant 10 à 40 µm de longueur et 5 à 10 µm de largeur dans le stroma antérieur [12]. D’autres micro-organismes de type fongique comme Microsporidium, Beauveria Bassiana, Alternaria alternate ou encore Penicillium ont aussi été décrits en IVCM, mais l’utilité de cette technique d’imagerie pour leur diagnostic reste encore à déterminer [9].
Plusieurs travaux ont évalué la sensibilité et la spécificité diagnostiques de l’IVCM dans les kératites fongiques [2, 9, 11]. Kanavi et al. ont ainsi retrouvé une sensibilité de 94 % et une spécificité de 78 % pour le diagnostic des kératites fongiques sans distinction du type de champignon [13]. Plus récemment, dans une étude portant sur 103 cas de kératites amibiennes ou fongiques prouvées microbiologiquement, Vaddavali et al. ont retrouvé une sensibilité diagnostique de l’IVCM de 88,3 % pour une spécificité de 91,1 % [10]. Malgré ces travaux, la place exacte de l’IVCM pour le diagnostic des kératites fongiques nécessite encore d’être précisée [2, 9]. À l’image des kératites amibiennes, l’IVCM pourrait néanmoins être aussi utile pour l’évaluation et le suivi des traitements des kératites fongiques. Shi et al. ont ainsi utilisé l’IVCM pour guider le traitement chez 121 patients qui présentaient une kératite fongique et ont confirmé l’intérêt de cette technique rapide et non invasive [14]. D’autres auteurs ont également utilisé cette technique d’imagerie avant la réalisation d’une greffe de cornée afin de vérifier l’absence d’infection fongique active [9].
Parce que la plupart des bactéries ont une taille inférieure ou proche de la limite de résolution de l’IVCM, peu d’études ont décrit les aspects des kératites bactériennes avec cette technique d’imagerie. Quelques bactéries, comme Bacillus cereus, Borrelia burgdorferi ou Nocardia, qui ont une morphologie particulière ou une grande taille permettant leur visualisation et leur reconnaissance en IVCM, ont néanmoins été décrites [2, 9]. Certains changements tissulaires associés aux kératites bactériennes, comme l’infiltration de cellules inflammatoires (fig. 2-17i) ou la cicatrisation stromale, ont été aussi observés en IVCM [2, 9, 11].
À l’image des kératites bactériennes, l’utilité de l’IVCM pour le diagnostic et la prise en charge des kératites virales est encore limitée par sa résolution [9, 11]. L’IVCM a donc été utilisée pour évaluer les altérations tissulaires induites par les infections virales, à herpes simplex virus (HSV) et adénovirus en particulier, mais peu d’études ont réellement analysé son potentiel en tant qu’outil diagnostique. Les altérations des nerfs sous-épithéliaux ou l’infiltration de cellules de forme dendritique ont été évaluées en IVCM dans la kératite herpétique (fig. 2-17j). Cette technique d’imagerie a également été utilisée pour décrire de nouvelles formes cliniques comme la kératite en archipel [15]. L’IVCM serait par ailleurs aussi utile pour le diagnostic différentiel des pathologies associées à un œdème de cornée comme la kératite disciforme à HSV, le syndrome irido-cornéo-endothélial (ICE) ou encore la dystrophie de Fuchs [9]. Dans les kératites à adénovirus, les infiltrats sous-épithéliaux de cellules dendritiques ont pu être précisés et suivis dans le temps (fig. 2-17k) [16].
L’analyse des modifications tissulaires cornéennes dans les dystrophies de la cornée a été une des premières applications de l’IVCM. Depuis, cette technique d’imagerie est devenue une aide précieuse pour préciser et localiser les changements tissulaires mais aussi guider la thérapeutique dans les dystrophies cornéennes, les pathologies de surcharge et les pathologies endothéliales [1].
L’ensemble des dystrophies épithéliales et stromales ont été décrites en IVCM [1, 17]. La dystrophie microkystique de Meesmann se traduit par des zones hyporéflectives mesurant entre 40 et 150 µm, et ressemblant à des kystes au niveau de la couche basale de l’épithélium (fig. 2-18a). Des structures hyperréflectives sont parfois observées au sein de ces lésions kystiques et pourraient correspondre au matériel fibrogranulaire décrit en histologie. Dans la dystrophie de Lisch, on retrouve de nombreuses structures rondes hyporéflectives bien limitées par un tissu hyperréflectif (fig. 2-18b) [18]. Dans la dystrophie de la membrane basale ou dystrophie de Cogan, on observe en IVCM des structures hyperréflectives, linéaires ou incurvées au niveau des couches des cellules épithéliales intermédiaires et basales, correspondant à l’insinuation d’une membrane basale épaissie et anormale au sein de l’épithélium cornéen [19]. Des anomalies des cellules épithéliales et des microkystes intra-épithéliaux sont aussi associés (fig. 2-18c et d) [19]. Dans les kératites en bandelettes, les dépôts calciques apparaissent sous la forme de grandes plages très hyperréflectives à bords irréguliers, situées au niveau de l’épithélium. Dans les dystrophies de la couche de Bowman, l’IVCM permet de mettre en évidence des dépôts hyperréflectifs au niveau de cette membrane. La disposition et l’aspect en IVCM de ces dépôts pourraient permettre aussi de distinguer certaines dystrophies. Par exemple, dans la dystrophie de Thiel-Behnke, les dépôts ont une réflectivité homogène avec une zone d’ombre entourant des bords arrondis, alors que dans la dystrophie de Reis-Bücklers les dépôts sont plus fins, granuleux, hyperréflectifs et sans zone d’ombre périphérique (fig. 2-18e) [1]. Dans la dystrophie granulaire (ou de Groenouw de type I), on observe des dépôts irréguliers hyperréflectifs dans l’épithélium, la couche de Bowman et le stroma antérieur où ils peuvent prendre un aspect en « flocons de neige ». Au niveau du stroma postérieur, les dépôts sont de plus petite taille, voire punctiformes [20]. Les aspects en IVCM de la dystrophie maculaire (ou Groenouw de type II) ont été décrits comme la présence de dépôts hyperréflectifs à bords nets au sein de la couche basale de l’épithélium et du stroma, où ils sont associés à des stries plus sombres [21]. Dans la dystrophie grillagée ou lattice corneal dystrophy, les dépôts d’amylose sont visualisés sous la forme de structures linéaires hyporéflectives de taille variable et localisées au sein du stroma [21]. La dystrophie d’Avellino montre en IVCM des dépôts hyperréflectifs à bords irréguliers, d’assez grande taille, plutôt de type granulaire [21]. Enfin, en cas de dystrophie de Schnyder, on retrouve au stade précoce des dépôts hyperréflectifs entre les kératocytes et autour des plexus nerveux sous-épithéliaux (fig. 2-18f). Puis de véritables cristaux allongés et très hyperréflectifs apparaissent, désorganisant l’architecture et l’innervation du stroma [22, 23].

Fig. 2-18 Images de microscopie confocale in vivo (HRT-RCM®) dans les dystrophies cornéennes, les pathologies de surcharge et les atteintes endothéliales (400 µm × 400 µm).
a. Aspect de microkystes épithéliaux dans la dystrophie de Meesmann. b. Structures rondes hyporéflectives bien limitées au sein d’un tissu hyperréflectif dans une dystrophie de Lisch. c, d. Membrane basale anormale au sein de l’épithélium dans une dystrophie de Cogan. e. Dépôt de matériel anormal au niveau de la membrane de Bowman dans une dystrophie de Reis-Bücklers. f. Cristaux hyperréflectifs au sein du stroma dans une dystrophie de Schnyder. g. Dépôts épithéliaux d’amiodarone. h. Dépôts épithéliaux de cristaux de cystine dans une cystinose. i. Dépôts de cristaux de cystine au sein du stroma. j. Aspect de cornea guttata avec gouttes endothéliales. k. Polymégathisme et pléomorphisme cellulaire endothélial. l. Aspect épithélioïde des cellules endothéliales dans un syndrome irido-cornéo-endothélial.
Les dépôts d’amiodarone sont visualisés en IVCM sous la forme d’inclusions épithéliales hyperréflectives intracellulaires (fig. 2-18g) [1]. Dans les formes plus avancées, les autres couches de la cornée peuvent présenter ce type d’inclusions. Cet aspect est similaire à celui observé pour les dépôts de chloroquine [24]. Certaines maladies systémiques comme la maladie de Fabry ou encore la cystinose se caractérisent par une accumulation de matériel anormal au niveau des différentes couches de la cornée. Dans la cystinose, on observe ainsi des cristaux de cystine sous la forme de dépôts fusiformes hyperréflectifs au niveau de toutes les couches de la cornée excepté l’endothélium (fig. 2-18h et i) [25]. Dans la maladie de Fabry, l’IVCM retrouve des lésions sous la forme d’inclusions intracellulaires hyperréflectives au niveau de la couche basale de l’épithélium cornéen associées à des inclusions conjonctivales prédominant au niveau de la conjonctive tarsale [26].
Dans la dystrophie endothéliale de Fuchs, l’IVCM met en évidence des gouttes qui apparaissent comme des structures rondes hyporéflectives avec parfois un matériel réflectif central (fig. 2-18j) [1]. Ces images sont associées à un polymégathisme, un pléiomorphisme cellulaire et à une diminution de la densité cellulaire endothéliale qui peut également être quantifiée en IVCM (fig. 2-18k). Dans la dystrophie postérieure polymorphe, on retrouve des lésions curvilignes et vésiculaires ainsi que des zones focales d’accumulation de particules hypo- et hyperréflectives associées à des stries au niveau de la membrane de Descemet [27]. Enfin, dans les syndromes irido-cornéo-endothéliaux (ICE), des cellules épithélioïdes réflectives de grande taille et de formes irrégulières avec des bords flous et des noyaux visibles sont observées (fig. 2-18l) [1].
La sécheresse oculaire est l’une des pathologies les plus fréquentes de la surface oculaire. Outre les anomalies du film lacrymal, elle est caractérisée par de nombreux changements au niveau des tissus qui composent la surface oculaire comme la cornée, la conjonctive ou encore les paupières. Ces modifications tissulaires peuvent être évaluées en IVCM et cette technique d’imagerie a été largement utilisée pour préciser les altérations morphologiques des tissus de la surface oculaire en cas de sécheresse oculaire [1, 3]. La microscopie confocale offre ainsi de nouvelles opportunités pour comprendre les mécanismes physiopathologiques complexes liés à cette pathologie.
Au niveau de l’épithélium cornéen superficiel, la présence de cellules épithéliales de taille variable est caractéristique, avec une augmentation des cellules hyperréflectives (en desquamation) et un noyau bien visible (fig. 2-19a) [3]. Dans les atteintes plus sévères, les couches profondes de l’épithélium peuvent également être touchées avec des cellules basales de plus grande taille et des noyaux visibles (fig. 2-19b). Ces changements s’accompagnent d’une diminution de la densité des cellules épithéliales superficielles et intermédiaires et d’une augmentation de la densité des cellules basales [2]. Une augmentation du nombre des cellules dendritiques est également observée au niveau de l’épithélium basal, au centre et en périphérie de la cornée (fig. 2-19c) [2, 3]. Au niveau des plexus nerveux sous-épithéliaux, on constate le plus souvent une diminution de la densité des nerfs associée à une augmentation de la tortuosité, bien que ces résultats soient encore controversés (fig. 2-19d) [28]. Des kératocytes hyperréflectifs dits « activés » ont également été observés dans la sécheresse oculaire [2].
Au niveau conjonctival, une métaplasie squameuse avec une augmentation de la taille des cellules épithéliales et une diminution du rapport nucléocytoplasmique a été observée en IVCM dans le syndrome de Gougerot-Sjögren [2]. L’infiltration de cellules inflammatoires a pu aussi être quantifiée (fig. 2-19e) [3]. Des modifications de la densité des cellules à mucus pourraient être observées en IVCM, mais ces résultats restent encore largement discutés [2]. Enfin, certains détails intracellulaires peuvent aussi être observés comme un enroulement de la chromatine des noyaux des cellules conjonctivales (aspect snake-like chromatin) (fig. 2-19f). Celui-ci résulterait d’un effet mécanique de frottement de la paupière sur une conjonctive desséchée ou hyperlaxe. Cet aspect est également retrouvé en cas de kératoconjonctivite limbique supérieure.
Les glandes de Meibomius ont également été étudiées en IVCM. Le diamètre des acini, leur densité, l’aspect des orifices, l’infiltration de cellules inflammatoires périglandulaires ou encore la réflectivité des sécrétions ont été analysés de manière quantitative et semi-quantitative [2, 29]. Le diagnostic de dysfonctionnement des glandes de Meibomius (DGM) et l’évolution sous traitement pourraient être aussi évalués [2]. L’IVCM pourrait ainsi différencier l’atteinte des glandes de Meibomius dans diverses pathologies comme la sécheresse oculaire, la réaction du greffon contre l’hôte, le port de lentilles de contact ou encore le vieillissement [2].

Fig. 2-19 Images de microscopie confocale in vivo (HRT-RCM®) de la surface oculaire dans la sécheresse oculaire (400 µm × 400 µm).
a. Cellules épithéliales superficielles hyperréflectives et activées. b. Cellules épithéliales basales activées. c. Infiltration de cellules de type dendritique au sein de la cornée. d. Modifications des plexus nerveux sous-épithéliaux avec une diminution de la densité et une augmentation de la tortuosité des nerfs. e. Infiltrations de cellules dendritiques au sein de l’épithélium conjonctival. f. Aspect de snake-like chromatine au niveau de la cornée.
L’IVCM a été largement utilisée pour l’analyse préopératoire ou pour évaluer les changements tissulaires cornéens impliqués dans les greffes transfixiantes ou lamellaires de la cornée, les greffes de membrane amniotique ou encore le crosslinking [1]. Après une greffe transfixiante de la cornée, une diminution significative des densités épithéliales, kératocytaires, nerveuses et endothéliales a été démontrée en IVCM [30]. Cette technique d’imagerie serait également une aide pour identifier un rejet de greffe dans lequel on va retrouver une accumulation focale de cellules dendritiques hyperréflectives au niveau de l’épithélium basal et de la couche de Bowman associée à des anomalies des kératocytes (fig. 2-20a) [31]. Certains diagnostics différentiels de cette complication comme une infection, une invasion épithéliale ou une décompensation endothéliale peuvent aussi être diagnostiqués en IVCM [20, 31]. Les techniques de greffes lamellaires ont bénéficié tout particulièrement de la microscopie confocale qui permet d’évaluer l’interface entre la cornée réceptrice et le greffon, de comparer différentes techniques chirurgicales ou encore d’évaluer les changements tissulaires cornéens après Descemet stripping endothelial keratoplasty (DSEK) ou Descemet stripping with automated endothelial keratoplasty (DSAEK) [2]. L’observation des membranes amniotiques transplantées, de leur résorption et de la cornée sous-jacente est également possible [32]. Enfin, cette technique offre une visualisation directe des effets de la photopolymérisation sur les tissus cornéens et des complications éventuelles du crosslinking [33].

Fig. 2-20 Images de microscopie confocale in vivo (HRT-RCM®) après chirurgie cornéenne et chirurgie réfractive (400 µm × 400 µm).
a. Importante infiltration de cellules dendritiques en périphérie de la cornée lors d’un rejet de greffe de cornée. b. Activation des kératocytes après PKR. c. Aspect de nerfs cornéens anormaux plusieurs mois après un Lasik. d. Particules hyperréflectives au niveau de l’interface d’un capot de Lasik. e. Limite d’un capot de Lasik après découpe au laser femtoseconde.
La chirurgie réfractive cornéenne est l’un des domaines ou l’IVCM a été très largement utilisée pour : caractériser in vivo les modifications cellulaires associées à la cicatrisation ; comparer différentes techniques chirurgicales ; aider dans la prise en charge de certaines complications [34, 35]. L’épithélium, le stroma cornéen et l’interface, les kératocytes et les nerfs cornéens peuvent être analysés de manière non invasive et suivis lors de la cicatrisation après chirurgie réfractive [2, 34, 35]. Après photokératectomie réfractive (PKR), le nombre, la localisation et l’apparence des kératocytes peuvent être analysés précisément. Certaines complications ont été analysées en IVCM et il a ainsi été montré que le haze visible cliniquement correspondait à une activation des kératocytes (fig. 2-20b) [2, 35]. De nombreuses études sur le laser in situ keratomileusis (Lasik) ont aussi été réalisées en IVCM, en particulier sur les nerfs cornéens et leur repousse après chirurgie [34, 35]. La microscopie confocale a ainsi révélé une diminution postopératoire de la densité des plexus nerveux sous-épithéliaux [2, 35]. La régénération postopératoire des nerfs cornéens apparaît aussi incomplète et anormale même plusieurs années après le Lasik (fig. 2-20c). D’autres applications ont été proposées comme l’analyse de l’interface qui montre des particules hyperréflectives de dimensions variables et dont la nature reste encore indéterminée (fig. 2-20d) [34, 35]. Les complications de la chirurgie réfractive ont aussi été évaluées en IVCM. En cas d’infiltrat cornéen, il serait possible de différencier une kératite lamellaire diffuse, avec une infiltration de cellules inflammatoires au niveau de l’interface, d’une kératite infectieuse [2, 34, 35]. Enfin, l’IVCM est aussi intéressante pour caractériser et comparer la réponse cicatricielle et les modifications tissulaires cornéennes induites lors de l’utilisation de nouveaux matériels ou techniques employés en chirurgie réfractive (fig. 2-20e) [36].
Au-delà de l’analyse des kératites infectieuses qui peuvent être de sévères complications du port de lentilles de contact, l’IVCM a permis une meilleure compréhension des changements tissulaires impliqués dans l’utilisation des lentilles. On retrouve ainsi une augmentation de la taille des cellules épithéliales chez tous les porteurs de lentilles quel que soit le type de lentille, et aussi une augmentation de la densité des cellules dendritiques au niveau des plexus nerveux sous-épithéliaux [2, 37]. D’autres modifications notamment au niveau du stroma comme des variations de la densité des kératocytes, la présence de microdots ou des anomalies endothéliales font débat [2, 37].
Dans le glaucome, l’IVCM a permis de mieux comprendre les mécanismes liés à la filtration après chirurgie filtrante, mais aussi d’évaluer les effets des traitements collyres au niveau de la surface oculaire. Le développement d’une chirurgie du glaucome efficace à long terme dépend en grande partie du développement d’une bulle de filtration conjonctivale fonctionnelle. Le développement de cette bulle de filtration lié aux processus de cicatrisation conjonctivale peut ainsi être analysé en IVCM. La présence des microkystes épithéliaux, la densité du tissu conjonctif, l’aspect des vaisseaux sanguins et des cellules inflammatoires conjonctivales au niveau des tissus de la bulle de filtration ont été observés en IVCM [38]. Les bulles de filtration fonctionnelles ont de nombreux microkystes associés à un tissu conjonctival lâche (fig. 2-21a et b). Les bulles non fonctionnelles ont peu de microkystes et un tissu conjonctif dense et de nombreux vaisseaux sanguins tortueux (fig. 2-21c et d) [38]. L’infiltration des bulles par des cellules inflammatoires peut aussi être analysée et suivie dans le temps [39].
L’utilisation chronique de collyres antiglaucomateux et de leurs conservateurs est responsable de changements tissulaires au niveau de la surface oculaire. Ces changements ont été observés au niveau de la cornée, avec une diminution de la densité des cellules épithéliales superficielles, une activation des kératocytes du stroma, une diminution de la densité et une augmentation de la tortuosité des nerfs cornéens [5, 40], mais aussi au niveau conjonctival [41]. Cette technique est par ailleurs utile sur les modèles expérimentaux animaux pour évaluer et comparer différentes formulations de collyres et de conservateurs [42].

Fig. 2-21 Images de microscopie confocale in vivo (HRT-RCM®) après chirurgie filtrante du glaucome (400 µm × 400 µm).
a, b. Bulle de filtration fonctionnelle, nombreux microkystes intra-épithéliaux (a) et tissu sous-conjonctival lâche (b). c, d. Bulle de filtration non fonctionnelle, absence de microkystes (c) et tissu sous-conjonctival dense et fibrosé (d).
Les modifications cornéennes associées à certaines maladies systémiques ou oculaires ont aussi été évaluées en IVCM comme dans le diabète, en particulier à la recherche d’atteintes nerveuses, le syndrome de Marfan, le kératocône, les conjonctivites et kératoconjonctivites allergiques, les kératites neurotrophiques, les brûlures cornéennes [1, 2]. Dans le ptérygion, l’analyse en IVCM a révélé le rôle des cellules dendritiques dans sa physiopathogénie [29]. Bien que ne remplaçant pas l’histologie, l’IVCM pourrait également être une aide dans l’analyse des tumeurs pigmentées et non pigmentées de la conjonctive (fig. 2-22a) [43], du limbe mais aussi pour les néoplasies intra-épithéliales (fig. 2-22b) [44, 45].

Fig. 2-22 Images de microscopie confocale in vivo (HRT-RCM®, 400 µm × 400 µm).
a. Image d’un nævus conjonctival avec mycrokystes et dépôts pigmentés hyperréflectifs. b. Cellules épithéliales anormales au sein de l’épithélium cornéen dans une néoplasie intra-épithéliale.
Une des principales limites de la microscopie confocale est le faible champ de vision offert par les appareils actuellement commercialisés (approximativement 0,16 mm2) [46]. Des systèmes de reconstruction automatisés en deux dimensions sont à l’étude, notamment pour l’analyse des nerfs cornéens et afin de faciliter l’analyse de surfaces tissulaires de plus grande taille (fig. 2-23) [47]. La microscopie confocale permet d’obtenir des coupes des tissus analysés et ainsi de comparer les résultats avec l’histologie classique. Grâce à des logiciels de reconstruction d’images, il sera certainement possible de reconstituer facilement les images en trois dimensions dans un futur proche [46].
L’IVCM pour être véritablement utile doit être réalisée mais aussi interprétée par un opérateur expérimenté. Afin d’améliorer l’analyse des images et diminuer sa subjectivité, des systèmes d’analyse automatisée des images sont en cours de développement, notamment pour l’analyse des nerfs cornéens [2, 5]. Enfin, la résolution actuelle (de l’ordre de quelques microns) et l’absence de coloration utilisable in vivo chez l’homme, limite l’exploration en IVCM à une analyse morphologique en niveau de gris. L’amélioration de la résolution, le développement d’objectifs non-contacts et l’utilisation de colorants permettra certainement d’augmenter la sensibilité de cette imagerie qui est déjà un outil important pour l’analyse de la surface oculaire et de ses nombreuses pathologies.

Fig. 2-23 Reconstruction en deux dimensions à partir d’images (5) en microscopie confocale in vivo (HRT-RCM®, 400 µm × 400 µm) montrant la disposition des plexus nerveux sous-épithéliaux au centre de la cornée.
La tomographie par cohérence optique ou ocular coherence tomography (OCT) est une technique d’imagerie non-contact, qui utilise un principe d’interférométrie à basse cohérence pour offrir in vivo des coupes des structures tissulaires. Cette technique mesure le délai et l’intensité de la lumière (d’une longueur d’onde de 830 à 1325 nm) réfléchie sur la structure analysée en la comparant à une lumière réfléchie sur un miroir de référence, la combinaison de ces deux signaux produisant un phénomène dit d’interférence. L’intensité du signal dépend des propriétés optiques des tissus et, à partir de cet enregistrement, l’appareil reconstruit une coupe sagittale de la structure analysée. Le principe de fonctionnement de l’OCT est en réalité similaire à celui de l’échographie mais avec l’émission d’une onde lumineuse au lieu d’un ultrason [1]. La vitesse de la lumière étant un million de fois plus élevée que celles des ultrasons, ce type d’imagerie permet d’atteindre des niveaux de résolution longitudinale de l’ordre de quelques microns [1, 48].
Commercialisé pour la première fois au milieu des années 1990, l’OCT est encore aujourd’hui principalement utilisé en ophtalmologie pour l’imagerie du segment postérieur de l’œil. L’OCT est ainsi devenu un examen de routine indispensable pour le diagnostic et le suivi des maladies rétiniennes ou dans le glaucome, et de très nombreuses pathologies ont ainsi bénéficié de l’apport de cette technique. Les premières images du segment antérieur en tomographie à cohérence optique ont été réalisées en 1994 à l’aide d’un OCT time-domain (TD-OCT) ayant une longueur d’onde de 820 nm et destiné à l’étude du segment postérieur [49]. En réalité, ce n’est qu’à partir des années 2000 qu’est apparu un OCT utilisant une longueur d’onde de 1310 nm permettant une visualisation optimale du segment antérieur [50]. Depuis, de nouveaux OCT dits spectral-domain (SD-OCT), plus rapides et offrant une meilleure résolution, ont été développés ; avec des modules adaptés, ils permettent l’analyse de la cornée et de l’ensemble de la surface oculaire avec des résolutions approchant 5 µm (fig. 2-24) [48]. Grâce à cette technologie, il est également possible d’acquérir des volumes en trois dimensions et de reconstruire des images parallèles à la surface de la cornée dites « en face » ou « C-scans » (fig. 2-25) [51]. Enfin, des prototypes d’appareils utilisant une technique d’ultra-high resolution (UHR-OCT) ont été développés ; dans un avenir proche, ils permettront d’obtenir en pratique clinique de meilleures résolutions [51].

Fig. 2-24 Images d’une cornée normale en SD-OCT (RTVue®, Optovue Inc., Fremont, États-Unis).
a. Image en fenêtre large, jusqu’à 8 mm × 8 mm (CAM L pour corneal adaptor module long). b. Image en petite fenêtre, jusqu’à 3 mm × 3 mm, offrant une meilleure résolution (CAM S pour corneal adaptor module short). Toutes les couches de la cornée, depuis le film lacrymal jusqu’à l’endothélium, sont visualisées.

Fig. 2-25 Images en SD-OCT (RTVue®) dans une dystrophie de Cogan.
a. Membrane basale anormale s’insinuant au sein de l’épithélium. b. Reconstruction d’une image dite « en face » parallèle au tissu analysé.
L’analyse biométrique du segment antérieur et de la surface oculaire a largement bénéficié de cette technique d’imagerie objective et totalement non invasive. Les nouveaux appareils d’OCT de segment antérieur (SD-OCT et UHR-OCT) sont capables de mesurer l’épaisseur de l’ensemble de la cornée et de chaque couche séparément, depuis l’épithélium jusqu’à l’endothélium. La pachymétrie mesurée en OCT est fiable, reproductible et corrélée à la pachymétrie ultrasonore [52]. La profondeur exacte de dépôts ou d’anomalies tissulaires cornéennes peut ainsi être déterminée avec précision (fig. 2-26a) [48]. Ces mesures quantitatives sont aussi obtenues au niveau du limbe et de la conjonctive (fig. 2-26b) [53] et apportent des informations utiles à la compréhension de pathologies de la surface oculaire comme la sécheresse oculaire ou la toxicité des traitements du glaucome.

Fig. 2-26 Images de la cornée en SD-OCT à haute résolution.
a. Image d’une cicatrice cornéenne en SD-OCT (RTVue®). Hyperréflectivité stromale antérieure suite à un abcès de cornée bactérien. L’OCT permet de réaliser des mesures quantitatives de la profondeur de la cicatrice. b. Évaluation de l’épithélium conjonctival, limbique et cornéen en SD-OCT (Spectralis OCT®, Heidelberg Engineering GmbH, Heidelberg, Allemagne).
Bien que les protocoles d’analyse ne soient pas encore standardisés et que l’analyse de la réflectivité ne soit que qualitative, l’imagerie en OCT s’est rapidement imposée comme un outil utile pour la prise en charge des patients nécessitant une greffe de la cornée ou ayant déjà bénéficié de ce traitement. En préopératoire, l’évaluation précise du type et de la profondeur des anomalies tissulaires cornéennes aide à déterminer le type de procédure à proposer au patient (fig. 2-27) [48]. Dans les greffes transfixiantes, outre la mesure de la pachymétrie au niveau de l’ensemble du greffon, l’OCT permet d’analyser l’architecture de l’interface entre la cornée réceptrice et le greffon, la profondeur des sutures ou encore de suivre la progression de la cicatrisation (fig. 2-28) [48]. En révélant l’anatomie du segment antérieur, même au travers d’un œdème de cornée, cette technique d’imagerie facilite le diagnostic de certaines complications comme l’existence de synéchies entre l’iris et le greffon qui peuvent être responsables d’hypertonies oculaires et de glaucomes secondaires [48, 54].
L’évolution des techniques chirurgicales, avec le développement des greffes lamellaires postérieures et des greffes endothéliales, a fait apparaître de nouvelles indications pour l’OCT. Dans les kératoplasties lamellaires, l’OCT permet d’évaluer précisément l’épaisseur des différentes couches cornéennes, notamment stromales résiduelles, de vérifier la bonne apposition des tissus et de comparer différentes techniques chirurgicales (fig. 2-29) [48, 55]. Dans les greffes endothéliales, il est possible de mesurer objectivement et sur toute sa surface le greffon endothélial ou l’épaisseur de la cornée réceptrice (fig. 2-30) [56]. Certaines complications comme un détachement de la membrane de Descemet (fig. 2-31), un rejet de greffe, la présence de synéchies antérieures périphériques ou un blocage pupillaire pourront aussi être recherchées en OCT [55]. Enfin, chez les patients ayant bénéficié d’une kératoprothèse, l’OCT permet d’analyser de manière non invasive les différentes surfaces en contact avec les tissus oculaires et constitue une aide lors du suivi [48].

Fig. 2-27 Image de la cornée en SD-OCT (Spectralis OCT®) dans une dystrophie cornéenne de Reis-Bücklers.
Le matériel anormal apparaît sous la forme de dépôts hyperréflectifs prédominant au niveau de la membrane de Bowman.

Fig. 2-28 Image de la cornée en OCT de segment antérieur (OCT Visante®, Carl Zeiss Meditec, Dublin, États-Unis) dans un rejet de greffe de cornée après une kératoplastie transfixiante.

Fig. 2-29 Images de la cornée après kératoplastie lamellaire antérieure.
a. Image de l’ensemble du greffon en OCT de segment antérieur (OCT Visante®). b. Image de la cornée centrale du même patient en SD-OCT (RTVue®).

Fig. 2-30 Images d’une greffe endothéliale en SD-OCT (RTVue®) (a). Des mesures quantitatives sont possibles (b).

Fig. 2-31 Image d’un décollement descemétique après greffe endothéliale en SD-OCT (RTVue®).
L’OCT donne de nombreuses informations utiles pour la prise en charge des patients opérés ou souhaitant être opérés de chirurgie réfractive. En préopératoire, les OCT de haute résolution permettent une mesure précise et non invasive de l’épaisseur cornéenne, de la profondeur du capot d’un précédent Lasik ou encore de la localisation et du volume d’une cicatrice intrastromale [48]. L’OCT offre également une cartographie de la pachymétrie sur une large zone cornéenne permettant ainsi d’évaluer la profondeur d’ablation stromale. Après Lasik, une mesure de la profondeur du volet cornéen et de l’épaisseur du stroma résiduel est possible sur la totalité de la zone de découpe (fig. 2-32) [57]. Cet examen a ainsi permis de comparer différentes techniques chirurgicales comme l’utilisation d’un microkératome mécanique ou la photodisruption cornéenne au laser femtoseconde [58]. Les découpes intrastromales et les phénomènes de cicatrisation physiologique ou pathologique du volet peuvent être analysés en OCT [48]. Les zones de jonction périphériques sont également visualisées avec une analyse possible de l’angulation stromale des bords du capot ou encore de la repousse épithéliale à la jonction. Les complications de la chirurgie réfractive sont aussi analysées en OCT de haute résolution afin d’identifier les phénomènes entraînant un remodelage tissulaire anormal pouvant conduire à une véritable ectasie.

Fig. 2-32 Image de la cornée en SD-OCT (Spectralis OCT®) d’un capot de Lasik.
L’interface correspond à une ligne discrètement hyperréflective.
(Source : image Dr E. Landman.)
Lors des greffes de membranes amniotiques, on peut utiliser l’OCT pour analyser l’intégration progressive de la membrane amniotique dans la cornée, la cicatrisation stromale et épithéliale et le maintien de l’architecture de la chambre antérieure lorsque la membrane recouvre un ulcère très profond ou une perforation de cornée [32]. La ligne de démarcation stromale après crosslinking est aussi visualisée en OCT [59]. Enfin, l’OCT permet d’analyser les dispositifs intracornéens, anneaux ou lenticules (fig. 2-33). On peut ainsi en déterminer la position, quantifier les réactions stromales de voisinage et suivre les variations de courbure cornéenne relatives aux réorganisations architecturales secondaires [48].
L’imagerie par OCT a aussi été utilisée pour analyser et quantifier le film lacrymal et le ménisque des larmes (fig. 2-34a) ou encore visualiser un conjonctivochalasis (fig. 2-34b). Cette technique a par ailleurs permis d’évaluer l’efficacité de traitements contre la sécheresse oculaire comme l’occlusion des points lacrymaux [60]. Lors de l’examen des patients porteurs de lentilles de contact, l’OCT peut renseigner sur l’état d’hydratation de la cornée et aider à l’adaptation des lentilles sur la surface cornéenne et limbique (fig. 2-35) [61].
Des études récentes ont également montré que l’OCT pourrait apporter des informations utiles concernant l’extension des infections et la réponse au traitement même si la résolution actuelle de cette imagerie ne permet pas d’identifier directement l’agent infectieux responsable. L’épaisseur cornéenne augmente ainsi au stade initial de l’infection et diminue avec la résolution de l’infection [62]. La profondeur de l’infiltrat et sa taille peuvent être mesurées, quantifiées précisément et suivies dans le temps.
Enfin, on peut, grâce à l’OCT, différencier les tumeurs kystiques des lésions solides de la surface oculaire, évaluer la pénétration des lésions sein du tissu ou encore évaluer l’efficacité du traitement (fig. 2-36) [63]. Les images obtenues en UHR-OCT seraient bien corrélées aux résultats histologiques [63].

Fig. 2-34 Applications de l’OCT pour l’exploration du ménisque lacrymal.
a. Image du ménisque lacrymal en OCT de segment antérieur (OCT Visante®). b. Image d’un conjonctivochalasis en SD-OCT (RTVue®).

Fig. 2-35 Image d’une lentille de contact rigide et de l’épithélium cornéen dans un cas de kératocône en SD-OCT (RTVue®).

Fig. 2-36 Images en SD-OCT (Spectralis OCT®) d’un carcinome in situ (a) et d’un ptérygion (b).
(Source : images Dr QF. Liang.)
L’analyse en AS-OCT n’atteint pas encore la résolution quasi histologique de l’IVCM. Les développements de nouveaux systèmes, basés sur d’autres longueurs d’ondes et sur une meilleure transduction du signal et de son analyse, vont certainement améliorer dans le futur la résolution spatiale tout comme l’analyse de structures plus profondes ou plus opaques. Simple d’utilisation, l’OCT nécessite néanmoins une certaine expérience pour obtenir des images de bonne qualité et des mesures quantitatives fiables.
L’IVCM et l’OCT sont des techniques d’imagerie non invasives qui offrent des images de haute résolution de la cornée et pour lesquelles de nombreuses applications cliniques ont été développées. Malgré certaines limites, ces deux techniques d’imagerie offrent déjà des données qualitatives et quantitatives de l’ensemble de la surface oculaire, des paupières et du film lacrymal jusqu’au couches les plus profondes de la cornée. Les futures générations de ces appareils d’imageries, avec une meilleure résolution, une meilleure pénétration tissulaire, une plus grande rapidité et simplicité d’acquisition des images, permettront de multiplier les applications de ces techniques en pratique clinique courante.
[1] Labbé A, Kallel S, Denoyer A, et al. Imagerie de la cornée. Encycl Méd Chir (Elsevier, Paris). Ophtalmologie. 2012 : p. 1-9.
[2] Villani E, Baudouin C, Efron N, et al. In vivo confocal microscopy of the ocular surface : from bench to bedside. Curr Eye Res 2014 ; 39 : 213-31.
[3] Zhivov A, Stachs O, Kraak R, et al. In vivo confocal microscopy of the ocular surface. Ocul Surf 2006 ; 4 : 81-93.
[4] Patel DV, McGhee CN. In vivo confocal microscopy of human corneal nerves in health, in ocular and systemic disease, and following corneal surgery : a review. Br J Ophthalmol 2009 ; 93 : 853-60.
[5] Labbé A, Alalwani H, Van Went C, et al. The relationship between subbasal nerve morphology and corneal sensation in ocular surface disease. Invest Ophthalmol Vis Sci 2012 ; 53 : 4926-31.
[6] Efron N, Al-Dossari M, Pritchard N. In vivo confocal microscopy of the bulbar conjunctiva. Clin Experiment Ophthalmol 2009 ; 37 : 335-44.
[7] Efron N, Al-Dossari M, Pritchard N. In vivo confocal microscopy of the palpebral conjunctiva and tarsal plate. Optom Vis Sci 2009 ; 86 : 1303-8.
[8] Villani E, Ceresara G, Beretta S, et al. In vivo confocal microscopy of meibomian glands in contact lens wearers. Invest Ophthalmol Vis Sci 2011 ; 52 : 5215-9.
[9] Labbé A, Khammari C, Dupas B, et al. Contribution of in vivo confocal microscopy to the diagnosis and management of infectious keratitis. Ocul Surf 2009 ; 7 : 41-52.
[10] Vaddavalli PK, Garg P, Sharma S, et al. Role of confocal microscopy in the diagnosis of fungal and acanthamœba keratitis. Ophthalmology 2011 ; 118 : 29-35.
[11] Kumar RL, Cruzat A, Hamrah P. Current state of in vivo confocal microscopy in management of microbial keratitis. Semin Ophthalmol 2010 ; 25 : 166-70.
[12] Brasnu E, Bourcier T, Dupas B, et al. In vivo confocal microscopy in fungal keratitis. Br J Ophthalmol 2007 ; 91 : 588-91.
[13] Kanavi MR, Javadi M, Yazdani S, Mirdehghanm S. Sensitivity and specificity of confocal scan in the diagnosis of infectious keratitis. Cornea 2007 ; 26 : 782-6.
[14] Shi W, Li S, Liu M, et al. Antifungal chemotherapy for fungal keratitis guided by in vivo confocal microscopy. Graefes Arch Clin Exp Ophthalmol 2008 ; 246 : 581-6.
[15] Gabison EE, Alfonsi N, Doan S, et al. Archipelago keratitis : a clinical variant of recurrent herpetic keratitis ? Ophthalmology 2007 ; 114 : 2000-5.
[16] Dosso AA, Rungger-Brandle E. Clinical course of epidemic keratoconjunctivitis : evaluation by in vivo confocal microscopy. Cornea 2008 ; 27 : 263-8.
[17] Weiss JS, Moller HU, Lisch W, et al. The IC3D classification of the corneal dystrophies. Cornea 2008 ; 27 : S1-83.
[18] Lisch W, Wasielica-Poslednik J, Lisch C, et al. Contact lens-induced regression of Lisch epithelial corneal dystrophy. Cornea 2010 ; 29 : 342-5.
[19] Labbé A, Nicola RD, Dupas B, et al. Epithelial basement membrane dystrophy : evaluation with the HRT II Rostock Cornea Module. Ophthalmology 2006 ; 113 : 1301-8.
[20] Traversi C, Martone G, Malandrini A, et al. In vivo confocal microscopy in recurrent granular dystrophy in corneal graft after penetrating keratoplasty. Clin Experiment Ophthalmol 2006 ; 34 : 808-10.
[21] Kobayashi A, Fujiki K, Fujimaki T, et al. In vivo laser confocal microscopic findings of corneal stromal dystrophies. Arch Ophthalmol 2007 ; 125 : 1168-73.
[22] Ciancaglini M, Carpineto P, Doronzo E, et al. Morphological evaluation of Schnyder’s central crystalline dystrophy by confocal microscopy before and after phototherapeutic keratectomy. J Cataract Refract Surg 2001 ; 27 : 1892-5.
[23] Kobayashi A, Fujiki K, Murakami A, Sugiyama K. In vivo laser confocal microscopy findings and mutational analysis for Schnyder’s crystalline corneal dystrophy. Ophthalmology 2009 ; 116 : 1029-36.
[24] Dosso A, Rungger-Brandle E. In vivo confocal microscopy in hydroxychloroquine-induced keratopathy. Graefes Arch Clin Exp Ophthalmol 2007 ; 245 : 318-20.
[25] Labbé A, Niaudet P, Loirat C, et al. In vivo confocal microscopy and anterior segment optical coherence tomography analysis of the cornea in nephropathic cystinosis. Ophthalmology 2009 ; 116 : 870-6.
[26] Mastropasqua L, Nubile M, Lanzini M, et al. Corneal and conjunctival manifestations in Fabry disease : in vivo confocal microscopy study. Am J Ophthalmol 2006 ; 141 : 709-18.
[27] Patel DV, McGhee CN. Contemporary in vivo confocal microscopy of the living human cornea using white light and laser scanning techniques : a major review. Clin Experiment Ophthalmol 2007 ; 35 : 71-88.
[28] Labbé A, Liang Q, Wang Z, et al. Corneal nerve structure and function in patients with non-sjogren dry eye : clinical correlations. Invest Ophthalmol Vis Sci 2013 ; 54 : 5144-50.
[29] Wang Y, Le Q, Xu J. Application of in vivo laser scanning confocal microscopy for evaluation of ocular surface diseases : lessons learned from pterygium, meibomian gland disease, and chemical burns. Cornea 2012 ; 31 : 968.
[30] Niederer RL, Perumal D, Sherwin T, McGhee CN. Corneal innervation and cellular changes after corneal transplantation: an in vivo confocal microscopy study. Invest Ophthalmol Vis Sci 2007 ; 48 : 621-6.
[31] Niederer RL, Sherwin T, McGhee CN. In vivo confocal microscopy of subepithelial infiltrates in human corneal transplant rejection. Cornea 2007 ; 26 : 501-4.
[32] Nubile M, Dua HS, Lanzini M, et al. In vivo analysis of stromal integration of multilayer amniotic membrane transplantation in corneal ulcers. Am J Ophthalmol 2011 ; 151 : 809-22.
[33] Guthoff RF, Zhivov A, Stachs O. In vivo confocal microscopy, an inner vision of the cornea - a major review. Clin Experiment Ophthalmol 2009 ; 37 : 100-17.
[34] Dhaliwal JS, Kaufman SC, Chiou AG. Current applications of clinical confocal microscopy. Curr Opin Ophthalmol 2007 ; 18 : 300-7.
[35] Kaufman SC, Kaufman HE. How has confocal microscopy helped us in refractive surgery ? Curr Opin Ophthalmol 2006 ; 17 : 380-8.
[36] Sonigo B, Iordanidou V, Chong-Sit D, et al. In vivo corneal confocal microscopy comparison of intralase femtosecond laser and mechanical microkeratome for laser in situ keratomileusis. Invest Ophthalmol Vis Sci 2006 ; 47 : 2803-11.
[37] Efron N. Contact lens-induced changes in the anterior eye as observed in vivo with the confocal microscope. Prog Retin Eye Res 2007 ; 26 : 398-436.
[38] Labbé A, Dupas B, Hamard P, Baudouin C. In vivo confocal microscopy study of blebs after filtering surgery. Ophthalmology 2005 ; 112 : 1979-86.
[39] Messmer EM, Zapp DM, Mackert MJ, et al. In vivo confocal microscopy of filtering blebs after trabeculectomy. Arch Ophthalmol 2006 ; 124 : 1095-103.
[40] Martone G, Frezzotti P, Tosi GM, et al. An in vivo confocal microscopy analysis of effects of topical antiglaucoma therapy with preservative on corneal innervation and morphology. Am J Ophthalmol 2009 ; 147 : 725-35.
[41] Frezzotti P, Fogagnolo P, Haka G, et al. In vivo confocal microscopy of conjunctiva in preservative-free timolol 0.1 % gel formulation therapy for glaucoma. Acta Ophthalmol 2014 ; 92 : e133-40.
[42] Liang H, Baudouin C, Labbé A, et al. Conjunctiva-associated lymphoid tissue (CALT) reactions to antiglaucoma prostaglandins with or without BAK-preservative in rabbit acute toxicity study. PLoS One 2012 ; 7 : e33913.
[43] Messmer EM, Mackert MJ, Zapp DM, Kampik A. In vivo confocal microscopy of pigmented conjunctival tumors. Graefes Arch Clin Exp Ophthalmol 2006 ; 244 : 1437-45.
[44] Gabison EE, Labbé A, Brignole-Baudouin F, et al. Confocal biomicroscopy of corneal intraepithelial neoplasia regression following interferon alpha 2b treatment. Br J Ophthalmol 2010 ; 94 : 134-5.
[45] Xu Y, Zhou Z, Xu Y, et al. The clinical value of in vivo confocal microscopy for diagnosis of ocular surface squamous neoplasia. Eye (Lond) 2012 ; 26 : 781-7.
[46] Zhivov A, Stachs O, Stave J, Guthoff RF. In vivo three-dimensional confocal laser scanning microscopy of corneal surface and epithelium. Br J Ophthalmol 2009 ; 93 : 667-72.
[47] Edwards K, Pritchard N, Gosschalk K, et al. Wide-field assessment of the human corneal subbasal nerve plexus in diabetic neuropathy using a novel mapping technique. Cornea 2012 ; 31 : 1078-82.
[48] Sayegh RR, Pineda R 2nd. Practical applications of anterior segment optical coherence tomography imaging following corneal surgery. Semin Ophthalmol 2012 ; 27 : 125-32.
[49] Izatt JA, Hee MR, Swanson EA, et al. Micrometer-scale resolution imaging of the anterior eye in vivo with optical coherence tomography. Arch Ophthalmol 1994 ; 112 : 1584-9.
[50] Radhakrishnan S, Rollins AM, Roth JE, et al. Real-time optical coherence tomography of the anterior segment at 1310 nm. Arch Ophthalmol 2001 ; 119 : 1179-85.
[51] Adhi M, Duker JS. Optical coherence tomography--current and future applications. Curr Opin Ophthalmol 2013 ; 24 : 213-21.
[52] Huang J, Ding X, Savini G, et al. A Comparison between Scheimpflug imaging and optical coherence tomography in measuring corneal thickness. Ophthalmology 2013 ; 120 : 1951-8.
[53] Francoz M, Karamoko I, Baudouin C, Labbé A. Ocular surface epithelial thickness evaluation with spectral-domain optical coherence tomography. Invest Ophthalmol Vis Sci 2011 ; 52 : 9116-23.
[54] Dada T, Shah BM, Bali SJ, et al. Anterior segment OCT imaging in opaque grafts with secondary glaucoma following tectonic penetrating keratoplasty for perforated corneal ulcers. Eye (Lond) 2011 ; 25 : 1522-4.
[55] Lim LS, Aung HT, Aung T, Tan DT. Corneal imaging with anterior segment optical coherence tomography for lamellar keratoplasty procedures. Am J Ophthalmol 2008 ; 145 : 81-90.
[56] Yeh RY, Quilendrino R, Musa FU, et al. Predictive value of optical coherence tomography in graft attachment after Descemet’s membrane endothelial keratoplasty. Ophthalmology 2013 ; 120 : 240-5.
[57] Kim JH, Lee D, Rhee KI. Flap thickness reproducibility in laser in situ keratomileusis with a femtosecond laser: optical coherence tomography measurement. J Cataract Refract Surg 2008 ; 34 : 132-6.
[58] von Jagow B, Kohnen T. Corneal architecture of femtosecond laser and microkeratome flaps imaged by anterior segment optical coherence tomography. J Cataract Refract Surg 2009 ; 35 : 35-41.
[59] Doors M, Tahzib NG, Eggink FA, et al. Use of anterior segment optical coherence tomography to study corneal changes after collagen cross-linking. Am J Ophthalmol 2009 ; 148 : 844-51.
[60] Chen F, Shen M, Chen W, et al. Tear meniscus volume in dry eye after punctal occlusion. Invest Ophthalmol Vis Sci 2010 ; 51 : 1965-9.
[61] Tao A, Shao Y, Jiang H, et al. Entire thickness profiles of the epithelium and contact lens in vivo imaged with high-speed and high-resolution optical coherence tomography. Eye Contact Lens 2013 ; 39 : 329-34.
[62] Mantopoulos D, Cruzat A, Hamrah P. In vivo imaging of corneal inflammation : new tools for clinical practice and research. Semin Ophthalmol 2010 ; 25 : 178-85.
[63] Shousha MA, Karp CL, Canto AP, et al. Diagnosis of ocular surface lesions using ultra-high-resolution optical coherence tomography. Ophthalmology 2013 ; 120 : 883-91.
P.-J. Pisella
Le film lacrymal représente la première interface de l’œil d’un point de vue anatomique mais également optique. Toute instabilité du film lacrymal secondaire à son altération par atteinte d’une ou de plusieurs de ses composantes aura un retentissement visuel variable mais systématique. Celui-ci est particulièrement remarqué chez les patients opérés de chirurgie réfractive cornéenne ou même après chirurgie de la cataracte. L’exploration de ce retentissement visuel peut être faite à l’aide d’aberromètres évaluant la qualité de vision selon des protocoles de mesures continues afin d’en apprécier la fluctuation en rapport avec l’instabilité du film lacrymal.
Le film lacrymal constitue la première interface entre l’œil et le milieu extérieur chez l’homme et la majorité des espèces animales. En effet, la cornée, organe essentiel de la vision, est la muqueuse la plus exposée de l’organisme au milieu extérieur avec un temps d’ouverture moyen de la fente palpébrale d’environ 92 % du temps et un clignement moyen de 15 fois par minute. D’un point de vue optique, il représente ainsi la première zone de transition entre deux milieux d’indices de réfraction différents et possède donc un pouvoir réfractif ; celui-ci est donné par la formule :
D = n′ – n/r
où D est le pouvoir réfractif de la surface de transition en dioptries ;
n et n′, les indices de réfraction des milieux avant et après la surface de transition ;
et r le rayon de la surface de transition en mètres (m).
Naturellement, le pouvoir réfractif du film lacrymal est très dépendant de la stabilité de celui-ci et peut donc subir de profondes modifications en fonction de la qualité de celle-ci pouvant entraîner des perturbations visuelles non négligeables en pathologie.
Ainsi, la variation d’épaisseur du film lacrymal, physiologique entre deux clignements, peut être responsable, en cas d’atteinte sévère, de perturbations optiques équivalentes à des aberrations optiques d’ordre élevé [1] contribuant ainsi à une réduction de la qualité de l’image rétinienne et donc de la fonction visuelle.
Les méthodes utilisées pour évaluer le retentissement visuel des perturbations du film lacrymal proviennent pour l’essentiel du domaine de la chirurgie réfractive et de l’analyse de la qualité de vision, notamment l’aberrométrie, de type Hartmann-Schack ou double passage, mais aussi la topographie cornéenne de Placido ou l’interférométrie.
Un simple calcul illustre assez bien l’importance de cette relation [1] ; le rayon antérieur du film lacrymal est approximativement de 7,8 mm et son index de réfraction est de 1,336, donnant une surface cornéenne d’une puissance de 43,08 D. Pour une épaisseur de film comprise entre 6 et 20 microns, une réduction uniforme de l’épaisseur du film aura un effet modeste sur la puissance cornéenne en raison d’une modification maximale de 20 microns du rayon du film lacrymal, entraînant une modification maximale de 0,10 D de puissance. À l’inverse, si le film lacrymal devient irrégulier en épaisseur, de plus grandes variations du rayon de courbure du film pourront apparaître de façon localisée, pouvant ainsi générer de plus grandes variations de puissance. Ainsi, une réduction du rayon de 7,8 à 7,6 mm entraîne une augmentation de puissance de la surface de 1,30 D, expliquant ainsi facilement le retentissement visuel (fig. 2-37).

Fig. 2-37 a. Modification de l’épaisseur du film lacrymal et pouvoir réfractif. b. Illustration d’une réduction irrégulière du film lacrymal chez un patient présentant un syndrome sec avec diminution du temps de rupture du film lacrymal et apparition de dry spots sur la surface cornéenne.
Les topographes cornéens utilisant la technique de Placido ne sont pas, à proprement parler, des appareils destinés à l’étude du film lacrymal, mais l’altération de la surface épithéliale cornéenne secondaire à une diminution quantitative des larmes peut entraîner des modifications kératométriques et topographiques non négligeables.
Ainsi, l’index de régularité de surface (surface regularity index ou SRI) et l’index d’asymétrie de surface (surface asymmetry index ou SAI) sont les index les plus sensibles lors de perturbations du film lacrymal [2, 3]. Ces indices constituent éventuellement une aide au suivi, plus qu’un outil diagnostique, en complément de l’examen clinique mais ne renseignent pas sur l’aspect fonctionnel et encore moins sur la qualité de vision du patient. Une étude avait cependant pu déterminer une altération significative des principaux indices de topographie (SRI, SAI, IAI ou irregular astigmatism index) dans une population de patients souffrant d’œil sec comparée à une population de sujets sains, concluant à l’aide de cette technique dans le diagnostic mais surtout dans l’évaluation de la sévérité fonctionnelle du syndrome sec [4]. Leurs principaux intérêts résident dans leur caractère ubiquitaire susceptible d’apporter des renseignements sur la cinétique du film lacrymal ou sur le retentissement épithélial cornéen d’un déficit éventuel (fig. 2-38). Certains appareils ont été récemment développés dans ce sens, incluant un programme d’analyse de la stabilité du film lacrymal dans leur outil diagnostique [5].

Fig. 2-38 Aspect en topographie cornéenne d’un patient souffrant d’une kératite sèche avant (a) et après (b) utilisation de collyre lubrifiant. L’acuité visuelle est donnée en corrélation.
Cette notion de qualité de vision a vu le jour initialement en chirurgie réfractive, cornéenne et cristallinienne, où elle s’est attachée à renseigner ce que l’acuité visuelle ne donne pas en termes de confort de vue par le patient, à acuité visuelle égale. Ainsi la qualité de vision peut être définie à la fois dans sa composante optique, incluant la traversée des milieux du globe en commençant par le film lacrymal, et dans une composante neurosensorielle, après stimulation des photorécepteurs rétiniens par traitement du signal recueilli au niveau des aires corticales visuelles. C’est principalement à la première composante « réfractive » que le clinicien pourra tenter d’analyser le retentissement d’un dysfonctionnement, notamment lacrymal, sur la vision. Le principe d’analyse est essentiellement basé sur les techniques d’aberrométrie, étudiant la déformation d’un front d’onde à travers un système optique, soit de type Hartmann-Schack, soit de type double passage (optical quality analysing system ou OQAS).
Le principe de l’appareil est basé sur l’analyse de la déformation d’un front d’onde émis de façon sphérique et récupéré à la sortie de l’œil après traversée des milieux et réflexion fovéale. Ce front d’onde est naturellement délimité par le pourtour de la pupille de sortie. En pratique, aucun œil, même emmétrope, n’est dépourvu d’aberrations optiques de haut degré, principalement représentées par le coma ou l’aberration sphérique.
Tout trouble des milieux, déformation cornéenne ou cristallinienne peut induire des aberrations de haut degré, l’instabilité du film lacrymal pouvant également en induire.
Une aberration optique traduit donc la déviation d’un front d’onde étudié par rapport à un front d’onde idéal. Cet écart est mesuré par le coefficient RMS (root mean square) qui correspond à la racine carrée de la somme de ces écarts, élevés au carré et divisés par le nombre de points ayant servi à la mesure.
La mesure du RMS chez le sujet sain montre une fluctuation physiologique entre deux clignements (fig. 2-39) [1]. Ainsi la valeur du RMS, donc la quantité d’aberrations, augmente progressivement après un clignement jusqu’au prochain, ce qui permet d’abaisser à nouveau le niveau total des aberrations. Il a été montré une corrélation directe entre RMS et volume du ménisque lacrymal inférieur, avec une moindre variation du premier après clignement lorsque le second est plus élevé avant clignement [1, 6]. De façon analogue, Kaido et al. ont montré une amélioration de l’acuité visuelle fonctionnelle chez les patients souffrant de sécheresse oculaire par utilisation de bouchons méatiques [7].

Fig. 2-39 Variation physiologique du coefficient RMS entre deux clignements, d’après Montes Mico et Phil [1].
L’utilisation d’un appareil de type double passage (DP) permet de déterminer la fonction de modulation de transfert (modulation transfer function ou MTF), laquelle renseigne sur les performances optiques globales de l’œil, incluant les défauts optiques susceptibles de dégrader la qualité de l’image rétinienne comme la diffraction, les aberrations et la diffusion de lumière [8]. Cette dernière a tendance à augmenter avec l’âge et la perte de transparence du cristallin rendant, chez le sujet âgé, le système DP plus performant dans la détection des aberrations visuelles que le système Hartmann-Schack. Le système DP a l’avantage de permettre une mesure objective de l’effet conjoint des aberrations optiques de haut degré et de la perte de transparence de l’ensemble des tissus oculaires. L’appareil est piloté au moyen d’un logiciel permettant de réaliser une mesure dynamique de la fonction d’étalement du point (point spread function ou PSF) sur 20 secondes avec une résolution d’une demi-seconde ; ainsi, les fluctuations de PSF observées sont directement imputables aux modifications du film lacrymal. À chaque mesure de la PSF est associé un indice objectif de diffusion (objective scattering index ou OSI). Celui-ci correspond au rapport de la lumière enregistrée entre une zone annulaire située entre 12 et 20 minutes de l’arc et une zone circulaire centrale de 1 minute d’arc. Les valeurs de l’OSI augmentent avec le niveau de diffusion intra-oculaire. Le système prend également en compte les clignements survenus dans la période des 20 secondes, ce qui permet également une analyse indirecte de la sévérité du syndrome sec [9, 10]. Ainsi, les variations d’OSI apparaissent plus importantes pour évaluer le degré de retentissement fonctionnel de l’œil sec que la valeur absolue de l’index (fig. 2-40). L’index OSI doit, pour être utilisé dans l’analyse fonctionnelle de la sécheresse oculaire, être confronté à la clinique, en particulier en éliminant un trouble de transparence des milieux comme une cataracte, susceptible d’influer sur sa valeur.

Fig. 2-40 Évaluation en OQAS de l’index OSI en fonction du degré de sévérité de l’œil sec.
Cette méthode, développée initialement au Japon, est basée sur l’évaluation dynamique de l’acuité visuelle [11]. Si cette dernière est le plus souvent excellente en dehors de pathologies associées, elle ne reflète que très mal la qualité de vision du sujet souffrant de sécheresse oculaire et surtout la stabilité de sa vision. Ainsi, l’idée d’une évaluation dynamique de l’acuité visuelle a permis le développement d’un outil spécifique permettant l’enregistrement d’une acuité visuelle d’un sujet pendant 30 secondes sans clignements (sous anesthésique de contact). Le système initial a été ensuite modifié pour permettre une évaluation dynamique sur 60 secondes en laissant le sujet cligner et sans anesthésie. Une étude préliminaire comparant des sujets atteints de sécheresse (SS) modérée à des sujets sains a mis en évidence des scores plus bas de FVA dans le groupe SS confirmant ainsi l’intérêt de la méthode [11]. D’autres études, basées sur l’évaluation de la FVA, ont confirmé son intérêt, montrant l’influence positive de bouchons méatiques sur la stabilité de l’acuité visuelle dans une population de patients souffrant de sécheresse oculaire [12] ou, plus récemment, utilisant le test FVA conjointement à un questionnaire pour dépister un syndrome sec dans une population de sujets travaillant sur écran [13].
Le patient présentant une anomalie de surface avec retentissement sur le film lacrymal peut, quelle que soit l’étiologie, subir une altération de sa qualité de vision, voire une diminution de son acuité visuelle. Il faut garder à l’esprit que, au-delà du sujet souffrant d’un syndrome sec avéré, avec retentissement épithélial cornéen – source de signes fonctionnels à type de gêne, douleurs et troubles visuels –, une instabilité du film lacrymal, non associée à une épithéliopathie, sera également à l’origine d’une altération de la qualité de vision. Cette notion permet de comprendre que le nombre de patients touchés va bien au-delà du patient clairement identifié « syndrome sec » [14].
Cette notion d’instabilité du film lacrymal, distinguée du syndrome sec par hyposécrétion aqueuse et atteinte épithéliale est également associée à un déficit mucinique, principalement MUC5AC et MUC16, majoritairement en cause dans l’effondrement du BUT (break-up time). L’étude de Shimazaki-Den et al. retrouvent, dans deux groupes de patients, ceux avec instabilité seule et ceux avec instabilité associée à une atteinte tissulaire, une altération de la fonction visuelle, notamment évaluée par la mesure de l’acuité visuelle fonctionnelle [15].
Une étude récente retrouve d’ailleurs une diminution de la rapidité de lecture et une atteinte de la sensibilité aux contrastes chez des patients souffrant de sécheresse oculaire comparés à des patients indemnes avec une corrélation avec le degré de sévérité du syndrome sec [16]. Plus le syndrome sec est sévère, moins bonne est la vitesse de lecture.
De façon analogue, Denoyer et al. ont étudié l’impact de la sécheresse oculaire sur la conduite automobile à l’aide d’un simulateur de conduite (détaillé au chapitre 3-II : Qualité de vie, qualité de vision) [17]. Les études de qualité de vie analysant le retentissement du syndrome sec sur les patients atteints confirment également le rôle prépondérant de la baisse de qualité de vision, notamment en vision de près et donc en lecture [18].
Les étiologies susceptibles d’induire une telle instabilité du film lacrymal sont multiples et les causes chirurgicales, cornéennes réfractives ou post-cataracte, représentent un nombre considérable de patients quelle que soit leur prédisposition initiale. Ainsi, la chirurgie de la cataracte est fréquemment pourvoyeuse de syndrome sec postopératoire clairement mis en évidence par questionnaire ou examen clinique et pouvant persister jusqu’à 3 mois postopératoires. L’influence de l’incision cornéenne, des antiseptiques préopératoires, du lavage abondant peropératoire et des collyres postopératoires conservés a été citée, entre autres facteurs, pour en expliquer la survenue [19]. Ainsi, de nombreux patients vont ressentir des symptômes de sécheresse oculaire, le plus souvent dans le mois postopératoire et plus encore à l’arrêt du traitement anti-inflammatoire. Ils pourront se traduire soit en cortège de symptômes habituels à type de gêne, sensation de sable dans l’œil ou brûlures, soit, de façon courante, uniquement sous forme de gêne fonctionnelle visuelle, à type de flou ou de vision fluctuante, faisant parfois remettre en cause la qualité du résultat réfractif ou de la paire de lunettes complémentaires postopératoires. La prise en charge passera alors par un diagnostic, une évaluation de la sévérité du syndrome sec, un traitement substitutif et surtout une explication afin de rassurer le patient souvent angoissé par le résultat chirurgical en lui-même. Ce retentissement est encore accentué par l’utilisation d’implants à valeur réfractive ajoutée, comme les implants toriques et surtout les implants multifocaux, utilisés pour une meilleure qualité de vision et d’indépendance aux lunettes et pour lesquelles, une fluctuation visuelle postopératoire peut faire remettre la qualité du résultat en question. Certains auteurs ont d’ailleurs proposé l’utilisation systématique d’un traitement postopératoire comme la ciclosporine chez les patients implantés en optique multifocale, avec une amélioration significative de la sensibilité aux contrastes comparés à ceux qui n’en bénéficiaient pas [20].
Le syndrome sec induit ou renforcé après chirurgie réfractive cornéenne est bien connu et sera développé au chapitre 12-VI. Il représente, de façon presque unanime selon les séries, la deuxième cause de non-satisfaction du patient après l’erreur réfractive, en PKR comme en Lasik, avec découpe mécanique ou au laser femtoseconde [21, 22]. Son incidence est telle qu’il convient de prévenir le patient systématiquement en préopératoire, voire d’anticiper en utilisant, par exemple, des bouchons méatiques transitoires [23]. De façon analogue, au patient opéré de cataracte, l’instabilité du film lacrymal aura une incidence visuelle non négligeable en postopératoire et devra être expliquée et traitée pendant une durée variable allant de quelques semaines à plusieurs mois.
Les patients susceptibles d’avoir un impact fonctionnel visuel d’un dysfonctionnement du film lacrymal, simple instabilité ou atteinte tissulaire de surface associée, sont donc nombreux et le motif de consultation dépasse largement le cadre strict de la sécheresse oculaire ou même de la surface oculaire.
[1] Montes-Mico R, Phil M. Role of the tear film in the optical quality of the human eye. J Cataract Refract Surg 2007 ; 33 : 1631-35.
[2] Goto T, Zheng X, Klyce SD, et al. A new method for tear film stability analysis using videokeratography. Am J Ophthalmol 2003 ; 135 : 607-12.
[3] Labbé A, Brignole-Baudouin F, Baudouin C. Ocular surface investigations in dry eye. J Fr Ophtalmol 2007 ; 30 : 76-97.
[4] de Paiva CS, Lindsey JL, Pflugfelder SC. Assessing the severity of keratitis sicca with videokeratoscopic indices. Ophthalmology 2003 ; 110 : 1102-9.
[5] Gumus K, Crockett CH, Rao K, et al. Noninvasive assessment of tear stability with the tear stability analysis system in tear dysfunction patients. Invest Ophthalmol Vis Sci 2011 ; 52 : 456-61.
[6] Koh S, Tung C, Aquavella J, et al. Simultaneous measurement of tear film dynamics using wavefront sensor and optical coherence tomography. Invest Ophthalmol Vis Sci 2010 ; 51 : 3441-48.
[7] Kaido M, Ishida R, Dogru M, et al. Efficacy of punctum plug treatment in short break-up time dry eye. Optom Vis Sci 2008 ; 85 : 758-63.
[8] Díaz-Doutón F, Benito A, Pujol J, et al. Comparison of the retinal image quality with a Hartmann- Shack wavefront sensor and a double-pass instrument. Invest Ophthalmol Vis Sci 2006 ; 47 : 1710-6.
[9] Habay T, Majzoub S, Perrault O, et al. Évaluation objective de l’impact fonctionnel de la sévérité de la sécheresse oculaire sur la qualité de vision par aberrométrie double passage. J Fr Ophtalmol 2014 ; 37 : 188-94.
[10] Benito A, Pérez GM, Mirabet S, et al. Objective optical assessment of tear film quality dynamics in normal and mildly symptomatic dry eyes. J Cataract Refract Surg 2011 ; 37 : 1481-7.
[11] Ishida R, Kojima T, Dogru M, et al. The application of a new continuous functional visual acuity measurement system in dry eye syndromes. Am J Ophthalmol 2005 ; 139 : 253-8.
[12] Kaido M, Ishida R, Dogru M, Tsubota K. Visual function changes after punctal occlusion with the treatment of short BUT type of dry eye. Cornea 2012 ; 31 : 1009-13.
[13] Kaido M, Uchino M, Yokoi N, et al. Dry-eye screening by using a functional visual acuity measurement system: the osaka study. Invest Ophthalmol Vis SCI 2014 ; 55 : 3275-81.
[14] Aragona P, Rolando M. Towards a dynamic customised therapy for ocular surface dysfunctions. Br J Ophthalmol 2013 ; 97 : 955-60.
[15] Shimazaki-Den S, Dogru M, Higa K, Shimazaki J. Symptoms, visual function, and mucin expression of eyes with tear film instability. Cornea 2013 ; 32 : 1211-8.
[16] Ridder WH, Zhang Y, Huang JF. Evaluation of reading speed and contrast sensitivity in dry eye disease. Optom Vis Sci 2013 ; 90 : 37-44.
[17] Deschamps N, Ricaud X, Rabut G, et al. The impact of dry eye disease on visual performance while driving. Am J Ophthalmol 2013 ; 156 : 184-9.
[18] Li M, Gong L, Chapin WJ, Zhu M. Assessment of vision-related quality of life in dry eye patients. Invest Ophthalmol Vis Sci 2012 ; 53 : 5722-7.
[19] Kasetsuwan N, Satitpitakul V, Changul T, Jariyakosol S. Incidence and pattern of dry eye after cataract surgery. PLoS One 2013 ; 12-8 : e78657.
[20] Donnenfeld ED, Solomon R, Roberts CW, et al. Cyclosporine 0.05 % to improve visual outcomes after multifocal intraocular lens implantation. J Cataract Refract Surg 2010 ; 36 : 1095-100.
[21] Levinson BA, Rapuano CJ, Cohen EJ, et al. Referrals to the Wills Eye Institute Cornea Service after laser in situ keratomileusis : reasons for patient dissatisfaction. J Cataract Refract Surg 2008 ; 34 : 32-9.
[22] Golas L, Manche EE. Dry eye after laser in situ keratomileusis with femtosecond laser and mechanical keratome. J Cataract Refract Surg 2011 ; 37 : 1476-80.
[23] Yung YH, Toda I, Sakai C, et al. Punctal plugs for treatment of post-LASIK dry eye. Jpn J Ophthalmol 2012 ; 56 : 208-13.
A. Labbé, L. Batellier, C. Baudouin
De très nombreuses techniques d’exploration ont été développées pour analyser cliniquement ou biologiquement la stabilité et la composition du film lacrymal. Certains de ces tests sont aujourd’hui validés et constituent des méthodes standard pour analyser les maladies de la surface oculaire en pratique clinique. D’autres méthodes restent encore du domaine de la recherche et nécessitent d’être évaluées afin de préciser les conditions de leur utilisation. Toutes ces techniques permettent néanmoins de mieux comprendre la physiopathologie du film lacrymal et les pathologies de la surface oculaire qui lui sont associées.
La surface cornéoconjonctivale est la muqueuse de l’organisme la plus exposée aux agressions extérieures et le film lacrymal constitue sa deuxième ligne de défense après les paupières. De nombreuses techniques d’exploration ont donc été développées pour évaluer objectivement le film lacrymal et la surface oculaire en pratique clinique d’une manière peu ou pas invasive. Sur le plan de la biologie, c’est dans les cas complexes où le diagnostic étiologique est difficile, en raison de l’intrication de différents mécanismes physiopathologiques, que l’exploration des protéines lacrymales et/ou le bilan allergologique lacrymal peuvent s’avérer utiles. Le facteur limitant principal de ces explorations reste néanmoins le prélèvement de larmes. Le développement d’appareils multiparamétriques performants et travaillant sur des volumes minimes d’échantillons offrira, après leur validation technique pour l’analyse des larmes, de nouvelles stratégies diagnostiques mais aussi une meilleure compréhension des mécanismes impliqués dans les nombreuses pathologies impliquant le film lacrymal.
Malgré leur utilisation fréquente en pratique clinique, les tests standard pour évaluer le syndrome sec et les maladies de la surface oculaire – recherche des symptômes, temps de rupture du film lacrymal, évaluation des glandes de Meibomius, test à la fluorescéine cornéen, test de Schirmer – ont montré une reproductibilité et une fiabilité faibles. De plus, les symptômes subjectifs sont souvent peu ou mal corrélés aux signes objectifs. De nombreuses autres techniques d’exploration ont donc été développées pour évaluer le film lacrymal et la surface oculaire en pratique clinique [1]. Certaines sont facilement accessibles aux cliniciens, alors que d’autres restent des procédures de recherche qui nécessitent encore d’être validées mais pourraient constituer dans un futur proche une batterie de méthodes fiables pour l’évaluation clinique des désordres de la surface oculaire.
Les méthodes pour mesurer l’épaisseur totale du film lacrymal ne sont pas actuellement utilisées en pratique clinique. Différentes techniques utilisant le principe de l’interférométrie, de la réflectance ou encore de la tomographie par cohérence optique (OCT) ont ainsi retrouvé des épaisseurs allant de 3 à 6 µm chez les sujets normaux et aux alentours de 2 µm chez les sujets atteints de sécheresse oculaire [2]. Certains auteurs ont suggéré une valeur limite d’épaisseur du film lacrymal de 2,75 µm qui aurait une sensibilité de 86 % et une spécificité de 94 % pour le diagnostic de sécheresse oculaire [3].
Le ménisque des larmes correspond au réservoir concave de larmes situé au niveau des marges palpébrales supérieures et inférieures. La plus grande partie du film lacrymal se situe au niveau du ménisque lacrymal dont la mesure représenterait un bon indicateur du volume lacrymal total [4]. Sa hauteur, son rayon, sa profondeur, sa surface, son volume ou encore sa courbure ont été mesurés avec des techniques variées comme la lampe à fente, la vidéo-kératographie, la vidéo-méniscométrie en réflexion spéculaire, le système Tearscope® et récemment en TD-OCT et SD-OCT (fig. 2-41) [1, 2]. Pour certains auteurs, une diminution de la hauteur et du rayon du ménisque lacrymal inférieur serait un bon indicateur de sécheresse oculaire avec des valeurs seuils respectivement de 1,64 mm et 1,82 mm [5]. Les études les plus récentes utilisant la technique de SD-OCT ont également montré une bonne corrélation entre les paramètres d’évaluation du ménisque des larmes et les paramètres cliniques comme le test de Schirmer ou le BUT [6]. Cependant, à la différence du test de Schirmer I qui mesure aussi une partie de la sécrétion réflexe, la hauteur du ménisque des larmes ne représente que le volume basal des larmes. Ces techniques ont aussi été utilisées pour évaluer l’élimination de collyres instillés dans les culs-de-sac conjonctivaux ou encore l’efficacité de traitements comme l’occlusion des points lacrymaux [7].

Fig. 2-41 Évaluation du ménisque des larmes à l’aide d’un OCT de segment antérieur.
a. Image d’un ménisque lacrymal normal. b. Disparition du ménisque lacrymal qui est remplacé par un conjonctivochalasis.
La fluorophotométrie des larmes a été développée initialement par David Maurice en 1963. La technique a été améliorée par l’utilisation de fluorophotomètres automatisés de grande sensibilité (Fluorotron Master®, Coherent Radiation, Inc., États-Unis) [8]. Le volume des larmes et leur renouvellement peuvent être calculés après l’application d’une goutte de fluorescéine et le recueil d’un échantillon de larmes. Eter et Gobbels ont également proposé une technique non-contact de fluorophotométrie des larmes en établissant une calibration avec différentes concentrations de fluorescéine dans une chambre test [9]. Cela a rendu possible la mesure du volume lacrymal et son renouvellement sans recueil d’un échantillon de larmes. La disparition de la fluorescéine après instillation de 1 µl de fluorescéine à 2 % est enregistrée sur une période de plus de 30 minutes. Cette élimination suivrait une courbe biphasique permettant de calculer un taux de renouvellement du film lacrymal [10]. Dans la plupart des études de la littérature, le flux normal de larmes approche 1 µl/minute, avec un taux de renouvellement des larmes de 15 à 22 %/minute. Ce flux diminue dans l’œil sec à des valeurs entre 0,10 et 0,55 µl/minute et le renouvellement chute entre 6 à 8 %/minute, avec des valeurs plus élevées dans les atteintes meibomiennes par rapport aux déficits aqueux [10, 11]. À cause de la concentration de fluorescéine utilisée, du temps choisi pour effectuer les mesures séquentielles après instillation, de l’influence du temps d’examen, et du manque de standardisation de cette technique, les résultats peuvent être très différents d’un investigateur à l’autre, raison pour laquelle cette technique n’est pas devenue pour l’instant un standard dans l’exploration des syndromes secs.
La couche lipidique superficielle du film lacrymal peut être observée et mesurée par interférométrie. L’aspect des interférences générées par réflexion spéculaire d’une lumière sur la couche lipidique du film lacrymal préoculaire fournit des informations intéressantes concernant l’épaisseur de la couche lipidique, sa répartition et sa stabilité (fig. 2-42). Différents appareils ont été développés (Tearscope Plus®, Keeler Instruments, Broomall, États-Unis ; DR-1®, Kowa Co., Ltd., Torrance, États-Unis) pour analyser l’aspect des interférences [2, 12, 13]. Plusieurs classifications des anomalies observées ont également été proposées. Yokoi et al. [14] proposent cinq stades : le stade 1 montre un aspect grisâtre et une distribution uniforme de la couche lipidique ; le grade 2 montre une couleur grisâtre avec une distribution non uniforme ; le stade 3 montre une répartition non uniforme d’interférences colorées ; le stade 4 montre de nombreuses couleurs avec une distribution non uniforme ; le stade 5 montre l’absence de couche lipidique et des zones de cornée exposées. Les films lacrymaux normaux sont cotés entre 1 et 2, les yeux secs sont cotés entre 2 et 5, le grade 2 pouvant être retrouvé dans des films lacrymaux normaux comme dans les yeux secs. La classification de Guillon [15] qui utilise le Tearscope Plus® est un peu différente. Elle est subdivisée en dix niveaux différents (encadré 2-2).
• Niveau 0 : aspect de couche lipidique absente
• Niveau 1 : aspect de fin réseau ouvert
• Niveau 2 : aspect de réseau plus détaillé
• Niveau 3 : aspect de réseau fermé, bien défini
• Niveau 4 : combinaison de l’aspect en réseau et d’un aspect fluide en forme de vagues
• Niveau 5 : aspect en forme de vagues
• Niveau 6 : combinaison d’aspect en forme de vagues et d’aspect amorphe
• Niveau 7 : aspect amorphe
• Niveau 8 : combinaison d’un aspect amorphe et de franges colorées
• Niveau 9 : franges colorées
Les niveaux les plus élevés ont été retrouvés de manière prédominante chez les nouveau-nés et les enfants, montrant une couche lipidique épaisse, alors que les adultes se distribuaient à des niveaux inférieurs [15]. Une limite majeure de cette technique reste néanmoins la très grande variabilité des aspects normaux, les aspects anormaux étant uniquement situés aux extrêmes de cette classification, que sont l’absence de lipides ou une épaisseur augmentée avec un aspect globulaire. Une amélioration de l’analyse des interférences a été proposée en utilisant des enregistrements vidéo de la répartition du film lacrymal et de ses aspects [16, 17] ou en offrant des graphiques assistés par ordinateur colorés en fonction de l’épaisseur de la couche lipidique [18]. Des études dynamiques de la couche lipidique du film lacrymal après le clignement montrent, chez le sujet normal, une stabilisation complète en moins d’une seconde après une propagation d’aspect horizontal. Dans des cas de dysfonctionnements meibomiens ou dans les cas de déficits aqueux, le temps pour atteindre un film lacrymal stable est beaucoup plus long, de plusieurs secondes ou plus, et l’aspect de la propagation est vertical et inégal, avec une couche lipidique plus épaisse en cornée inférieure et plus mince, déficiente, en cornée supérieure [18].
Plus récemment encore, de nouveaux appareils utilisant le principe d’interférométrie, comme le LipiView® interferometer (TearScience Inc, Morrisville, États-Unis), ont également été commercialisés et offrent des mesures quantitatives directes de la couche lipidique du film lacrymal [19]. Ces appareils pourraient être directement utiles au diagnostic de sécheresse oculaire associée à une atteinte des glandes de Meibomius (œil sec par évaporation) [19].
Toutes ces techniques sont utiles pour étudier de manière non invasive le film lacrymal préoculaire et particulièrement sa composante lipidique, son épaisseur à l’aide de mesures qualitatives et semi-quantitatives, sa dynamique juste après le clignement et sa stabilité dans le temps. Cependant, le potentiel discriminatif de ces tests est encore limité par le chevauchement entre les aspects normaux et ceux retrouvés dans des yeux secs modérés. Ces techniques doivent donc s’intégrer dans une évaluation clinique complète de la surface oculaire incluant en particulier les glandes de Meibomius. Ces dernières sont analysées cliniquement mais aussi en meibographie à infrarouge ou encore en OCT (voir chapitres 2-II et 22).

Fig. 2-42 Exemples d’aspect de la phase lipidique du film lacrymal par la technique d’éclairage en lumière froide (Tearscope®).
Noter les franges d’interférence en fonction de l’épaisseur de la couche lipidique.
L’évaporation du film lacrymal semble être le résultat de la stabilité et de la composition de la couche lipidique et possiblement de l’épithélium cornéen, mais elle dépend également de nombreux facteurs individuels et environnementaux, comme la surface interpalpébrale, la position des yeux, le degré d’hygrométrie, les conditions lumineuses et la température. Différents appareils et procédures ont été décrits, mais le principe fondamental est de mesurer l’humidité dans le temps avec un évaporimètre dans une chambre isolée réalisée par des lunettes adhérentes à l’intérieur desquelles la quantité d’eau et la température sont connues. Dans une méta-analyse, Tomlinson et al. ont retrouvé un taux d’évaporation de : 13,57 × 10-7 g/cm2 chez les sujets normaux ; 17,91 × 10-7 g/cm2 chez les sujets avec une déficience aqueuse ; 25,34 × 10-7 g/cm2 chez les sujets avec une sécheresse par excès d’évaporation [20]. La plupart de ces études montrent ainsi une augmentation du taux d’évaporation dans les syndromes secs, avec une hyperosmolarité et une température plus élevées, diminuées après le clignement [21, 22]. Les dysfonctionnements meibomiens entraînent systématiquement une augmentation très importante de l’évaporation par rapport aux yeux normaux ou aux syndromes secs par insuffisance lacrymale. Cependant, les valeurs observées d’une étude à l’autre ne sont pas constantes et montrent de grandes variations des taux d’évaporation calculés. Le taux d’évaporation serait cependant bien corrélé avec la destruction des glandes de Meibomius [23].
La thermographie utilise une méthode indirecte pour évaluer le taux d’évaporation. La température de la cornée est ainsi plus élevée juste après le clignement et diminue rapidement après l’ouverture des yeux. Ces changements subtils peuvent être enregistrés grâce à des thermographes très rapides utilisant les radiations infrarouges. La température de la surface oculaire des patients atteints de sécheresse oculaire serait significativement plus élevée que chez les sujets normaux. En parallèle, la diminution de température lors de l’ouverture des yeux serait plus importante chez les patients avec une sécheresse oculaire [24]. Une relation entre la température et l’inflammation de la surface oculaire a aussi été suggérée [25]. Les conditions d’examen doivent cependant être standardisées pour toutes ces évaluations fonctionnelles du film lacrymal (température constante de la pièce, humidité, luminance et position fixe des yeux), ce qui rend leur diffusion difficile pour la plupart des cliniciens. Par ailleurs, leur intérêt diagnostique n’est pas encore clairement démontré.
Le facteur limitant de l’exploration biologique du film lacrymal réside dans le prélèvement de larmes et ce, malgré le développement de techniques de plus en plus sensibles et utilisant des volumes de plus en plus faibles. La technique de référence reste le prélèvement de larmes à la pipette de transfert, de préférence sans stimulation (fig. 2-43). Le volume précis de larmes ainsi prélevé permet des résultats quantitatifs précis et sensibles.
Compte tenu de la très grande réduction de volume du film lacrymal dans les syndromes secs par déficit aqueux, l’utilisation de techniques de stimulation des larmes, mécaniques ou chimiques, est nécessaire, elle risque toutefois de causer un biais en stimulant la sécrétion réflexe et en provoquant l’arrivée de protéines sériques par exsudation. Ainsi, les taux lacrymaux d’albumine, d’IgG, de transferrine et de fibronectine, protéines non synthétisées par la glande lacrymale mais issues du secteur vasculaire, après une rapide diminution transitoire, sont augmentés en cas de larmoiement réflexe prolongé. Ces résultats seraient identiques dans les larmes prélevées aussitôt après le réveil, en raison d’une inflammation infraclinique pendant la nuit et de la fermeture prolongée des yeux [26]. Dans certains cas, la réalisation d’un échantillon de larmes d’un volume aussi petit que 15 µl peut prendre plus de 40 minutes sans stimulation réflexe [27]. Dans le syndrome de Sjögren, il n’est pas rare de ne pas obtenir de larmes, malgré des tentatives prolongées et des stimulations répétées. Cet obstacle est donc une limitation majeure à tous les examens biologiques du film lacrymal et de nombreux chercheurs ont essayé de développer des techniques nécessitant de très faibles quantités de larmes, de l’ordre de quelques microlitres. Différentes méthodes pour dépasser ce problème de recueil de larmes ont été essayées en collectant les larmes à partir des papiers de test de Schirmer ou de membranes en papier-filtre [28]. Si elle est simple et pratique, cette technique peut cependant altérer certains constituants des larmes qui peuvent être adsorbés sur le papier-filtre et plus ou moins relâchés dans la solution. Une autre technique consiste à rincer la surface oculaire avec du sérum physiologique et analyser la solution obtenue [29]. Ces techniques de prélèvement sont applicables à des tests semi-quantitatifs comme l’étude électrophorétique des protéines lacrymales, mais l’approximation du volume prélevé et du degré d’élution permet difficilement de quantifier de façon précise des constituants lacrymaux.
Ces considérations techniques, associées à la nécessité d’avoir un laboratoire expérimenté dans le recueil des larmes et dans les techniques biologiques qui peuvent être appliquées à de petites quantités de produit biologique, restent néanmoins des limites majeures à l’exploration biologique du film lacrymal.

Fig. 2-43 Prélèvement de larmes à la pipette de transfert.
Ces techniques, validées scientifiquement et accessibles avec un matériel standard, sont une aide au diagnostic de syndrome sec en discriminant le déficit aqueux lié à une atteinte de la glande lacrymale de l’instabilité du film lacrymal dans laquelle les protéines lacrymales ne sont théoriquement pas atteintes. Elles permettent également d’estimer le degré de l’inflammation locale ou de mettre en évidence une sensibilisation locale à un ou plusieurs allergènes dans le cadre des conjonctivites et kératoconjonctivites allergiques.
La concentration totale en protéines dans les larmes varie entre 6 et 11 g/l, elle est un peu plus élevée chez l’enfant et le jeune adulte [30]. Les protéines majeures des larmes peuvent être facilement séparées en utilisant les techniques habituelles d’électrophorèse sur gel d’agarose ou gel de sodium dodecyl sulfate-polyacrylamide (SDS-PAGE). Seulement 5 µl de larmes sont nécessaires pour réaliser une électrophorèse. En utilisant un gel d’agarose, quatre fractions ont été décrites représentant les protéines principales du film lacrymal. Les lipocalines, membres d’une famille de protéines liées aux lipides, forment le premier pic près de l’anode et représentent 25 à 35 % des protéines totales. Elles sont suivies par un petit pic (6 à 10 %) de protéines indéterminées d’origine sérique et lacrymale, puis par une bande faite essentiellement de lactoferrine et d’immunoglobulines (28 à 42 %). Le dernier pic correspond à une protéine unique, le lysozyme, qui migre vers la cathode et constitue 20 à 30 % des protéines totales (fig. 2-44) [30]. Dans des cas de syndromes secs liés à la glande lacrymale, plusieurs pics peuvent être diminués selon la sévérité de la maladie (fig. 2-45). Cette technique pourrait aussi aider à évaluer l’intensité des processus inflammatoires, identifiés par l’augmentation des taux de protéines totales et des protéines d’origine sérique, en particulier l’albumine qui migre au niveau du pic des lipocalines et les immunoglobulines. Cette réaction inflammatoire peut être considérable, au point de réaliser un profil dit « sérique » par passage important de l’ensemble des protéines sériques à travers la barrière hématolacrymale (voir fig. 2-45).
La technique iso-électrique focalisée sur le gel d’électrophorèse permet d’augmenter la séparation des protéines des larmes. Plus de 31 bandes d’électrophorèse ont été observées par Reitz, certaines d’entre elles restant indéterminées à ce jour [31].

Fig. 2-44 a. Tracés d’électrophorèse des protéines lacrymales sur gel d’agarose. b. Exemple de profil électrophorétique normal

Fig. 2-45 Gels d’électrophorèse montrant des tracés pathologiques : diminution des fractions et profil inflammatoire.
Le lysozyme et la lactoferrine sont deux protéines majeures des larmes, sécrétées par les acini des glandes lacrymales. Elles jouent un rôle très important dans la défense de la surface oculaire contre les micro-organismes et possèdent des propriétés anti-oxydantes [32]. Leur diminution dans le film lacrymal est un indicateur intéressant de dysfonctionnement de la glande lacrymale [33]. Les techniques d’immunodiffusion radiale, de turbidimétrie, d’immunonéphélémétrie ou ELISA (enzyme-linked immunosorbent assay) peuvent être utilisées pour leur dosage.
La concentration de lysozyme varie entre 1 et 3 mg/ml dans les larmes normales selon les auteurs et les techniques de dosage utilisées, mais diminue de manière constante dans les syndromes secs [34]. Elle peut également diminuer en fonction de l’âge et du moment de la journée, chaque valeur doit donc être interprétée en fonction d’une population comparable en âge et en fonction des valeurs normales du laboratoire qui doit être habitué à cette technique.
La concentration lacrymale de lactoferrine varie également entre 1 et 3 mg/ml selon les auteurs et les techniques de dosage utilisées. Elle a été évaluée par immunonéphélémétrie dans les larmes normales à 1,66 ± 0,35 mg/l par Batellier et al. [35]. Comme pour le lysozyme, elle diminue de manière constante dans les syndromes secs non Sjögren, dans les syndromes de Sjögren et dans les syndromes de Stevens-Johnson [33]. Une valeur limite à 1,1 mg/ml a été proposée par Fukuda et Wang avec une sensibilité (79,4 %) et une spécificité (78,3 %) optimales [26]. Une étude de Da Dalt et al. en 1996 a comparé la sensibilité et la spécificité du dosage de la lactoferrine avec ceux du test de Schirmer I, du test de cristallisation et d’analyses immunologiques du syndrome de Sjögren (anticorps antinucléaires ou biopsie des glandes salivaires accessoires). Les auteurs ont montré que le dosage de la lactoferrine, par la technique de Lactoplate®, et le test de cristallisation étaient les tests les plus sensibles et les plus spécifiques et étaient également mieux corrélés au diagnostic de syndrome de Sjögren que le test de Schirmer I [36]. Néanmoins, d’autres auteurs ont fait remarquer le manque de corrélation avec des tests cliniques de l’analyse de la lactoferrine dans les yeux secs légers à modérés [37, 38], reflétant probablement la grande hétérogénéité des syndromes secs en pratique clinique.
Quel que soit le type d’œil sec, une donnée commune est l’augmentation de l’osmolarité du film lacrymal, résultant d’une réduction de son volume ou d’une évaporation excessive dans le cas d’un volume normal mais avec un film lacrymal instable. L’hyperosmolarité apparaît donc comme la conséquence terminale des variations de flux du film lacrymal et un élément de mesure important pour analyser les maladies de la surface oculaire. Par ailleurs, l’hyperosmolarité a été largement démontrée comme entraînant une atteinte épithéliale, contribuant au développement de la kératoconjonctivite sèche (KCS), à la libération de cytokines inflammatoires et stimulant des réactions inflammatoires chroniques [2, 39–41]. Même si la mesure de l’osmolarité ne permet pas de différencier l’œil sec par excès d’évaporation et l’œil sec par insuffisance aqueuse, l’osmolarité serait le meilleur marqueur de la sévérité de la sécheresse oculaire [42].
L’osmolarité du film lacrymal peut être mesurée par pression de vapeur, par mesure de l’abaissement du point de congélation ou par impédance électrique [2]. C’est le développement d’appareils permettant la mesure de l’osmolarité en pratique clinique qui a largement contribué à l’essor de cette technique pour la prise en charge des patients atteints de sécheresse oculaire.
Le système TearLab® (Tearlab Inc., San Diego, États-Unis) mesure l’osmolarité par une technique d’impédance électrique. L’avantage de cette technique est le petit volume (0,05 µl) de larmes nécessaire, l’absence d’obligation de transfert du prélèvement – la puce permettant le recueil des larmes est également celle qui analyse l’osmolarité –, et enfin la rapidité d’obtention du résultat (30 secondes pour les deux yeux) [43]. Une valeur d’osmolarité supérieure à 308 mOsms/l pourrait être un indicateur sensible d’une sécheresse oculaire modérée mais surtout un élément permettant de quantifier la sévérité de la sécheresse oculaire. La valeur la plus élevée des deux yeux doit être utilisée (la variabilité de l’osmolarité étant également un marqueur de sécheresse oculaire) et analysée en corrélation avec les résultats des autres tests cliniques. Plus récemment, une valeur de 312 mOsms/l a été proposée et pourrait être plus sensible pour détecter les sécheresses modérées à sévères (sensibilité de 73 % et spécificité de 92 %) [40].
Le Tear Osmometer® (Advanced Instruments Inc., Norwood, États-Unis) calcule l’osmolarité à l’aide de la technique de l’abaissement du point de congélation. Avec cette technique, le prélèvement doit être transféré ensuite dans l’appareil de mesure et nécessite un volume de 0,5 µl [44]. Des études ont montré la bonne corrélation entre la sévérité de l’œil sec et l’osmolarité ainsi mesurée [2].
La précision de ces techniques de mesure reste néanmoins un élément crucial dans le développement de leur utilisation car des chevauchements peuvent être observés entre les valeurs normales et celles des patients atteints de sécheresse oculaire. Par ailleurs, cette mesure peut être variable en raison des modifications intrinsèques de l’osmolarité des larmes, de la localisation du prélèvement ou encore de la technique de recueil.
Une caractéristique physique du film lacrymal est la capacité des mucines à cristalliser et à former des aspects en feuilles de fougère quand il est laissé 5 à 10 minutes à sécher à température ambiante et qu’il est observé sous un microscope à contraste de phase ou un microscope polarisé [45]. Ce test simple peut être utile pour l’évaluation qualitative de la production de mucines [46]. Quatre grades ont été décrits (encadré 2-3 et fig. 2-46).
• Type I : arborisation uniforme de l’ensemble du champ d’observation sans espace entre les aspects en feuilles de fougère. Les arborisations sont nombreuses et de grande taille.
• Type II : le phénomène de cristallisation est toujours abondant mais les aspects en feuilles de fougère sont plus petits et avec une arborisation moindre par rapport au type I. Des espaces vides commencent à apparaître entre les aspects en feuilles de fougère.
• Type III : les arborisations du mucus sont partiellement présentes. Les aspects en feuilles de fougère sont plus petits et incomplètement formés avec peu ou pas de branchements. De grands espaces sans arborisation sont visibles dans le champ du microscope, incluant des agglutinations de mucus sans signe d’organisation.
• Type IV : absence de phénomène de cristallisation. Le mucus apparaît sous forme d’amas ou de filaments, ce qui correspond probablement à une contamination ou à une dégénérescence du mucus associé à des cellules exfoliées.
Selon Rolando, les grades I et II sont retrouvés chez 82,7 % des sujets normaux, alors que les grades III et IV sont observés chez 91,7 % des patients avec une KCS [47]. Aucune différence ne semblait être observée entre les hommes et les femmes, mais l’âge pourrait influencer ce test, car la cristallisation est qualitativement altérée après l’âge de 40 ans. En routine, ce test reste peu pratiqué et des précautions doivent être prises pour éviter certains biais d’interprétation de l’aspect en feuilles de fougère, résultant par exemple de particules provenant du maquillage ou de l’examen des premières gouttes de larmes qui contiennent de nombreux débris cellulaires.

Fig. 2-46 Les quatre stades de la cristallisation des larmes au microscope.
Stades : 1 (a), 2 (b), 3 (c) et 4 (d).
Si l’examen clinique, l’interrogatoire et les tests standard suffisent dans la grande majorité des conjonctivites allergiques, la contribution du laboratoire pour confirmer l’étiologie et permettre d’instaurer un traitement efficace peut être nécessaire devant certains aspects cliniques peu évocateurs ou accompagnés de signes de gravité (conjonctivites chroniques atypiques de l’adulte, kératoconjonctivites vernales, etc.). Les IgE totales lacrymales du sujet non allergique sont très faibles, voire indétectables. Leur dosage nécessite donc une technique immuno-enzymatique à la fois spécifique, sensible et précise, permettant de détecter de façon reproductible des taux d’IgE faibles, de l’ordre de 0,15 kUI/l [48]. Pour les IgE spécifiques, la technique est la même mais le facteur limitant est le volume de larmes nécessaire par allergène recherché.
La seule présence d’IgE dans les larmes ne suffit pas à affirmer l’existence d’une sensibilisation du sujet à un ou plusieurs allergènes. Pour une interprétation satisfaisante du résultat, il est important de différencier les IgE sécrétées localement des IgE lacrymales provenant du secteur vasculaire et filtrées à travers la barrière hématolacrymale. Le taux lacrymal de l’albumine, qui n’est pas synthétisée par les glandes lacrymales, est le reflet de l’état fonctionnel de la barrière hématolacrymale. Son dosage dans le sérum et les larmes, en parallèle de celui des IgE, permet de calculer le rapport des IgE dosées/filtrées. Dans une conjonctivite chronique isolée, la présence d’IgE totales lacrymales peut être le seul argument en faveur d’une origine allergique. Dans tous les cas, le rapport doit être confronté aux autres éléments cliniques et biologiques. Des tests semi-quantitatifs de détection d’IgE totales et/ou spécifiques par technique immunochromatographique ont été récemment développés. De sensibilité inférieure, ils ne permettent pas de différencier les IgE filtrées des IgE dosées [49, 50].
Une grande variété de constituants lacrymaux (protéines, lipides, autres marqueurs) a été étudiée dans le cadre de recherches dont les objectifs principaux sont d’améliorer les possibilités de dosage dans les larmes, de discriminer l’œil sec d’autres atteintes de la surface oculaire et de déterminer les profils inflammatoires, spécialement depuis qu’un processus inflammatoire infraclinique a été identifié comme un mécanisme clé dans la KCS [51, 52].
La principale source de protéines lacrymales est la glande lacrymale avec ses cellules acineuses. Les protéines primaires du film lacrymal sont le lysozyme, la lactoferrine et les lipocalines. Récemment, la protéomique, association d’une électrophorèse bidimensionnelle et d’une analyse protéique par spectrométrie de masse, a permis l’établissement d’une carte protéique bidimensionnelle des larmes. L’objectif est d’identifier l’ensemble des protéines présentes dans les larmes et de corréler les changements des profils protéiques des larmes avec la sécheresse oculaire et, potentiellement, d’utiliser ces protéines comme biomarqueurs du syndrome sec [53]. Ainsi, de nombreuses protéines, dont des dizaines de protéines de faible abondance, ont été identifiées mais la littérature reste partagée concernant leur nombre et leurs fonctions spécifiques [54, 55].
Des approches génomiques sont également en cours de développement avec détection et mesure, avec ou sans amplification, des ARN messagers, permettant de détecter simultanément plusieurs centaines de gènes exprimés dans les larmes ou à la surface de la conjonctive. Elles restent cependant des méthodes complexes et coûteuses limitées à certains laboratoires spécialisés.
Les nouvelles technologies de type multiplex permettent la mesure simultanée d’IgE totales et/ou spécifiques vis-à-vis de plusieurs composants allergéniques différents en un seul test et sur seulement 20 à 30 µl d’échantillon. Déjà utilisées en routine ou en recherche sur le sérum, elles restent à valider sur les larmes mais sont très prometteuses. De nombreux médiateurs de l’allergie font l’objet de recherche dans les larmes : médiateurs synthétisés par les mastocytes (histamine, tryptase, chymase), médiateurs synthétisés par les polynucléaires éosinophiles (eosinophil cationic protein ou ECP) et plus récemment cytokines.
Les glycanes participent à presque tous les processus biologiques, de la signalisation intracellulaire au développement des organes et à la croissance tumorale. La glycomique correspond à l’étude de tous les glycanes exprimés dans des systèmes biologiques. Grâce à de nouvelles méthodes d’étude de ces glycanes, ceux-ci peuvent être envisagés comme de nouveaux biomarqueurs. Vieira et al. ont montré que les glycanes offraient certains avantages, car leur biosynthèse est plus affectée par les maladies que celle des protéines. Il semble techniquement plus facile d’identifier et de quantifier l’expression d’oligosaccharides par rapport à celle des protéines. Dans leur étude, ils ont recueilli les larmes de 28 témoins sains et de 23 patients atteints de rosacée oculaire, montrant une réduction des N-glycanes fucosylés et une augmentation spectaculaire des O-glycanes sulfatés dans ces échantillons. Ils en ont conclu que ces nouveaux glycanes pourraient potentiellement devenir des biomarqueurs objectifs dans la rosacée oculaire [56].
Le facteur de croissance épithélial (epidermal growth factor ou EGF) a un rôle important dans la régulation de la surface oculaire et le renouvellement épithélial. Ce facteur de croissance synthétisé par la glande lacrymale a été retrouvé diminué dans les syndromes secs liés ou non à un syndrome de Gougerot-Sjögren [33, 57] mais aussi dans les cas de syndromes de Stevens-Johnson [33]. Ces auteurs ont également testé l’aquaporine-5 en ELISA. Il s’agit d’une protéine membranaire impliquée dans la sécrétion d’eau de part et d’autre des membranes apicales des cellules acinaires et ductales des glandes lacrymales, mais aussi au niveau de l’épithélium cornéen. Ils ont observé une concentration d’aquaporine-5 quatre fois supérieure dans les larmes des yeux de syndromes de Sjögren par rapport aux yeux des sujets contrôles, mais avec une grande variabilité et parfois des résultats contradictoires. Les syndromes secs non-Sjögren présentent également une augmentation de la concentration d’aquaporine-5 qui pourrait résulter d’une atteinte cornéenne entraînant la libération de cette protéine dans les larmes à partir de l’épithélium cornéen [33].
Les cystatines S et SN, des inhibiteurs des protéases contrôlant l’activité protéase de la cystéine, sont présentes dans le film lacrymal [31]. Elles ont un rôle de protection vis-à-vis des cellules de l’épithélium cornéoconjonctival.
L’activation des phospholipases dans les maladies de la surface oculaire serait liée aux endotoxines bactériennes ou aux réactions inflammatoires induites par les phagocytes mononucléés. Elle pourrait être également le résultat d’une sécrétion par la glande lacrymale en réponse à un stimulus inflammatoire provenant de la surface oculaire. Une grande concentration de phospholipases dans les larmes peut entraîner une augmentation de la dégradation des lipides ainsi qu’une instabilité accrue du film lacrymal.
La principale métalloprotéinase retrouvée dans le film lacrymal est la MMP-9. C’est un marqueur inflammatoire non spécifique dont le taux est augmenté dans les larmes chez les patients atteints de sécheresse oculaire. Chotikavanich et al. ont montré que l’activité de la MMP-9 était plus élevée dans les larmes des patients atteints de syndromes secs et cette activité était corrélée aux paramètres cliniques d’évaluation de la surface oculaire [58]. Une activité accrue de la MMP-9 pourrait ainsi contribuer à l’altération de la barrière épithéliale cornéenne [59]. Un test immunochromatographique semi-quantitatif utilisable en pratique clinique a ainsi été développé pour évaluer de manière rapide la présence de cette MMP dans les larmes (RPS [rapid pathogen screening] InflammaDry® detector). Chez l’homme, le taux normal de MMP-9 dans les larmes se situerait entre 3 et 40 ng/ml [58] et le test détecterait des taux de MMP-9 égaux ou supérieurs à 40 ng/ml.
Les produits du gène MUC5AC synthétisés par les cellules à mucus ont été analysés en utilisant les bandelettes du test de Schirmer grâce à des techniques d’immunoperoxydase [60]. Les résultats ont montré une concentration diminuée dans les yeux secs, comme pour les résultats d’empreintes conjonctivales, mais la très grande variabilité des niveaux de MUC5AC chez les sujets normaux limite les avantages de cette technique. Les quantités de mucines ont aussi été mesurées en utilisant la technique ELISA, elles étaient diminuées dans les syndromes secs par rapport aux yeux normaux, mais aussi chez les patients glaucomateux et chez les porteurs de lentilles de contact [61].
La technique de chromatographie haute performance sur couche fine a été décrite pour séparer les principales classes de lipides présentes dans les larmes [62]. Des techniques supplémentaires peuvent être utilisées sur les sécrétions meibomiennes pour différencier la très grande variété de lipides des larmes où peuvent s’associer différentes classes de phospholipides, sphingolipides, céramides, cérébrosides et acides gras. Les acides gras insaturés seraient présents uniquement chez les patients avec un dysfonctionnement meibomien [63].
Plusieurs cytokines inflammatoires ont été retrouvées avec succès dans les larmes, dans des états pathologiques mais aussi à l’état normal. L’IL-6 et l’IL-8 ont été retrouvées dans les larmes normales [64]. L’IL-6 a aussi été retrouvée à des niveaux significativement plus élevés dans les larmes de patients avec un syndrome de Sjögren par rapport aux yeux normaux. Les cytokines pro-inflammatoires IL-1α et IL-1β ont aussi été retrouvées à des niveaux augmentés dans l’œil sec, comme la MMP-9 matricielle, une enzyme qui clive le précurseur de l’IL-1β en sa forme active, probablement parce qu’ils ont pour origine, au moins pour une partie, l’épithélium conjonctival [65]. Une activité élevée des plasmines a aussi été retrouvée dans les larmes de patients avec un syndrome de Sjögren, suggérant une activité protéolytique importante probablement associée aux réactions inflammatoires dans les glandes lacrymales et/ou les cellules de la surface oculaire [66].
Le stress oxydant a aussi été recherché dans les larmes de sujets normaux et de patients souffrant de syndromes secs. Des niveaux élevés de peroxydes lipidiques et une activité myéloperoxidase ont été retrouvés dans les larmes de l’œil sec, indiquant un stress oxydant et une activité inflammatoire dans cette maladie [67]. Ces tests sont cependant peu discriminants entre les différentes formes de syndromes secs, ceux avec une sécrétion aqueuse de larmes déficiente et ceux qui présentent des symptômes subjectifs mais avec une sécrétion lacrymale préservée. Néanmoins, le stress oxydant peut être augmenté par des réactions inflammatoires et favorisé par la diminution des agents anti-oxydants comme le lysozyme et la lactoferrine. Cette évaluation du stress oxydant au niveau de la surface oculaire reste d’un grand intérêt, car il peut devenir dans le futur la cible de nouveaux traitements locaux.
Des auto-anticorps ont aussi été testés dans les larmes de patients avec un syndrome de Sjögren avec la technique ELISA. Des anticorps anti-SSA et anti-SSB ont été retrouvés dans les larmes comme dans le sérum, mais étrangement certains patients (plus de quatre sur dix pour la recherche d’anti-SSB) montraient des larmes positives, alors que les anticorps correspondant étaient négatifs dans le sérum [63].
De très nombreuses explorations sont possibles pour analyser cliniquement ou biologiquement la stabilité et la composition du film lacrymal ainsi que l’atteinte de la surface oculaire. Beaucoup de ces tests ont été validés et constituent maintenant des méthodes standard pour analyser les maladies de la surface oculaire. Pour d’autres, une validation définitive est encore nécessaire avant la diffusion de leur utilisation, mais elles sont prometteuses et présentent un très grand intérêt en recherche. Néanmoins, toutes ces techniques offrent de nombreuses avancées vers une meilleure compréhension de l’atteinte du film lacrymal dans les désordres de la surface oculaire et constituent une base d’évaluation pour le traitement des patients souffrant de syndromes secs.
[1] Labbé A, Brignole-Baudouin F, Baudouin C. Méthodes d’évaluation de la surface oculaire dans les syndromes secs. J Fr Ophtalmol 2007 ; 30 : 76-97.
[2] McGinnigle S, Naroo SA, Eperjesi F. Evaluation of dry eye. Surv Ophthalmol 2012 ; 57 : 293-316.
[3] Azartash K, Kwan J, Paugh JR, et al. Pre-corneal tear film thickness in humans measured with a novel technique. Mol Vis 2011 ; 17 : 756-67.
[4] Johnson ME, Murphy PJ. The agreement and repeatability of tear meniscus height measurement methods. Optom Vis Sci 2005 ; 82 : 1030-7.
[5] Shen M, Li J, Wang J, et al. Upper and lower tear menisci in the diagnosis of dry eye. Invest Ophthalmol Vis Sci 2009 ; 50 : 2722-6.
[6] Altan-Yaycioglu R, Sizmaz S, Canan H, Coban-Karatas M. Optical coherence tomography for measuring the tear film meniscus : correlation with schirmer test and tear-film breakup time. Curr Eye Res 2013 ; 38 : 736-42.
[7] Park DI, Lew H, Lee SY. Tear meniscus measurement in nasolacrimal duct obstruction patients with Fourier-domain optical coherence tomography : novel three-point capture method. Acta Ophthalmol 2012 ; 90 : 783-7.
[8] Sorbara L, Simpson T, Vaccari S, et al. Tear turnover rate is reduced in patients with symptomatic dry eye. Cont Lens Anterior Eye 2004 ; 27 : 15-20.
[9] Eter N, Gobbels M. A new technique for tear film fluorophotometry. Br J Ophthalmol 2002 ; 86 : 616-9.
[10] Tomlinson A, Khanal S. Assessment of tear film dynamics : quantification approach. Ocul Surf 2005 ; 3 : 81-95.
[11] McCann LC, Tomlinson A, Pearce EI, et al. A clinical alternative to fluorophotometry for measuring tear production in the diagnosis of dry eye. Cornea 2010 ; 29 : 745-50.
[12] Nichols JJ, Sinnott LT. Tear film, contact lens, and patient-related factors associated with contact lens-related dry eye. Invest Ophthalmol Vis Sci 2006 ; 47 : 1319-28.
[13] Ounnoughene Y, Benhatchi N, Agboke J, et al. Le vidéo Tearscope : une nouvelle méthode d’évaluation du film lacrymal in vivo. J Fr Ophtalmol 2006 ; 29 : 476-84.
[14] Yokoi N, Takehisa Y, Kinoshita S. Correlation of tear lipid layer interference patterns with the diagnosis and severity of dry eye. Am J Ophthalmol 1996 ; 122 : 818-24.
[15] Isenberg SJ, Del Signore M, Chen A, et al. The lipid layer and stability of the preocular tear film in newborns and infants. Ophthalmology 2003 ; 110 : 1408-11.
[16] Goto E, Tseng SC. Kinetic analysis of tear interference images in aqueous tear deficiency dry eye before and after punctal occlusion. Invest Ophthalmol Vis Sci 2003 ; 44 : 1897-905.
[17] Goto E, Tseng SC. Differentiation of lipid tear deficiency dry eye by kinetic analysis of tear interference images. Arch Ophthalmol 2003 ; 121 : 173-80.
[18] Goto E, Dogru M, Kojima T, Tsubota K. Computer-synthesis of an interference color chart of human tear lipid layer, by a colorimetric approach. Invest Ophthalmol Vis Sci 2003 ; 44 : 4693-7.
[19] Finis D, Pischel N, Schrader S, Geerling G. Evaluation of lipid layer thickness measurement of the tear film as a diagnostic tool for Meibomian gland dysfunction. Cornea 2013 ; 32 : 1549-53.
[20] Tomlinson A, Doane MG, McFadyen A. Inputs and outputs of the lacrimal system : review of production and evaporative loss. Ocul Surf 2009 ; 7 : 186-98.
[21] Rolando M, Refojo MF. Tear evaporimeter for measuring water evaporation rate from the tear film under controlled conditions in humans. Exp Eye Res 1983 ; 36 : 25-33.
[22] Craig JP, Singh I, Tomlinson A, et al. The role of tear physiology in ocular surface temperature. Eye (Lond) 2000 ; 14 : 635-41.
[23] Mathers WD. Ocular evaporation in meibomian gland dysfunction and dry eye. Ophthalmology 1993 ; 100 : 347-51.
[24] Kamao T, Yamaguchi M, Kawasaki S, et al. Screening for dry eye with newly developed ocular surface thermographer. Am J Ophthalmol 2011 ; 151 : 782-91e1.
[25] Mori A, Oguchi Y, Okusawa Y, et al. Use of high-speed, high-resolution thermography to evaluate the tear film layer. Am J Ophthalmol 1997 ; 124 : 729-35.
[26] Fukuda M, Wang HF. Dry eye and closed eye tears. Cornea 2000 ; 19 : S44-8.
[27] Glasson MJ, Stapleton F, Keay L, et al. Differences in clinical parameters and tear film of tolerant and intolerant contact lens wearers. Invest Ophthalmol Vis Sci 2003 ; 44 : 5116-24.
[28] Baudouin C, Bourcier T, Brignole F, et al. Correlation between tear IgE levels and HLA-DR expression by conjunctival cells in allergic and nonallergic chronic conjunctivitis. Graefes Arch Clin Exp Ophthalmol 2000 ; 238 : 900-4.
[29] Ng V, Cho P, Mak S, Lee A. Variability of tear protein levels in normal young adults : between-day variation. Graefes Arch Clin Exp Ophthalmol 2000 ; 238 : 892-9.
[30] Batellier L, Rea A, Chaumeil C, Scat Y. Protein evaluation of tears: different biological parameters and their respective value. J Fr Ophtalmol 1996 ; 19 : 520-6.
[31] Reitz C, Breipohl W, Augustin A, Bours J. Analysis of tear proteins by one- and two-dimensional thin-layer iosoelectric focusing, sodium dodecyl sulfate electrophoresis and lectin blotting. Detection of a new component : cystatin C. Graefes Arch Clin Exp Ophthalmol 1998 ; 236 : 894-9.
[32] Van Haeringen NJ. Clinical biochemistry of tears. Surv Ophthalmol 1981 ; 26 : 84-96.
[33] Ohashi Y, Ishida R, Kojima T, et al. Abnormal protein profiles in tears with dry eye syndrome. Am J Ophthalmol 2003 ; 136 : 291-9.
[34] Sen DK, Sarin GS. Immunoassay of human tear lysozyme. Am J Ophthalmol 1980 ; 90 : 715-8.
[35] Batellier L, Rea A, Circaud R, et al. Quantitative determination of lactoferrine and lysozyme in tears by immunonephelemetric assay on Immage 800 (Beckman Coulter). Methodology and clinical interest. IVth International Congress on tear fluid, ISD. Stockholm, 1996.
[36] Da Dalt S, Moncada A, Priori R, et al. The lactoferrin tear test in the diagnosis of Sjogren’s syndrome. Eur J Ophthalmol 1996 ; 6 : 284-6.
[37] Yolton DP, Mende S, Harper A, Softing A. Association of dry eye signs and symptoms with tear lactoferrin concentration. J Am Optom Assoc 1991 ; 62 : 217-23.
[38] Glasson M, Stapleton F, Willcox M. Lipid, lipase and lipocalin differences between tolerant and intolerant contact lens wearers. Curr Eye Res 2002 ; 25 : 227-35.
[39] Tomlinson A, Khanal S, Ramaesh K, et al. Tear film osmolarity : determination of a referent for dry eye diagnosis. Invest Ophthalmol Vis Sci 2006 ; 47 : 4309-15.
[40] Lemp MA, Bron AJ, Baudouin C, et al. Tear osmolarity in the diagnosis and management of dry eye disease. Am J Ophthalmol 2011 ; 151 : 792-8e1.
[41] The definition and classification of dry eye disease : report of the definition and classification subcommittee of the International Dry Eye WorkShop (2007). Ocul Surf 2007 ; 5 : 75-92.
[42] Sullivan BD, Whitmer D, Nichols KK, et al. An objective approach to dry eye disease severity. Invest Ophthalmol Vis Sci 2010 ; 51 : 6125-30.
[43] Versura P, Profazio V, Campos EC. Performance of tear osmolarity compared to previous diagnostic tests for dry eye diseases. Curr Eye Res 2010 ; 35 : 553-64.
[44] Yildiz EH, Fan VC, Banday H, et al. Evaluation of a new tear osmometer for repeatability and accuracy, using 0.5-microL (500-Nanoliter) samples. Cornea 2009 ; 28 : 677-80.
[45] Rolando M. Tear mucus ferming test in normal and keratoconjunctivitis sicca eyes. Chibret Int J Ophthalmol 1984 ; 2 : 32-9.
[46] Ravazzoni L, Ghini C, Macri A, Rolando M. Forecasting of hydrophilic contact lens tolerance by means of tear ferning test. Graefes Arch Clin Exp Ophthalmol 1998 ; 236 : 354-8.
[47] Rolando M, Baldi F, Zingirian M. The effect of hyperosmolarity on tear mucus ferning. Fortschr Ophthalmol 1986 ; 83 : 644-6.
[48] Batellier L, Moens C, Mavier C, et al. Le dosage des IgE totales dans les larmes par la technique ultrasensible « 0-100 » sur l’Immunocap 100 Phadia et son intérêt dans le diagnostic étiologique des atteintes allergiques de la surface oculaire. Immuno-Anal Biol Spec 2008 ; 23 : 89-94.
[49] Mimura T, Usui T, Mori M, et al. Rapid immunochromatographic measurement of specific tear immunoglobulin E in moderate to severe cases of allergic conjunctivitis with Immfast Check J1 in the spring. Cornea 2011 ; 30 : 524-7.
[50] Inada N, Shoji J, Kato H, et al. Clinical evaluation of total IgE in tears of patients with allergic conjunctivitis disease using a novel application of the immunochromatography method. Allergol Int 2009 ; 58 : 585-9.
[51] Stern ME, Pflugfelder SC. Inflammation in dry eye. Ocul Surf 2004 ; 2 : 124-30.
[52] Baudouin C. The pathology of dry eye. Surv Ophthalmol 2001 ; 45 : S211-20.
[53] Zhou L, Beuerman RW, Chan CM, et al. Identification of tear fluid biomarkers in dry eye syndrome using iTRAQ quantitative proteomics. J Proteome Res 2009 ; 8 : 4889-905.
[54] de Souza GA, Godoy LM, Mann M. Identification of 491 proteins in the tear fluid proteome reveals a large number of proteases and protease inhibitors. Genome Biol 2006 ; 7 : R72.
[55] Green-Church KB, Nichols KK, Kleinholz NM, et al. Investigation of the human tear film proteome using multiple proteomic approaches. Mol Vis 2008 ; 14 : 456-70.
[56] Vieira AC, An HJ, Ozcan S, et al. Glycomic analysis of tear and saliva in ocular rosacea patients : the search for a biomarker. Ocul Surf 2012 ; 10 : 184-92.
[57] Pflugfelder SC, Jones D, Ji Z, et al. Altered cytokine balance in the tear fluid and conjunctiva of patients with Sjogren’s syndrome keratoconjunctivitis sicca. Curr Eye Res 1999 ; 19 : 201-11.
[58] Chotikavanich S, de Paiva CS, Li de Q, et al. Production and activity of matrix metalloproteinase-9 on the ocular surface increase in dysfunctional tear syndrome. Invest Ophthalmol Vis Sci 2009 ; 50 : 3203-9.
[59] De Paiva CS, Corrales RM, Villarreal AL, et al. Corticosteroid and doxycycline suppress MMP-9 and inflammatory cytokine expression, MAPK activation in the corneal epithelium in experimental dry eye. Exp Eye Res 2006 ; 83 : 526-35.
[60] Zhao H, Jumblatt JE, Wood TO, Jumblatt MM. Quantification of MUC5AC protein in human tears. Cornea 2001 ; 20 : 873-7.
[61] Garcher C, Bron A, Baudouin C, et al. CA 19-9 ELISA test : a new method for studying mucus changes in tears. Br J Ophthalmol 1998 ; 82 : 88-90.
[62] Wollensak G, Mur E, Mayr A, et al. Effective methods for the investigation of human tear film proteins and lipids. Graefes Arch Clin Exp Ophthalmol 1990 ; 228 : 78-82.
[63] Toker E, Yavuz S, Direskeneli H. Anti-Ro/SSA and anti-La/SSB autoantibodies in the tear fluid of patients with Sjogren’s syndrome. Br J Ophthalmol 2004 ; 88 : 384-7.
[64] Nakamura Y, Sotozono C, Kinoshita S. Inflammatory cytokines in normal human tears. Curr Eye Res 1998 ; 17 : 673-6.
[65] Solomon A, Dursun D, Liu Z, et al. Pro- and anti-inflammatory forms of interleukin-1 in the tear fluid and conjunctiva of patients with dry-eye disease. Invest Ophthalmol Vis Sci 2001 ; 42 : 2283-92.
[66] Virtanen T, Konttinen YT, Honkanen N, et al. Tear fluid plasmin activity of dry eye patients with Sjogren’s syndrome. Acta Ophthalmol Scand 1997 ; 75 : 137-41.
[67] Augustin AJ, Spitznas M, Kaviani N, et al. Oxidative reactions in the tear fluid of patients suffering from dry eyes. Graefes Arch Clin Exp Ophthalmol 1995 ; 233 : 694-8.
P. Goldschmidt, C. Chaumeil
Les infections oculaires peuvent toucher toutes les tuniques de l’œil. En règle générale, les prélèvements de la surface oculaire pour analyse microbiologique sont effectués avant toute antibiothérapie. Les grattages de cornée sont effectués après instillation d’un anesthésique topique sans conservateur qui doit être abondamment rincé avant le prélèvement. Le laboratoire peut mettre en place deux approches : la détection et l’identification des agents pathogènes ; des tests pour identifier la réponse immunitaire.
Les tests utilisant des techniques de biologie moléculaire peuvent être réalisés directement sur les échantillons cliniques. Les modalités de prélèvement dépendent de la localisation ou de l’agent à rechercher :
conjonctivites infectieuses : prélèvement par écouvillonnage ;
conjonctivite folliculaire, trachome et conjonctivite du nouveau-né : prélèvement par grattage de la conjonctive tarsale supérieure ;
conjonctivites et kératoconjonctivites virales : grattage des lésions cornéennes ou par écouvillonnage conjonctival ;
kératites et ulcères de cornée : prélèvement par a) écouvillonnage pour examen direct ; b) écouvillonnage pour cultures ; c) écouvillonnage pour recherche de virus par polymerase chain reaction (PCR) ;
recherche de champignons ou d’acanthamibes : a) grattage profond de cornée pour examen direct et culture ; b) grattage profond avec bistouri pour PCR ;
lentilles de contact, boîtier et liquide de conservation : recherche par culture de bactéries, champignons et protozoaires ;
blépharites : extrusions de glandes enflammées ou grattage des zones affectées pour culture ;
rosacée : grattage des zones affectées ;
Demodex : prélèvement de chaque côté à la pince à épiler d’au moins cinq cils présentant des concrétions sur le bord libre de la paupière (manchons) ;
poux, pédiculoses et morpions oculaires : prélèvement des parasites à la pince à épiler ;
gale ophtalmique : grattage à la curette sur plusieurs sites et recueil de sérosités et squames ;
filarioses : extraction et identification des filaires sous-conjonctivales ;
toxocarose oculaire : dosage d’anticorps dans liquides de ponction de chambre antérieure (PCA) et sérum ; numération formule sanguine (NFS) ;
onchocercose et autres parasitoses : prélèvement des lésions et PCA ; dosage d’anticorps dans le sérum et dans la PCA ; NFS.
masses macroscopiques : biopsie pour examen parasitologique et anatomo-cytopathologique, NFS.
Les infections oculaires touchent toutes les tuniques de l’œil et les annexes et présentent des tableaux cliniques qui vont de la simple conjonctivite (autolimitée) jusqu’à des maladies cécitantes (trachome, kératites fongiques ou amibiennes, etc.).
L’expérience clinique et les résultats du laboratoire spécialisé orientent le choix thérapeutique rationnel. En outre, le laboratoire s’associe aux travaux de surveillance des infections dans la communauté, aux alertes pour les infections nosocomiales, à la détection des épidémies, à la surveillance des agents endémiques multirésistants et à l’identification d’événements émergents.
En règle générale, les prélèvements de la surface oculaire pour analyse microbiologique, effectués avant toute antibiothérapie ou après une fenêtre thérapeutique de plusieurs heures, sont effectués à l’aide d’une lampe à fente ou au bloc opératoire sous microscope parfois après instillation d’un anesthésique topique sans conservateur (prélèvements de cornée) qui doit être rincé abondamment avant le prélèvement.
Les biopsies de cornée sont à envisager pour des lésions inaccessibles au grattage ou lorsque les résultats des grattages ne sont pas concluants.
Les échantillons biologiques de la surface oculaire destinés aux tests microbiologiques doivent être conditionnés selon des procédures validées (lames cerclées pour examens directs, microtubes pour tests de biologie moléculaire, milieux de transport sélectifs pour les isolements microbiens) et acheminés au laboratoire le plus rapidement possible pour être analysés.
La standardisation de procédures d’échantillonnage pour la bactériologie, la mycologie, la parasitologie et la virologie a été possible grâce à l’adaptation d’un kit de prélèvement contenant différents dispositifs de prélèvement adaptés aux besoins spécifiques de la surface oculaire.
Les tests de diagnostic in vitro visent à détecter et à identifier l’agent infectieux (virus, bactérie ou parasite) responsable des signes cliniques. Le laboratoire effectue deux sortes d’approches :
des tests de détection et d’identification des agents pathogènes soit par mise en culture afin de les multiplier et d’augmenter la probabilité de la détection, soit par détection de leur matériel génétique par les tests moléculaires ;
des tests indirects pour identifier la réponse immunitaire à l’infection : quantification du titre d’anticorps dont la présence signe un contact et une réponse humorale vis-à-vis d’un virus, une bactérie ou un parasite.
Les tests de diagnostic basés sur des techniques de biologie moléculaire peuvent être réalisés directement sur les échantillons cliniques et permettent d’obtenir des résultats en quelques heures. Ces tests nécessitent la mise au point et la validation de trois étapes (qui peuvent être automatisées) :
1. l’extraction des acides nucléiques (matériel génétique) à partir de l’échantillon ;
2. l’amplification de séquences génétiques ciblées par des enzymes thermostables ;
3. la détection des copies de séquences amplifiées.
En fonction des différents tableaux cliniques des infections de la surface oculaire, les tests d’aide au diagnostic adaptés aux micro-échantillons sont décrits ci-après.
Des sécrétions purulentes indiquent en général une conjonctivite bactérienne purulente de l’adulte ou de l’enfant et, plus rarement, une kératoconjonctivite gonococcique de l’adulte ou de l’enfant, infection sévère, dont la présentation clinique quasi pathognomonique peut se compliquer rapidement de perforation cornéenne.
Le sujet se plaint de douleurs, de fatigues oculaires, de sensation de sable dans les yeux et a les yeux collés. Chez l’enfant, Haemophilus influenzae, Streptococcus pneumoniae, Staphylococcus aureus ainsi que Moraxella catarrhalis sont le plus souvent en cause. Il existe des variations saisonnières : l’incidence des conjonctivites à pneumocoques est plus fréquente en hiver contrairement à Haemophilus influenzae plus fréquent au printemps et en été [1, 2].
Chez le nouveau-né, les principaux agents à l’origine des conjonctivites purulentes sont Neisseira gonorrhoea et Chlamydia trachomatis. Les conjonctivites folliculaires nécessitent la confirmation par un test recherchant des Chlamydiae. Les conjonctivites virales sont généralement bilatérales, associées à des sécrétions claires, à une conjonctivite folliculaire (hyperplasie lymphocytaire) pouvant évoluer vers une kératite. Elles sont souvent épidémiques et les virus les plus courants sont les adénovirus [2, 3].
L’écouvillonnage conjonctival est pratiqué dans les indications décrites ci-dessous.
Conjonctivite :
aiguë ;
épidémique ;
chronique récidivante.
Suspicion de conjonctivite :
lors d’un bilan préchirurgical ;
bactérienne lors d’un bilan pré-injection intravitréenne.
La présence de nombreuses cellules épithéliales est le critère qui garantit la qualité de l’échantillon conjonctival prélevé.
Les cellules altérées avec images de cytolyse sont le reflet d’une agression tissulaire d’origine infectieuse, inflammatoire non infectieuse ou toxique médicamenteuse.
La présence de cristaux peut être due à un excès de collyres qui précipitent au contact de la surface oculaire ou à des résidus de produits utilisés lors de l’examen clinique (fluorescéine, rose Bengale, etc.).
La présence de polynucléaires neutrophiles est le marqueur biologique d’infection bactérienne, fongique ou à Acanthamœba.
La présence de polynucléaires éosinophiles oriente vers le diagnostic d’un tableau allergique et inflammatoire local ; elle peut révéler aussi une hyperréactivité contre les principes actifs ou les agents conservateurs présents dans des produits utilisés pour les traitements locaux.
La présence de macrophages peut être observée lors d’infections virales, bactériennes ou par acanthamibes.
La présence de lymphocytes oriente vers une infection virale et plus rarement une infection bactérienne à bactéries intracellulaires.
La présence de cellules épithéliales avec des inclusions basophiles périnucléaires (tunique, toge ou chlamyde) suggère une infection par des bactéries à réplication intracellulaire, surtout des Chlamydiae.
L’examen des lames à fort grossissement (× 1000) après coloration peut montrer des formes bactériennes, des levures, des champignons filamenteux, des trophozoïtes ou des kystes de protozoaires.
Lorsque des bactéries sont observées à la coloration de May-Grünwald-Giemsa (MGG), il est recommandé d’effectuer une coloration de Gram sur une autre lame ou sur la même lame après élimination de l’huile d’immersion et décoloration avec de l’alcool à 70°. La coloration de Gram peut orienter l’approche thérapeutique.
Le diagnostic d’infections ophtalmologiques requiert la mise en culture d’échantillons biologiques dans un milieu permettant aux micro-organismes éventuellement présents de se multiplier. Toutefois, pour les ulcères de cornée, l’examen direct prend un rôle déterminant : les résultats de la culture peuvent être limités par la taille des échantillons prélevés de la surface oculaire ainsi que par les prétraitements antimicrobiens, désinfectants ou biocides.
La culture est la clé pour l’identification phénotypique de nombreux micro-organismes et pour déterminer leur sensibilité aux antibiotiques.
Gélose chocolat Isovitalex® pour l’isolement des bactéries aérobies (et de certaines bactéries anaérobies lorsque les géloses sont placées en anaérobiose) et de champignons.
Milieu liquide de Schaedler désoxygéné pour l’isolement de germes micro-aérophiles et anaérobies.
Milieu de Sabouraud avec antibiotiques et sans inhibiteurs pour l’isolement des levures et des champignons filamenteux [2, 5].
Le résultat de la culture bactérienne peut être considéré négatif seulement après 10 jours d’incubation à 37 °C et après 3 semaines à 30 °C pour les champignons.
Si la culture bactérienne est positive : pratiquer les tests de sensibilité aux antibiotiques sur les souches isolées afin d’adapter le traitement en fonction des résultats des concentrations minimales inhibitrices (CMI) [1, 5].
Si la culture fongique est négative : uniquement après 3 semaines d’incubation à 30 °C.
Si la culture fongique est positive :
pratiquer les tests d’identification phénotypique ;
déterminer les CMI des antifongiques (amphotéricine B, voriconazole, caspofungine, posaconazole, 5-fluorocytosine, éconazole, fluconazole, etc.) afin d’adapter le traitement en fonction des profils obtenus (interprétations valables essentiellement pour les infections à levures) [2, 4, 5].
La conjonctivite à inclusions de l’adulte et la conjonctivite du nouveau-né sont une maladie oculogénitale ; le réservoir de germes se situe au niveau du tractus génital de l’adulte. L’affection prend parfois la forme d’un épisode aigu mais il s’agit le plus souvent d’un œil rouge chronique associé à une blépharite, des sécrétions mucopurulentes, une sensation de corps étranger et une photophobie. L’incubation varie de 2 jours à 3 semaines. Elle est dans un premier temps papillaire, unilatérale et peut être associée à une adénopathie prétragienne homolatérale [6].
Le trachome, l’une des premières causes évitables de cécité, est une infection oculaire chronique ou le résultat de réinfections par des sérovars particuliers de Chlamydiae qui atteignent au départ la conjonctive des paupières. Sans traitement l’évolution peut provoquer des lésions cornéennes irréversibles pouvant entraîner la cécité [7, 8].
Procéder au grattage profond de la conjonctive tarsale supérieure avec une spatule de Kimura ou un dispositif équivalent permettant le raclage des cellules de l’épithélium conjonctival (le cycle de réplication des Chlamydiae est intracellulaire).
Après grattage, placer le dispositif de prélèvement avec le matériel obtenu dans un tube sec pour congélation immédiate, puis extraire l’ADN (acide désoxyribonucléique) pour le soumettre à des procédures d’amplification d’acides nucléiques (PCR). Les résultats de PCR seront validés uniquement si l’échantillon est riche en cellules épithéliales [8, 9].
Si la PCR est positive, cela signe la présence du génome de Chlamydiae.
La cornée est un tissu avasculaire. Les lésions cornéennes activent la production de médiateurs de l’inflammation au site de la lésion et la migration des polynucléaires vers la cornée. Lors d’infections microbiennes sévères, la sécrétion locale de médiateurs de l’inflammation induit la formation de néovaisseaux partant du limbe vers le centre de la cornée [10]. Ces néovaisseaux peuvent s’associer à des zones de cicatrices (taies cornéennes opaques) compromettant la fonction visuelle.
Écouvillonnage et étalement du matériel sur deux lames cerclées pour examen au microscope (examen direct).
Écouvillonnage pour cultures microbiennes.
Écouvillonnage pour recherche de virus par PCR.
Grattage profond de cornée avec bistouri pour recherche de protozoaires par PCR.
Grattage profond pour examen direct sur au moins deux lames (recherche de filaments mycéliens) et culture.
La présence de nombreuses cellules épithéliales est un critère qui garantit la qualité de l’échantillon et les cellules altérées indiquent une agression tissulaire d’origine infectieuse, inflammatoire non infectieuse ou toxique médicamenteuse.
La présence de polynucléaires neutrophiles est le marqueur biologique associé à une infection bactérienne, fongique ou à acanthamibes.
La présence de polynucléaires éosinophiles peut indiquer une étiologie allergique qui non traitée peut aboutir à une lésion voire une surinfection ou peut alerter sur une hyperréactivité vis-à-vis des traitements topiques en cours.
La présence d’hématies est l’indicateur de microtraumatismes hémorragiques lors du prélèvement ou d’une néovascularisation cornéenne.
La présence de cristaux peut refléter un excès de collyres précipitants au contact de la surface oculaire.
La présence de lymphocytes oriente vers le diagnostic de kératite d’origine virale.
Lorsque des bactéries sont observées à la coloration de MGG, il est recommandé de pratiquer une coloration de Gram sur une autre lame ou sur la même lame après élimination de l’huile d’immersion et décoloration avec de l’alcool à 70°.
Les filaments mycéliens, pseudo-mycéliens et les kystes de protozoaires seront davantage mis en évidence après une coloration de MGG lente (pH : 7,4) et confirmés par la coloration de Grocott [1, 11].
La kératite se manifeste par des douleurs oculaires, des larmoiements, un blépharospasme et généralement une photophobie avec une baisse de l’acuité visuelle [12].
La kératite bactérienne est la plupart du temps associée à un traumatisme mineur de la cornée, très souvent lié au port de lentilles de contact [4, 11].
Examen direct après étalements sur lames.
Cultures microbiennes (voir plus haut Conjonctivite).
Test de sensibilité aux antibiotiques sur les souches isolées.
Test de sensibilité aux antifongiques sur les souches isolées.
Infiltrats stromales résistants aux antibiothérapies à large spectre dans un contexte de traumatisme par un corps étranger, de port de lentilles de contact, chez les sujets greffés ou après des traitements immunosuppresseurs.
Le test à la fluorescéine peut être négatif si l’épithélium se reforme, l’infection se développant alors en profondeur [13, 14].
Bien rincer la cornée avec une solution saline isotonique stérile, puis effectuer le prélèvement profond, après vérification de l’épaisseur cornéenne, par grattage au niveau des infiltrats et de leurs périphéries [1, 15–17].
Le grattage cornéen doit être profond, avec scalpel inoxydable stérile (jamais avec un écouvillon en coton).
Étalement fin d’une aliquote du matériel sur les lames pour l’examen direct.
Mise en culture d’une aliquote du matériel prélevé dans les milieux spécifiques [18, 19].
Déterminer les CMI des antifongiques (amphotéricine B, voriconazole, caspofungine, posaconazole, 5-fluorocytosine, éconazole, fluconazole, etc.) afin d’adapter le traitement en fonction des profils obtenus (interprétations valables essentiellement pour les infections à levures) [2, 4, 5].
Les kératomycoses à microsporidies débutantes peuvent ressembler aux kératites herpétiques et se compliquer de précipités kératiques et d’infiltrats profonds au niveau du stroma et d’un œdème [20].
La contamination par microsporidies se produit par ingestion, inhalation, contact direct (souillure de la conjonctive), contact avec des animaux et transmission interhumaine. Les microsporidies perforent la cellule hôte en inoculant le sporoplasme infectieux [21, 22].
La technique diagnostique de référence est la PCR.
L’examen direct (voir plus loin procédures kératites) peut permettre de déceler des images de microsporidies sur les grattages profonds de cornée. Ces images peuvent être mises en évidence par des composés fluorescents (fluorochromes intercalants) et moins facilement après coloration de MGG. La spore apparaît entourée par une membrane plasmique ainsi que par deux parois extracellulaires rigides.
Les microsporidies peuvent être isolées par culture à partir de prélèvements cornéens et conjonctivaux (grattages cornéens profonds) et sur des biopsies.
L’isolement des microsporidies par culture permet de déterminer les CMI des antifongiques (amphotéricine B, voriconazole, caspofungine, 5-fluorocytosine, éconazole, fluconazole) [23, 24].
La mise évidence des microsporidies par PCR est la technique la plus sensible.
Dans les pays industrialisés, la KA est presque toujours associée à l’utilisation de lentilles de contact, les acanthamibes pouvant adhérer et survivre sur les lentilles et dans les boîtiers, ce qui facilite leur contact direct avec la cornée lors du port de lentilles contaminées.
Dans les pays non industrialisés, la KA survient dans près de 50 % sur des yeux sans notion de port de lentilles mais après un traumatisme ; la chaleur et une faible hygrométrie associée à des vents chargés de poussière semblent la favoriser [25–27].
Le sujet atteint de KA présente une hyperhémie conjonctivale accompagnée d’une douleur oculaire et d’une photophobie. D’autres étiologies infectieuses le plus souvent d’origine herpétique, mycosique ou bactérienne sont en général évoquées en première intention [28]. Toutefois, l’observation d’une kératonévrite radiaire et la douleur très intense avec un œdème cornéen associé à un ou plusieurs infiltrats dans le stroma périlésionnel sont des signaux d’appel. À un stade plus tardif, la douleur peut être absente tandis que les infiltrats s’étendent dans le stroma [29].
Le diagnostic de KA est posé par la mise en évidence sur des grattages cornéens de trophozoïtes ou de kystes d’Acanthamœba (par examen direct ou par culture, ou par la détection de l’ADN spécifique par PCR).
Le prélèvement cornéen est effectué après vérification de l’épaisseur cornéenne, par grattage profond avec une lame de bistouri en périphérie de la lésion ou au niveau des infiltrats et de leurs périphéries (voir plus loin kératomycoses).
Des collyres utilisés pour l’examen ophtalmologique (fluorescéine, oxybuprocaïne) et les molécules biocides inhibent les techniques de PCR [30]. Afin d’éviter des résultats faussement négatifs de PCR, il est recommandé de rincer abondamment la surface de l’œil avec du NaCl 0,9 % stérile avant d’effectuer le prélèvement de cornée et de débuter tout traitement amœbicide. Afin d’optimiser les techniques de biologie moléculaire (PCR) et sachant que les prélèvements cornéens contiennent principalement des kystes, les méthodes d’extraction de l’ADN devront lyser en totalité la structure rigide des kystes et libérer l’ADN des protozoaires pour son amplification ultérieure [31].
Une réaction inflammatoire locale à macrophages et polynucléaires peut être observée. Les kystes d’Acanthamœba spp. présentent une double paroi après coloration au MGG, mais la pénétration intrakystique des colorants est variable suivant l’état de maturation de la double paroi (bleu plus ou moins clair à incolore). Des images peuvent parfois évoquer d’autres protozoaires retrouvés dans l’eau tels Hartmanella, Volkampfia, Naegleria, Balamuthia, Sappinia, etc.
La PCR en temps réel effectuée directement sur les prélèvements cornéens est l’examen le plus sensible et le plus spécifique pour le diagnostic de KA (> 90 % de sensibilité) [32, 33].
La HRM (high-resolution melting) real-time PCR permet la détection de toutes les espèces d’Acanthamœba et leur classification en quatre groupes sans procédures de post-amplification et sans l’utilisation de sondes radioactives ou fluorogéniques [34, 35].
Si la PCR est positive, cela signe la présence de génomes d’Acanthamœba spp. dans le grattage cornéen.
Recueillir le liquide contenu dans le boîtier, écouvillonner les parois de celui-ci et décharger l’écouvillon dans le liquide. Centrifuger le liquide et analyser le culot de centrifugation.
Culture bactérienne et fongique.
Culture de protozoaires :
le culot est déchargé sur une gélose à base d’agar pauvre avec une goutte de suspension d’Escherichia coli (ou Enterobacter aerogenes ou Pseudomonas), bactéries vivantes ou tuées, ou mieux, mises en culture en petits flacons pour culture cellulaire dans 5 ml de NaCl 0,9 %, ensemencé avec une goutte de suspension d’Escherichia coli ;
l’incubation a lieu pendant 21 jours à 30 °C. La lecture journalière des cultures en flacon ou en boîte se fait au microscope inversé (× 100 ou × 200). Si des protozoaires sont présents, ils vont ingérer les bactéries comme nutriment et se multiplier ;
la PCR peut également être utilisée comme outil de confirmation [27, 29].
La culture et l’examen microscopique sont des méthodes peu sensibles pour le diagnostic des KA (de 30 à 60 % de sensibilité), en particulier lorsque les patients ont reçu préalablement des traitements par des antibiotiques ayant une activité plus ou moins amœbicide [32, 34].
Les résultats des cultures de protozoaires positives des lentilles de contact, boîtiers et liquides de conservation doivent être pris en compte uniquement s’ils sont associés à des signes évocateurs. En effet, 5 à 20 % des boîtiers de porteurs de lentilles de contact asymptomatiques sont contaminés, le pouvoir prédictif positif de cet examen est donc limité. En revanche, à partir de grattages de lésions cornéennes, l’isolement d’Acanthamœba ou la PCR positive confirment le diagnostic [1, 33, 34].
Les kératoconjonctivites virales se caractérisent par des sécrétions claires (les sécrétions mucoïdes sont associées aux conjonctivites bactériennes, aux conjonctivites allergiques ainsi qu’aux cas graves de déficit lacrymal). Des adénopathies pré-auriculaires sont typiques des conjonctivites adénovirales ou à Pasteurella (syndrome de Parinaud), alors qu’elles sont le plus souvent absentes en cas d’atteinte bactérienne.
La kératoconjonctivite épidémique à adénovirus présente un début brutal avec une hyperhémie conjonctivale prononcée et une atteinte cornéenne précoce. Le plus souvent, la kératoconjonctivite adénovirale, associée à la formation de fausses membranes au niveau de la conjonctive palpébrale, peut induire la formation de fines ponctuations cornéennes superficielles captant la fluorescéine [36]. Ces ponctuations deviennent plus profondes et forment des opacités sous-épithéliales, ce qui peut entraîner une photophobie et une baisse de vision parfois irréversible [37].
La mise en évidence des virus par isolement sur culture de cellules permissives est de sensibilité discutable et relativement laborieuse. Les performances diagnostiques peuvent être améliorées en ajoutant à la culture un marquage par immunofluorescence ou par des techniques immuno-enzymatiques des cellules infectées.
La mise en évidence du génome viral amplifié par PCR est devenue la méthode de choix pour les prélèvements oculaires car la sensibilité des techniques d’amplification d’acides nucléiques est largement supérieure à celle de la culture, avec une spécificité de 100 % [37, 38].
Type d’échantillon : écouvillonnage ou grattage conjonctival.
Grattage de la conjonctive tarsale supérieure et inférieure et recueil de larmes, de fausses membranes et de sécrétions avec un dispositif en Dacron ou un écouvillon en coton. Le matériel est déchargé dans un tube sec et congelé immédiatement pour les procédures de PCR.
Si l’aspect de la conjonctivite est hémorragique (notamment en été au décours d’un voyage ou avec la notion de baignade en piscine), une infection par entérovirus peut être suspectée (entérovirus 70 associé à la conjonctivite hémorragique dite « Apollo »).
Les signes apparaissent dans un contexte épidémique en été et à l’automne avec des paupières qui gonflent rapidement, des hémorragies sous-conjonctivales ou une kératite, provoquant une douleur, des larmoiements et une photophobie. La forme généralisée est rare, bien que quelques cas de radiculomyélopathie lombosacrée transitoire ou de syndromes proches de la poliomyélite aient été observés lors de conjonctivites hémorragiques dues à l’entérovirus 70. Les entérovirus (ARN virus) 68-71 et 73, les poliovirus de type 1-3, les virus coxsackie A1-A22, A24 et B1-6, les échovirus 2-9, 11-21, 24-27 et 29-33 (entériques cytopathiques humains orphelins), qui sont excrétés par les sécrétions buccales, les selles, le sang et sont présents dans le liquide céphalorachidien (LCR), peuvent provoquer des signes ophtalmologiques. Le diagnostic est surtout clinique [38].
Le diagnostic biologique peut être établi par culture du virus, après rétrotranscription de l’ARN (acide ribonucléique) viral en ADN et amplification des fragments rétrotranscrits par PCR (reverse transcription polymerase chain reaction ou RT-PCR) ou par la mise en évidence d’une séroconversion [38, 39].
Type d’échantillon : écouvillonnage ou grattage conjonctival.
Grattage de la conjonctive tarsale supérieure et inférieure et recueil de larmes, de fausses membranes et de sécrétions avec un dispositif en Dacron ou un écouvillon en coton. Le matériel est déchargé dans un tube sec et congelé immédiatement pour rétrotranscription et amplification d’acides nucléiques (PCR).
Les PCR positives ou négatives doivent être validées par la présence de cellules épithéliales (qualité de l’échantillon) et par des contrôles internes d’extraction et de rétrotranscription des ARN, et de l’élimination des inhibiteurs de la PCR.
Herpes simplex virus (HSV) type 1 et type 2 sont responsables d’atteintes oculaires ayant tendance à récidiver : blépharite vésiculaire, conjonctivite, kératite et uvéite. Ils peuvent atteindre les couches profondes de la cornée et provoquer un œdème, accompagné ou non de nécrose tissulaire. Les lésions stromales inflammatoires peuvent laisser des cicatrices engageant la fonction visuelle [1, 3, 40].
Suivant le délai de prélèvement par rapport au début de l’apparition des lésions, le diagnostic peut être effectué par la mise en évidence du virus par culture, par la mise en évidence d’antigènes viraux au moyen d’anticorps monoclonaux conjugués (immunofluorescence ou immunopéroxydase) et parfois par la détection d’anticorps spécifiques dans les larmes. Suivant les présentations cliniques, les herpèsvirus (HSV-1, HSV-2 et varicella-zoster virus ou VZV) peuvent être mis en évidence dans les frottis de lésions, le liquide de vésicules, les croûtes et la peau.
La détection du génome viral après grattage des lésions par amplification génique par une PCR spécifique est la technique la plus sensible, et elle permet la quantification de la charge virale [36, 40].
À la phase prodromique avant l’apparition de l’éruption, le sujet peut présenter un malaise, une douleur et une fébricule. Les macules érythémateuses se transforment en papules et vésicules avec évolution ultérieure en lésions croûteuses. Les lésions dans le dermatome du nerf nasociliaire peuvent indiquer des complications ophtalmologiques sans relation avec l’âge ni la sévérité de l’atteinte cutanée.
Le zona ophtalmique est la conséquence d’une réactivation virale qui peut atteindre l’œil par les branches V1 ou V2 (20 % des cas) du trijumeau. L’atteinte du rameau supra-orbital conduit à une atteinte de la paupière supérieure, celle du rameau lacrymal, à une xérophtalmie et celle de la branche nasociliaire à un risque particulièrement élevé d’atteinte oculaire. Des complications au décours d’atteintes oculaires s’observent dans plus de 50 % des cas, surtout si le traitement antiviral efficace est retardé [41].
Le zona ophtalmique chez les sujets âgés ou immunodéprimés peut compromettre leur fonction visuelle.
L’infection des cellules de la peau et des muqueuses par des papillomavirus humains a été largement prouvée pour les verrues (papillomatoses acanthotiques et hyperkératosiques) [43, 44]. Toutefois, pour le ptérygion (néoformation conjonctivale se présentant sous forme d’un repli de la conjonctive qui empiète sur la cornée, qui l’envahit, finissant par cacher l’axe visuel et provoquant donc une baisse de la vision) l’association avec les Papillomaviridae et le ptérygion reste controversée [43].
Les papillomes conjonctivaux juvéniles et de l’adulte sont associés à l’infection des cellules épithéliales par les papillomavirus de type 6, 11, 16 qui peuvent déclencher la prolifération cellulaire ou envahir la tumeur secondairement.
Une infection par les Papillomaviridae de types 6 et 11 a pu être démontrée pour les tumeurs épithéliales bénignes de la conjonctive ou en cas d’hyperplasie adénomateuse, pseudo-épithéliomateuse ou pseudo-carcinomateuse.
Molluscum contagiosum est une infection virale provoquée par des poxvirus et transmise par un contact direct avec une peau contaminée qui provoque des petites élévations cutanées globuleuses et pédiculées, siégeant sur la paupière ou la marge palpébrale. L’infection virale induit la formation de petites papules hémisphériques de couleur de la peau normale, blanc nacré, fermes à la palpation. Certaines papules présentent une ombilication cupuliforme en leur centre, légèrement ombiliquées d’aspect charnu qui varie en taille de 2 à 5 mm de diamètre. Elles sont fréquentes chez l’enfant atopique et peuvent être nombreuses et volumineuses chez les sujets immunodéprimés.
Les circonstances de contamination sont retrouvées à la garderie ou à l’école, lors de la fréquentation de piscines publiques, lors de bains collectifs et aussi au cours de sports de contact (promiscuité et peaux en contact). L’utilisation d’objets ayant été en contact avec le virus (comme des serviettes de toilette) peut transmettre l’infection. La période d’incubation peut aller de 2 semaines à 6 mois et les récidives sont fréquentes [47, 48].
Cette infection peut s’accompagner d’une kératite et/ou d’une conjonctivite qui régresse après traitement par ablation de la lésion à la curette [1, 45, 46].
Devant une lésion conjonctivale, la biopsie ou la biopsie exérèse avec examen histologique est le seul moyen d’obtenir un diagnostic de certitude. Toutefois, l’échantillonnage par curetage est difficile à conduire au bord libre des paupières au contact immédiat du globe et de la cornée, ce qui implique une anesthésie générale pour le curetage et les prélèvements chez les jeunes enfants. Le prélèvement doit être rapidement conditionné soit par fixation, soit par congélation permettant la conservation de la morphologie des tissus.
Les résultats des tests d’amplification moléculaire doivent être nuancés sachant que des génomes de papillomavirus peuvent parfois être détectés par PCR dans des tissus cliniquement non affectés.
Certaines infections virales peuvent provoquer des signes à tous les étages de l’arbre respiratoire ainsi qu’à la surface oculaire. Elles sont provoquées surtout par : les paramyxovirus (virus de la rougeole) ; les virus Parainfluenza 1, 2, 3 et 4 ; le virus de la maladie de Newcastle ; le virus respiratoire syncytial ; les métapneumovirus ; le Myxovirus parotidis ; les togavirus (rubéole) ; les Flavivirus (fièvre jaune, West-Nile, encephalite japonaise, dengue) ; les arénavirus (fièvre de Lassa, fièvre hémorragique d’Argentine, fièvre hémorragique de Bolivie, fièvre hémorragique du Brésil, fièvre hémorragique du Venezuela) ; les filovirus (fièvre hémorragique africaine, fièvre hémorragique Ebola) ; les virus Influenza et les rhinovirus (agent du rhume dit banal) [1].
Le diagnostic est essentiellement clinique.
Dans un contexte épidémique, certains laboratoires spécialisés et les centres nationaux de référence disposent de techniques pour confirmer le diagnostic par isolement viral sur des cultures de cellules réceptrices, par PCR pour les virus à ADN ou par la RT-PCR pour les virus à ARN. Les preuves sérologiques peuvent confirmer l’infection a posteriori.
Les angiosarcomes conjonctivaux (sarcome de Kaposi) sont des tumeurs vasculaires d’aspect bleu-rouge retrouvées surtout au niveau des extrémités et au niveau conjonctival. Le virus herpès de type 8 (HHV-8) s’associe au déclenchement d’un processus de prolifération cellulaire qui se traduit par des lésions érythémateuses, puis violacées. L’atteinte muqueuse buccopharyngienne, anogénitale ou oculaire est observée dans plus de 50 % des cas.
Les résultats de PCR sont obtenus à partir des biopsies de lésions. Ils nécessitent une validation par des contrôles par PCR effectuées sur prélèvements du même sujet, dans des tissus voisins sans lésions apparentes, ou par détermination de la charge virale dans la lésion [1, 48].
La canaliculite est une des infections des voies lacrymales caractérisée par des larmoiements chroniques purulents. Elle est le plus souvent provoquée par des bactéries qui contaminent les voies lacrymales par voie rétrograde à partir des voies aériennes supérieures. Les sujets se présentent avec un canalicule dilaté, rouge et douloureux. Le traitement vise à retirer les concrétions et à éviter des récidives. La technique par curetage est efficace dans la plupart des cas et permet de conserver l’intégrité des voies lacrymales, elle peut nécessiter un traitement antibiotique spécifique [4, 46, 49].
Les stratégies thérapeutiques (topiques ou par voie générale) nécessitent un diagnostic clinique différentiel entre canaliculite et conjonctivite purulente. Les germes le plus fréquemment isolés sont les bactéries Actynomyces, Propionibacterium, Fusobacterium et Haemophilus, ainsi que plus rarement des levures.
La dacryocystite est une inflammation du sac lacrymal (dysfonctionnement des voies lacrymales dû à une sténose) qui survient essentiellement aux âges extrêmes : chez les nouveau-nés et les personnes âgées de plus de 70 ans. Les sujets atteints de dacryocystite présentent une douleur, une rougeur et une tuméfaction de l’angle interne de la paupière inférieure par obstruction des voies lacrymales [1, 4]. Chez les personnes âgées, la sténose des canaux lacrymaux et la diminution de la perméabilité des canaux empêchent l’élimination des larmes. Ainsi, des composants des larmes peuvent sédimenter (dacryolithiase), ce qui entraîne une obstruction des voies lacrymales qui peut se surinfecter. Un larmoiement chronique est caractéristique, suivi d’une infection puis d’un abcès du sac lacrymal avec tuméfaction rouge et douloureuse à l’angle interne de l’œil. Lorsqu’une pression sur cette zone est exécrée un reflux de pus apparaît au niveau des points lacrymaux. La complication majeure est la cellulite orbitaire qui se produit lorsque l’infection se propage au-delà du septum [1, 49, 50].
Dans la majorité de cas, le diagnostic est clinique. La mise en culture des prélèvements du canal lacrymonasal et les tests de sensibilité aux antibiotiques (ou aux antifongiques) permettent d’orienter le choix thérapeutique. Les germes le plus fréquemment rencontrés dans les sécrétions purulentes ou les grattages sont les staphylocoques, les streptocoques, les corynébactéries et Actynomyces [50–52].
La culture permet l’identification de micro-organismes et l’étude de leur sensibilité aux antibiotiques ou antifongiques.
Les infections cutanées peuvent se manifester sur le tissu des paupières : HSV, VZV, Molluscum contagiosum, papillomavirus, impétigo provoqué par des staphylocoques, érysipèle provoqué par des streptocoques bêta-hémolytique et plus rarement par Staphylococcus aureus, etc.
La cellulite est une infection des paupières qui débute par des démangeaisons et des brûlures avec un œdème tendre, chaud et rouge [4, 55, 56]. Les présentations variées doivent être différenciées selon la nature des lésions et les structures anatomiques atteintes. Le début de la dermohypodermite bactérienne (DHB), de la DHB nécrosante ou de la fasciite nécrosante (FN) est souvent brutal, associant des signes généraux (fièvre, frissons) et des signes locaux (placard inflammatoire parfois bulleux ou purpurique mais sans nécrose). Une adénopathie satellite sensible peut être observée dans 46 % des cas et une lymphangite dans 26 % des cas.
Chez l’enfant, la cellulite orbitaire peut être liée à une sinusite, avec généralement les mêmes germes que ceux isolés au cours des sinusites. Le diagnostic repose essentiellement sur l’examen clinique et l’imagerie ; le retard au diagnostic et l’attente d’une antibiothérapie adaptée peuvent expliquer pour partie un certain nombre d’évolutions défavorables.
La gravité initiale de l’état septique, l’âge et une pathologie sous-jacente sont des facteurs de risque de mortalité. La précocité de la prise en charge dans les premières heures est un déterminant majeur du pronostic [56, 57].
La culture des sécrétions (collections de pus) suivie des tests de sensibilité aux antibiotiques (ou aux antifongiques) peut orienter les choix thérapeutiques. Pour les cellulites rétroseptales, le traitement peut nécessiter une hospitalisation avec une bi-antibiothérapie par voie générale, active sur des bactéries aérobies et anaérobies. Pour les cellulites d’origine fongique, le traitement est basé sur un drainage et des antimycotiques adaptés aux profils de sensibilité des souches isolées [19, 48, 52, 57, 58].
Chaque paupière comporte 15 à 25 glandes de Meibomius, avec un orifice sur le bord libre de la paupière. Elles sécrètent un mucus abondant qui participe à la formation du film lacrymal. Le bord des paupières est colonisé par de multiples bactéries, principalement Staphylococcus à coagulase négative, Staphylococcus aureus et rarement des bactéries à Gram négatif [59]. Les blépharites sont des infections du bord libre des paupières et se distinguent de la forme focalisée (orgelets, chalazions) [60].
Généralement, les blépharites sont classées de façon anatomique : la blépharite antérieure affecte le bord libre, la blépharite postérieure est associée à l’obstruction ou à l’inflammation des glandes de Meibomius. Les deux types peuvent être tant infectieux qu’inflammatoires et la présence simultanée d’une inflammation antérieure et postérieure est habituelle. La blépharite staphylococcique est caractérisée par la présence de croûtes sur le bord libre, une perte des cils et une hyperhémie conjonctivale chronique. Des lésions peuvent apparaître sur la cornée [1, 4, 60].
Examen direct et culture microbienne. Les causes infectieuses de blépharite sont surtout bactériennes (Staphylococcus spp. principalement, puis Streptococcus spp., corynébactéries, plus rarement Mycobacterium spp. et Treponema pallidum) et sont parfois associées à la présence d’ectoparasites (Demodex). Chez l’immunodéprimé, elle peut être provoquée par Candida albicans, Pityrosporum ovale et par des virus (Molluscum contagiosum, herpèsvirus) [59, 60].
La culture et les tests de sensibilité aux antibiotiques et antifongiques peuvent orienter le choix thérapeutique.
La rosacée est caractérisée par une rougeur de la peau du visage souvent accompagnée de vésicules purulentes. Elle est plus communément observée chez les personnes à la peau claire et sa forme chronique est liée à une dilatation excessive des vaisseaux qui s’accompagne souvent de parakératose séborrhéique, eczéma ou psoriasis [61].
La rosacée oculaire est une complication de la rosacée qui peut associer une kératoconjonctivite à une blépharite. Les symptômes ophtalmologiques sont variés : déficit lacrymal, prurit, brûlures, irritation, rougeur oculaire, photophobie et vision trouble. La flore bactérienne retrouvée est composée principalement de Staphylococcus epidermidis, de Propionibacterium acnes, de Corynebacterium spp. et de Staphylococcus aureus [62]. La blépharite au cours de la rosacée oculaire augmente les risques d’infection (endophtalmie) lors des interventions chirurgicales oculaires.
Les Demodex sont des acariens vermiformes et lipophiles pourvus d’un abdomen strié. Situés au pôle d’insertion du cil, ils sont accrochés plus ou moins perpendiculairement. Les adultes possèdent quatre paires de pattes insérées à leur extrémité antérieure. Ils sont localisés au niveau des follicules pilosébacés où ils se nourrissent du sébum et où ils effectuent l’ensemble de leur cycle [64].
Demodex folliculorum est associé aux blépharites chroniques et à la rosacée lorsqu’il est abondant. Les Demodex peuvent transporter des bactéries (Staphylococcus aureus, Bacillus oleronius, etc.) et pérenniser des réactions inflammatoires, généralement récurrentes et insensibles aux traitements antibactériens classiques. Ils perturbent le fonctionnement des glandes de Meibomius et de Zeiss, altérant l’humidification de la cornée et entraînant des réactions d’hyperkératinisation et d’hyperplasie épithéliale.
La régression des manifestations cliniques sous traitement demeure, in fine, le meilleur argument de l’implication de Demodex dans ces symptomatologies [64, 65].
Au cours de la blépharite associée au Demodex, le signe le plus caractéristique et le plus constant est la présence de manchons de 1 à 2 mm (transparents, blanchâtres ou jaunâtres) à la base des cils [66].
Demodex brevis mesure de 70 à 210 µm et Demodex folliculorum de 280 à 300 µm ; ce dernier se retrouve dans le follicule ciliaire, tandis que Demodex brevis creuse plus profond dans la glande sébacée [67].
Devant une blépharite chronique, Demodex folliculorum doit être recherché par un examen microscopique direct des cils présentant des concrétions sur le bord libre de la paupière (après prélèvement à la pince à épiler). Il est usuel de prélever au moins cinq cils de chaque côté en ciblant les manchons et de les observer très rapidement au microscope entre lame et lamelle dans une goutte de sérum physiologique (objectif × 10). La présence de plus de trois Demodex par cil ou de dix pour cinq cils est considérée comme significative [1, 68].
Il existe trois espèces de poux : Pediculus humanus var capitis ou pou de tête, Phtirus pubis ou morpion et Pediculus humanus var corporis ou pou du corps. Les poux sont des parasites hématophages de l’humain, et leur cycle de multiplication va de deux (morpions) à trois (poux de tête) par semaine. Les morsures des poux occasionnent un prurit et leurs sécrétions peuvent provoquer des réactions allergiques.
La pédiculose est une infestation transmissible et généralement bénigne, cependant les poux de corps peuvent être vecteurs du typhus exanthématique à Rickettsia prowazekii, de la fièvre des tranchées à Bartonella quintana et de la fièvre récurrente due à Borrelia recurrentis.
Les Phtirius inguinalis montrent une avidité pour les poils pubiens mais peuvent également se retrouver accrochés aux cils [68, 69]. Leur transmission non sexuelle est peu fréquente et peut se faire par contact simple avec une personne infectée ou avec des objets (vêtements, linge) car ils peuvent survivre en dehors de l’hôte humain pendant 24 heures.
L’ectoparasitose provoquée par Phtirius inguinalis se rencontre surtout chez l’adulte ; chez l’enfant, la localisation ciliaire signifie une contamination au contact d’un adulte porteur de pédiculose pubienne [69].
La technique la plus utilisée est l’observation des cils (et sourcils) et nécessite le prélèvement des parasites à la pince à épiler suivi d’une observation rapide entre lame et lamelle dans une goutte de sérum physiologique au microscope (objectif × 10). Les poux mesurent de 1 à 4 mm, sont aplatis dorsoventralement et munis de trois paires de pattes terminées par des griffes [69].
Tableau 2-8 Pédiculoses.
Sarcoptes scabiei parasite des millions d’individus surtout dans les régions où les conditions d’hygiène sont mauvaises et survient par épidémies cycliques, notamment dans les foyers de personnes âgées ou chez des sujets atteints de troubles sociopsychologiques [64]. La période d’incubation est de 2 à 3 semaines, puis un prurit intense à recrudescence nocturne apparaît. Les lésions spécifiques peuvent être difficiles à observer (particulièrement chez des sujets ayant une bonne hygiène corporelle) et des lésions secondaires et de surinfection (impétigo) peuvent apparaître. Le visage, le cuir chevelu, les paupières, le cou et le haut du dos sont moins atteints que les extrémités [65, 68, 70].
Le grattage à la curette sur plusieurs sites permet le recueil de sérosités et de squames et la mise en évidence du parasite dans les squames. Les sarcoptes adultes, les larves et des œufs peuvent être observés à l’examen microscopique entre lame et lamelle. La négativité de cet examen n’élimine pas formellement le diagnostic qui doit figurer parmi les diagnostics différentiels de toute affection prurigineuse persistante des paupières [1, 64, 65, 68, 70].
Cette filariose est provoquée par le nématode loa-loa ; on l’appelle également loase ou ver africain de l’œil. Elle est fréquente dans les forêts tropicales d’Afrique de l’Ouest et d’Afrique centrale.
Les humains la contractent à la suite de la piqûre de mouches. La filaire adulte vit à l’intérieur des tissus sous-cutanés, les microfilaires (vers au stade embryonnaire) sont présentes dans la circulation sanguine avec une prédominance entre 12 et 14 heures. Les patients sont souvent asymptomatiques et peuvent présenter un œdème prurigineux fugace et migrateur des extrémités, en particulier des membres supérieurs ou de la face. Ces signes sont déclenchés par le passage du ver sous la peau ou sous la conjonctive, qui fait apparaître un fin cordon rose et mobile, à peine douloureux mais parfois avec une sensation de brûlure. Les complications cardiaques (endocardite) et rénales (protéinurie isolée peu sévère) sont rares [71].
L’identification des vers adultes est possible par examen à la loupe binoculaire après prélèvement lors du passage sous-conjonctival. Les microfilaires de loa-loa se caractérisent par leur taille (250–300 µ), une gaine difficilement colorée au MGG, des noyaux allongés plaqués sous la cuticule et un dernier noyau allongé en position terminale plus ou moins recouvert par les noyaux [72]. Le passage de la filaire adulte sous la conjonctive bulbaire ou palpébrale permet souvent de l’extraire.
La NFS avec un prélèvement entre 10 et 15 h permet, outre la recherche d’une hyperéosinophilie, la recherche de microfilaires sur un frottis mince coloré au MGG. L’absence de microfilaires se confirme par une technique de concentration [72]. L’EDTA (acide éthylène-diamine-tétra-acétique) ou le citrate utilisés comme anticoagulants permettent de garder les microfilaires vivantes plusieurs jours et la détection de l’antigène, en utilisant un test immunologique pour doser les antigènes filariens circulants, constitue une approche diagnostique utile.
L’observation de microfilaires de loa-loa et l’évaluation de la microfilarémie, par méthode de la goutte épaisse calibrée, leucoconcentration, concentration après hémolyse ou cytocentrifugation, permettent d’établir le protocole thérapeutique. En effet, si la microfilarémie est supérieure ou égale à 25 microfilaires par microlitre de sang, le traitement intempestif par l’ivermectine peut entraîner des complications neurologiques graves parfois mortelles (encéphalite) dues aux réactions anaphylactiques liées à la mort des microfilaires (d’où l’exigence de quantifier la microfilarémie avant d’initier toute thérapeutique) [73].
La détection des anticorps a une valeur limitée ; il existe des réactions antigéniques croisées entre les filaires et d’autres helminthes, et un test sérologique positif ne permet pas la distinction entre l’infection passée et celle en cours.
La toxocarose est une zoonose parasitaire cosmopolite due à la contamination humaine par ingestion d’œufs embryonnés d’Ascaris d’animaux présents dans la terre (géophagie), l’eau ou des aliments contaminés par les déjections d’Ascaris de chiens (Toxocara canis), de chats (Toxocara cati) ou par des larves de nématodes d’animaux sauvages. Ces larves en situation d’impasse parasitaire semblent avoir un tropisme sélectif pour les tissus du cerveau et de l’œil. Les jeunes enfants sont souvent infectés dans les bacs à sable ou par contact avec un chiot ou un chat [74–76].
Chez les adultes, l’infestation est souvent associée à des activités agricoles ou de jardinage. La toxocarose est le résultat de la migration intra-oculaire d’une larve (Larva migrans) révélée par une baisse de l’acuité visuelle de l’œil atteint. Les formes mineures de la toxocarose peuvent être asymptomatiques, cependant après une hyperéosinophilie transitoire peuvent être observés des signes cliniques dépendant de la localisation des larves, une asthénie, un prurit isolé ou éruptions prurigineuses, des douleurs de l’hypocondre droit. Les formes majeures comprennent le syndrome de Larva migrans viscérale, la toxocarose oculaire et la toxocarose neurologique qui peut se traduire par des signes d’épilepsie, une méningo-encéphalite, une myélite, une encéphalopathie, une méningoradiculite ou une méningomyélite [74].
Le traitement systématique des animaux domestiques par des antiparasitaires et l’interdiction absolue des chiens et chats dans les bacs à sable ont eu un impact notable sur le nombre de nouveau cas [75, 77].
Le diagnostic de la toxocarose peut s’appuyer sur l’hyperéosinophilie, l’élévation des IgE (taux supérieur à 150 UI/ml) et le dosage des IgG et IgM spécifiques (réactions croisées avec les Ascaris) [76]. La présence de polynucléaires éosinophiles dans les liquides intra-oculaires peut orienter le diagnostic, alors que l’hyperéosinophilie sanguine peut être absente et la sérologie négative chez des sujets atteints de toxocarose oculaire. Le diagnostic peut se confirmer par une PCR et par la quantification d’anticorps spécifiques sécrétés dans l’humeur aqueuse ou le vitré par rapport aux titres dans le sérum [77].
Dans la toxocarose neurologique, le diagnostic repose sur l’hyperéosinophilie (rachidienne) associée à l’immunodiagnostic positif dans le LCR ou l’éventuelle découverte d’une larve dans le LCR à l’examen direct ou par PCR [78, 79].
Les myases ophtalmiques sont des maladies liées à la présence de larves de mouches Œstrus ovis qui parasitent les cavités des sinus frontaux de moutons et de chèvres. Elles touchent surtout les populations rurales et se manifestent au début sous une forme similaire à une conjonctivite. Les ophtalmomyiases humaines sont le plus souvent estivales et plutôt accidentelles, dues le plus souvent au choc d’une mouche contre la cornée et à la libération des œufs, suivie de leur transformation rapide en larves [79, 80].
Cette affection doit être recherchée chez tout patient d’origine rurale présentant une inflammation oculaire plus ou moins sévère. Des opacités linéaires intrastromales et une kérato-uvéite peuvent être des signes d’appel probablement en rapport avec une migration des larves dans le stroma cornéen. L’examen clinique peut parfois montrer des ulcères de cornée. Les larves d’environ 1 mm de long se déplacent à grande vitesse pour fuir la lumière lors de l’examen à la lampe à fente et ainsi se cacher, se concentrant dans le cul-de-sac conjonctival inférieur. La détection dans la conjonctive de larves de mouche prélevées sous anesthésie topique avec une petite pince permet de confirmer le diagnostic (examen microscopique × 10). Le traitement des formes externes d’ophtalmomyiase repose sur l’extraction des larves pour éviter le passage au stade d’ophtalmomyiase interne. Les complications cécitantes sont à craindre en l’absence d’une prise en charge précoce et adaptée [78, 81].
L’onchocercose est une filariose dermique provoquée par la microfilaire Onchocerca volvulus (parasite spécifiquement humain). Onchocerca volvulus est transmise à l’homme par les piqûres de mouches (Simulium damnosum) qui se reproduisent dans les rivières aux eaux rapides, souvent dans des vallées fertiles. Il a été trouvé une association entre les nymphes de mouches vectrices de l’onchocercose et les crabes d’eau douce.
Les mouches inoculent la microfilaire le jour et à l’extérieur des habitations [78, 79] et l’activité de piqûre est très réduite quand la température excède 30 °C.
Chez le sujet piqué, les larves migrent vers le tissu sous-cutané où elles forment des nodules et deviennent matures au bout de 6 à 12 mois. Après maturation, les mâles adultes migrent et s’accouplent aux femelles adultes de plus grande taille, produisant entre 1 000 et 3 000 œufs par jour. Ce type de filaires semble être bien toléré par l’organisme tant qu’elles sont vivantes, mais lorsqu’elles meurent elles provoquent une réaction inflammatoire.
La surface de la cornée est une région vers laquelle migrent les microfilaires et dans la zone lésée apparaît une kératite ponctuée (au début en périphérie). Des lésions peuvent être cotonneuses, d’environ 0,5 mm de diamètre (kératites ponctuées) et si l’infection devient chronique, la cornée tout entière peut devenir opaque, ce qui conduit à la cécité. La sévérité de la maladie est directement proportionnelle au nombre de microfilaires et à l’intensité de la réponse inflammatoire qui en résulte. L’examen clinique consiste essentiellement dans le comptage des nodules par la palpation systématique :
chez les enfants : du crâne (régions mastoïde et occipitale) ;
chez les adultes : des épaules, omoplates, thorax, épineuses dorsolombaires, crêtes iliaques, trochanters, sacrum et genoux.
Le seul signe réellement pathognomonique de l’onchocercose est la présence de microfilaires dans la cornée ou dans la chambre antérieure de l’œil. La présence de nodules et la dépigmentation en peau de léopard sont des signes fortement évocateurs et nécessitent une confirmation diagnostique par une biopsie cutanée exsangue au niveau des nodules.
Le diagnostic est affirmé seulement après deux biopsies cutanées exsangues faites au niveau de crêtes iliaques prélevées à l’aide de ciseaux courbes ou d’une pince à sclérotomie (petits copeaux de peau sans faire saigner). Ces fragments sont placés dans un verre de montre contenant quelques gouttes d’eau distillée ou de sérum physiologique et 10 ou 30 minutes plus tard, l’examen microscopique au faible grossissement permet de voir les microfilaires. Les macrofilaires adultes sont faciles à reconnaître par l’analyse histologique des onchocercomes qui montrent des petits nodules fibrohyalins, avec multiples structures parasitaires d’environ 100 à 200 µm, dans certains contenants de multiples larves. En périphérie, il apparaît une réaction inflammatoire de type granulome gigantocellulaire et une fibrose [80, 82]. Le parasite est d’aspect blanc, opalin et finement strié transversalement. Le ver mâle, très petit, mesure 3 à 4 cm et son extrémité postérieure est recourbée. La femelle peut atteindre 50 cm pour un diamètre de 0,3 à 0,4 mm.
Lors de la lyse parasitaire se produit un recrutement de cellules inflammatoires et les sujets infestés présentent un prurit, des nodules sous-cutanés et des réactions inflammatoires dans la chambre antérieure [80]. Afin d’éviter des accidents iatrogènes graves, la recherche d’une coinfection par loa-loa avec une évaluation de la microfilarémie doit être effectuée avant tout traitement de l’onchocercose.
Le test de Mazzotti est une épreuve complémentaire pour le dépistage de l’onchocercose (très mal vécu par les sujets infestés). L’administration de 25 à 50 mg de diéthylcarbamazine orale provoque une réaction inflammatoire intense secondaire à la lyse massive des microfilaires, avec une flambée d’urticaire, une poussée fébrile pouvant atteindre 40 °C pendant 2 à 3 jours et une injection conjonctivale et il n’est pas sans danger en cas d’atteinte oculaire.
Ce test peut être remplacé par un test de provocation cutanée après application, sur des régions de la peau suspectées d’être parasitées, d’une crème contenant 1 % de diéthylcarbamazine qui pourra déclencher un érythème local caractéristique [81, 82].
Le colorant de May-Grünwald-Giemsa (mélange d’azur de méthylène et éosine) colore les éléments acidophiles, les granulations des polynucléaires neutrophiles et le cytoplasme des monocytes, des lymphocytes, la chromatine des noyaux et les cellules épithéliales. Les micro-organismes se colorent en bleu (cocci et bacilles), les doubles parois des kystes d’Acanthamœba apparaissent épaisses, les levures se colorent en bleu et les champignons filamenteux se présentent comme des mycéliums avec septa et parfois apparaissent comme des ombres claires qui ne se colorent pas, d’où l’importance d’une coloration selon la technique MGG lente.
➢ Bain dans la solution de May-Grünwald pendant 3 minutes.
➢ Bain dans la solution de tampon pH 7,4 pendant 1 minute.
➢ Bain dans la solution de Giemsa pendant au moins 10 minutes.
➢ Égoutter et lavage au tampon pendant 10 secondes et sécher à l’air.
Elle permet de mettre en évidence les propriétés de la paroi bactérienne et d’utiliser ces propriétés pour les distinguer et les classifier.
Sa méthode est basée sur une série de décolorations et recolorations successives, utilisant notamment le violet de gentiane, l’alcool puis la fuschsine, qui permettra la détermination du type de la bactérie en Gram positif ou négatif selon que la paroi bactérienne est épaisse ou fine.
➢ Colorer la lame par le violet de gentiane ou cristal violet pendant 30 secondes à 1 minute, puis rincer à l’eau déminéralisée.
➢ Traitement au lugol (solution d’iode iodo-iodurée) : étaler le lugol le même temps que le violet de gentiane ; rincer à l’eau déminéralisée.
➢ Décoloration : verser goutte à goutte un mélange alcool–acétone (V/V) sur la lame. Rincer abondamment avec de l’eau déminéralisée pour stopper la décoloration.
➢ Recoloration à la safranine ou à la fuchsine diluée 1/10 pendant 30 secondes à 1 minute. Laver à l’eau déminéralisée et laisser sécher à l’air.
➢ Observation avec une goutte d’huile à immersion objectif 100 (grossissement × 1000) :
■ cocci à Gram positif : surtout staphylocoques et streptocoques ;
■ cocci à Gram négatif : Neisseria gonorrhae, Neisseria meningitidis, Moraxella (cocobacille), etc. ;
■ Bacilles à Gram négatif : entérobactéries et Pseudomonas, Pasteurella, etc. ;
■ Bacilles à Gram positif : corynébatéries, Bacillus, Lactobacillus, etc.
Elle permet la détection de mycobactéries (bacilles acide alcool résistantes) : M. bovis, M. avium et M. africanum, M. tuberculosis, etc.
Elle comporte trois temps : l’application d’un colorant énergique à chaud ou à froid ; les décolorations successives par un acide fort puis à l’alcool à 90° ; une recoloration de contraste. Le premier colorant utilisé dans les techniques classiques est l’auramine (hautement toxique et cancérigène, tout particulièrement ses vapeurs).
➢ Recouvrir le frottis sec de fuchsine de Ziehl.
➢ Chauffer à émission de vapeur pendant 10 minutes au moins et rincer à l’eau distillée.
➢ Décoloration : recouvrir la lame 2 minutes à l’acide, suivi d’un rinçage. Recouvrir la lame 5 minutes dans l’alcool à 90°, suivi d’un rinçage.
➢ Contre-coloration : recouvrir la lame pendant 1 minute d’une solution de bleu de méthylène, puis rincer.
➢ Examen au microscope optique, avec objectif à immersion (× 100).
➢ Les mycobactéries apparaissent sous forme de bacilles rouges ou roses sur fond bleu-gris.
Les glucides de la paroi des champignons peuvent être transformés en aldéhydes par oxydation. Ces aldéhydes sont détectés par la réduction du complexe d’argent méthénamine. Les parois des champignons filamenteux et des levures se colorent en noir et un fond vert clair apparaît à la contre coloration.
➢ Colorer à l’acide chromique 10 minutes puis rincer à l’eau courante.
➢ Plonger dans le bisulfite de sodium (les coupes deviennent blanches).
➢ Rincer à l’eau courante puis rincer dans un bain d’eau bidistillée.
➢ Plonger dans un récipient fermé contenant l’argent méthénamine à 56 °C pendant 1 h. Solution de méthénamine d’argent : hexaméthylène tétramine + nitrate d’argent + borax.
➢ Arrêter la réaction lorsque les coupes deviennent brunâtres et rincer dans deux bains d’eau bidistillée.
➢ Plonger dans un bain de chlorure d’or 3 minutes et rincer à l’eau courante.
➢ Plonger dans un bain d’hyposulfite de sodium 5 minutes et rincer à l’eau courante.
➢ Plonger dans un bain de vert lumière 2 à 5 minutes et rincer à l’eau courante.
➢ Montage sous lamelle à l’aide de résine.
Les séquences génomiques cibles par PCR en temps réel sont : herpes simplex virus type 1 (HSV-1) ; herpes simplex virus type 2 (HSV-2) ; varicella-zoster virus (VZV) ; cytomégalovirus (CMV) ; Epstein-Barr virus (EBV) ; Adenoviridae ; Toxoplasma gondii ; Chlamydiae spp. ; Acanthamœba spp.
Utiliser des techniques manuelles ou automatisées d’extraction d’ADN à condition d’inclure des contrôles de l’extraction d’ADN et des contrôles d’absence d’inhibition de la PCR pour chaque prélèvement et pour chaque série de témoins et standards. Pour les prélèvements cornéens et pour la PCR Chlamydiae, ajouter un test qui dénombre les cellules épithéliales présentes dans l’échantillon, ce qui validera la qualité du prélèvement [31, 33, 35].
L’amplification a pour objectif la multiplication de la cible génique afin d’augmenter la sensibilité de la détection (cette procédure permet de détecter des quantités infimes d’agents infectieux). La PCR en temps réel utilise le principe de base de l’amplification cyclique d’un fragment d’ADN, avec pour différence une amplification mesurée non pas en final mais tout au long de la réaction. À chaque cycle d’amplification, la quantité d’ADN néoformé est mesurée grâce à un marqueur fluorescent dont l’émission est directement proportionnelle à la quantité d’amplicons produits. La spécificité de la réaction est liée à la fois à celle des amorces et à celle de la sonde réduisant significativement l’émission de fluorescence non spécifique. Cette technique permet de détecter plusieurs cibles dans le même tube en utilisant différentes sondes marquées avec des fluorochromes ayant des spectres d’émission différents (multiplexage).
Pour déterminer la positivité d’une PCR et/ou quantifier un échantillon par PCR en temps réel, le nombre de cycles à partir desquels le produit PCR est détectable doit être déterminé. Le moment d’apparition de ce signal seuil (cycle threshold ou Ct) est dépendant de la quantité de cibles présente dans l’échantillon.
Des sondes ont été ainsi sélectionnées pour cibler pour l’HSV-1 le gène US7, pour l’HSV-2 le gène US2, pour le VZV le gène codant pour la glycoprotéine Gp19, pour le CMV le gène codant pour la protéine ppUL83, pour les Adenoviridae le gène codant pour l’hexon et pour les Enteroviridae la région 5′ non codante. Grâce à un programme d’amplification commun, l’analyse des échantillons peut être faite simultanément avec des trousses du commerce pour HSV-1, HSV-2 et VZV ou pour CMV, HHV-6, HHV-7 et HHV-8 ou pour EBV. Les sondes TaqMan® comportent des marqueurs fluorescents différents, émettant des signaux fluorescents pour plusieurs cibles détectées simultanément dans un seul tube. Les résultats obtenus doivent toujours être validés par différents contrôles internes et externes, y compris des contrôles d’extraction [40].
Le diagnostic d’infection (infestation) par Acanthamœba nécessite l’exécution de deux techniques effectuées en parallèle : TaqMan® real-time PCR et SYBR® Green real-time PCR. En effet, la sonde TaqMan® reconnaît toutes les souches mais pour quelques espèces très rares sa sensibilité est diminuée d’au moins 10 fois. La SYBR® Green real-time PCR est utilisée comme outil de validation de la négativité des examens, car elle reconnaît toutes les séquences invariables de ce genre de protozoaires. Cette double approche prend bien compte du pouvoir prédictif positif limité des signaux négatifs de la TaqMan® real-time PCR. Pour la SYBR® Green real-time PCR, l’agent intercalant utilisé est peu ou pas fluorescent à l’état libre, mais l’émission de fluorescence augmente lorsqu’il est lié à l’ADN double brin, et cette augmentation de la fluorescence mesurée pendant l’étape de polymérisation est proportionnelle au nombre de cibles amplifiées.
En outre, l’émission fluorescente décroît complètement lors de l’étape de dénaturation du cycle suivant. Les amorces sélectionnées pour la SYBR® Green real-time PCR reconnaissent toutes les souches et toutes les espèces d’Acanthamœba, mais peuvent parfois se fixer sur des séquences non spécifiques de levures et bactéries. Pour vérifier que la séquence amplifiée par la SYBR® Green real-time PCR est celle recherchée, il faut soumettre les produits de la PCR (amplicons) à une température progressant de 55 à 95 °C par paliers de 0,5 °C, en mesurant l’intensité de la fluorescence en continu en fin de réaction, et analyser les courbes de fusion [32–34].
Les anticorps retrouvés dans les larmes (et dans les ponctions de chambre antérieure) sont des outils de diagnostic indirect d’une infection ophtalmologique. Ces anticorps résultent de la sécrétion locale d’anticorps spécifiques contre l’agent infectieux. Ils peuvent être quantifiés par des techniques immuno-enzymatiques (ELISA) ou par immunofluorescence.
La technologie Luminex® allie des microsphères fluorescentes et une double lecture après excitation par deux lasers [81, 83]. Plus de 100 billes différentes peuvent être couplées à leur surface avec des agents infectieux, des peptides ou des anticorps, permettant la détection et la quantification d’anticorps ou d’antigènes. Il est ainsi possible d’effectuer simultanément des dizaines de dosages différents en utilisant de très faibles quantités d’échantillons (de 10 à 50 µl) [84-86].
Les anticorps dosés dans les larmes peuvent être le résultat d’un passage passif d’anticorps plasmatiques à travers les capillaires vers la conjonctive ou marquer une infection locale. Les tests immunologiques adaptés aux dosages dans les larmes doivent pouvoir différencier ces deux cas de figure (sécrétion locale versus exsudat passif) et établir la charge immunitaire spécifique dans le fluide. Ceci est possible en appliquant le coefficient correctif de Goldmann-Witmer (GW) [87, 88]. Un coefficient GW supérieur à 3 suggère une sécrétion locale d’anticorps dirigés contre l’antigène testé [1, 87, 89].
Les explorations microbiologiques qui viennent d’être développées sont illustrées par les figures 2-47 à 2-75. Chacune d’entre elle porte sur un examen direct en particulier pour lequel sont indiqués les colorations utilisées et les résultats obtenus.


Fig. 2-47 Coloration : MGG sur grattage profond de cornée. Résultat : grattage de cornée chez un porteur de lentilles de contact. Image d’un élément lacunaire à paroi épaisse mais la structure n’est pas visible à ce faible grossissement. Un grossissement × 1000 permettra de visualiser la paroi épaisse caractéristique. Kyste à l’examen direct (× 400). Confirmation par PCR : Acanthamœba.

Fig. 2-48 Coloration : Gram sur grattage superficiel de cornée. Résultat : grattage très pauvre en cellules épithéliales avec image d’un élément lacunaire à paroi épaisse, mais la structure n’est pas visible à ce faible grossissement × 400. Un grossissement × 1000 pourra permettre de visualiser la paroi épaisse caractéristique d’un kyste. Confirmation par PCR : Acanthamœba.

Fig. 2-49 Coloration : MGG sur grattage profond de cornée. Résultat : Grattage de cornée chez un porteur de lentilles de contact. Kyste à l’examen direct (× 1000). Image d’éléments altérés présentant une paroi épaisse évocatrice de kystes d’Acanthamœba altérés. Confirmation par PCR : Acanthamœba.

Fig. 2-50 Coloration : MGG sur grattage de cornée. Résultat : grattage très pauvre en cellules épithéliales avec image dont la paroi peut évoquer un kyste d’Acanthamœba (× 1000). Confirmation par PCR : Acanthamœba.

Fig. 2-51 Coloration : MGG sur grattage profond de cornée. Résultat : grattage de cornée chez un porteur de lentilles de contact. Kyste d’Acanthamœba à l’examen direct (× 1000). Confirmation par PCR : Acanthamœba.

Fig. 2-52 Coloration : MGG sur grattage profond de cornée. Résultat : grattage de cornée chez un porteur de lentilles de contact. Kystes d’Acanthamœba à l’examen direct (× 1000). Confirmation par PCR : Acanthamœba.

Fig. 2-53 Coloration : coupe histologique de biopsie de cornée. Résultat : kyste d’Acanthamœba dans le stroma profond, coupe de cornéen (coloration hématoxyline/éosine) (× 1000).

Fig. 2-54 Coloration : MGG sur grattage profond de cornée. Filaments septés de champignons filamenteux. Résultat : champignons filamenteux (× 400). Par culture : Fusarium solani.

Fig. 2-55 Coloration : Gram sur grattage profond de cornée. Résultat : champignons filamenteux. Filaments septés de champignons filamenteux (× 1000). Par culture : Aspergillus fumigatus.

Fig. 2-56 Coloration : Grocott sur biopsie de cornée. Résultat : champignons filamenteux (× 400). Par culture : Fusarium solani (× 400).

Fig. 2-57 Coloration : MGG sur grattage de cornée. Résultat : pseudo-mycélium (levures) (× 1000).

Fig. 2-58 Coloration : MGG sur grattage profond de cornée. Résultat : image de levure (× 1000). Par culture : Candida parapsilosis.

Fig. 2-59 Coloration : Grocott sur biopsie de cornée. Résultat : champignons filamenteux (× 1000).

Fig. 2-60 Coloration : MGG sur grattage de cornée. Résultat : image de pseudo-mycélium de levures (× 400). Par culture : Candida albicans.

Fig. 2-61 Coloration : MGG sur grattage profond de cornée. Résultat : pseudo-mycélium. Levure (× 1000). Par culture : Candida parapsilosis.

Fig. 2-62 Coloration : MGG sur grattage profond de cornée. Résultat : champignons filamenteux (× 1000). Par culture : Aspergillus fumigatus.

Fig. 2-63 Coloration : MGG sur grattage profond de cornée. Résultat : très nombreux cocci (× 1000). Par culture : Staphylococcus aureus.
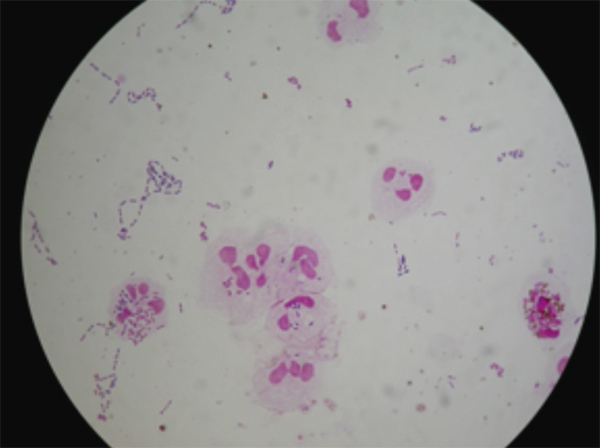
Fig. 2-64 Coloration : Gram sur grattage profond de cornée. Résultat : très nombreux cocci à Gram négatif et cocci à Gram positif (× 1000). Par culture : Neisseria meningitidis et Streptococcus mitis.

Fig. 2-65 Coloration : Ziehl-Nielsen sur grattage de cornée (kératite non répondant aux traitements de première intention). Résultat : mycobactéries (× 1000).

Fig. 2-66 Coloration : Ziehl-Nielsen sur grattage de cornée (kératite après accident avec corps étranger). Résultat : Mycobacterium chelonae (× 1000).

Fig. 2-67 Coloration : MGG sur grattage profond de cornée. Résultat : très nombreux bacilles (× 1000). Par culture : Pseudomonas aeruginosa.

Fig. 2-68 Coloration : MGG sur grattage de cornée. Résultat : cocci à Gram positif (× 1000). Par culture : Streptococci viridans.

Fig. 2-69 Coloration : MGG sur ponction de chambre antérieure (après cytocentrifugation). Résultat : très nombreux polynucléaires neutrophiles. Très nombreux bacilles (× 1000).

Fig. 2-70 Coloration : Gram sur ponction de chambre antérieure (après cytocentrifugation). Résultat : très nombreux polynucléaires neutrophiles. Très nombreux bacilles à Gram négatif (× 1000). Par culture : Serratia marcescens.

Fig. 2-71 Coloration : lames cerclées pour dépôts de grattages de cornée (étaler et laisser sécher à l’air au moins deux lames par patient).

Fig. 2-72 Coloration : immunofluorescence directe sur grattage conjonctival chez un sujet présentant une conjonctivite folliculaire aiguë (anticorps monoclonal anti-Chlamydiae couplé à la fluorescéine). Résultat : positif pour Chlamydiae trachomatis (× 400).

Fig. 2-73 Coloration : examen direct de cils entre lame et lamelle. Résultat : lente de Pediculus humanus humanus (× 10).

Fig. 2-74 Coloration : examen direct de cils entre lame et lamelle. Résultat : lente de Pediculus humanus humanus (× 40).

Fig. 2-75 Coloration : examen direct de cils entre lame et lamelle. Résultat : Demodex folliculorum (× 10).
[1] Les infections oculaires. Rapport annuel des sociétés d’ophtalmologie de France, novembre 2010. Paris : Édition L Groupe Ciel ; 2010.
[2] Cagle GD, Abshire RL. Quantitative ocular bacteriology : a method for the enumeration and identification of bacteria from the skin-lash margin and conjunctiva. Invest Ophthalmol Vis Sci 1981 ; 20 : 751-7.
[3] Azari AA, Barney NP. Conjunctivitis : a systematic review of diagnosis and treatment. JAMA 2013 ; 310 : 1721-9.
[4] Kunimoto DY, Kanitkar KD, Makar MS. Eds. The wills eye manual, office and emergency room diagnosis and treatment of eye disease. 4th ed. Philadelphie : Lippincott Williams & Wilkins ; 2004.
[5] Bhadange Y, Sharma S, Das S, Sahu SK. Role of liquid culture media in the laboratory diagnosis of microbial keratitis. Am J Ophthalmol 2013 ; 156 : 745-51.
[6] Chaurasia S, Ramappa M, Ashar J, Sharma S. Neonatal infectious keratitis. Cornea 2014 ; 33 : 673-6.
[7] Matejcek A, Goldman RD. Treatment and prevention of ophthalmia neonatorum. Can Fam Physician 2013 ; 59 : 1187-90.
[8] Goldschmidt P, Rostane H, Sow M, et al. Detection by broad-range real-time PCR assay of Chlamydiae species infecting human and animals. British Journal of Ophthalmology 2006 ; 90 : 1425-9.
[9] de Barbeyrac B, Goldschmidt P, Malembie S, et al. Quality assessment of conjunctival specimens for Chlamydia trachomatis PCR detection in children with active trachoma. Clin Microbiol Infect 2007 ; 13 : 689-94.
[10] Elner VM, Strieter RM, Pavilack MA, et al. Human corneal interleukin-8. IL-1 and TNF-induced gene expression and secretion. Am J Pathol 1991 ; 139 : 977-88.
[11] Schlegel L, Chaumeil C, Quesnot S, et al. Retrospective study of the prevalence and sensitivity to antibiotics of bacteria isolated from ocular samplings. J Fr Ophtalmol 1995 ; 18 : 250-8.
[12] Darugar A, Gaujoux T, Goldschmidt P, et al. Clinical, microbiological and therapeutic features of severe bacterial keratitis. J Fr Ophtalmol 2011 ; 34 : 362-8.
[13] Sharma S. Diagnosis of fungal keratitis : current options. Expert Opin Med Diagn 2012 ; 6 : 449-55.
[14] Rondeau N, Bourcier T, Chaumeil C, et al. Fungal keratitis at the centre hospitalier national d’ophtalmologie des Quinze-Vingts : retrospective study of 19 cases. J Fr Ophtalmol 2002 ; 25 : 890-6.
[15] Gaujoux T, Borsali E, Goldschmidt P, et al. Fungal keratitis in France. Acta Ophthalmol 2011 ; 89 : 215-6.
[16] Goldschmidt P, Degorge S, Benallaoua D, et al. New strategy for rapid diagnosis and characterization of keratomycosis. Ophthalmology 2012 ; 119 : 945-50.
[17] Gaujoux T, Chatel MA, Chaumeil C, et al. Outbreak of contactlens-related Fusarium keratitis in France. Cornea 2008 ; 27 : 1018-21.
[18] Thomas PA, Kaliamurthy J. Mycotic keratitis : epidemiology, diagnosis and management. Clin Microbiol Infect 2013 ; 19 : 210-20.
[19] Bourcier T, Chaumeil C. How to prescribe local antifungal and antiamœbicide topical drugs. J Fr Ophtalmol 2007 ; 30 : 431-5.
[20] Tham AC, Sanjay S. Clinical spectrum of microsporidial keratoconjunctivitis. Clin Experiment Ophthalmol 2012 ; 40 : 512-8.
[21] Troke P, Obenga G, Gaujoux T, et al. The efficacy of voriconazole in 24 ocular Fusarium infections. Infection 2013 ; 41 : 15-20.
[22] Schwab IR. The changing spectrum of microbial keratitis : is microsporia increasing as a cause of microbial keratitis or is it a previously unrecognized cause ? Br J Ophthalmol 2012 ; 96 : 774-5.
[23] Das S, Sharma S, Sahu SK, Nayak SS, Kar S. Diagnosis, clinical features and treatment outcome of microsporidial keratoconjunctivitis. Br J Ophthalmol 2012 ; 96 : 793-5.
[24] Garg P. Microsporidia infection of the cornea--a unique and challenging disease. Cornea 2013 ; 32 : S33-8.
[25] Lorenzo-Morales J, Marciano-Cabral F, Lindo JF, et al. Pathogenicity of amœbae. Exp Parasitol. 2010 ; 126 : 2-3.
[26] Niederkorn JY, Alizadeh H, Leher H, McCulley JP. The pathogenesis of Acanthamœba keratitis. Microbes and Infection 1999 ; 1 : 437-43.
[27] Singh S, Satani D, Patel A, Vhankade R. Colored cosmetic contact lenses : an unsafe trend in the younger generation. Cornea 2012 ; 31 : 777-9.
[28] Bouheraoua N, Gaujoux T, Goldschmidt P, et al. Prognostic factors associated with the need for surgical treatments in acanthamœba keratitis. Cornea 2013 ; 32 : 130-6.
[29] Sharma S, Garg P, Rao GN. Patient characteristics, diagnosis, and treatment of non-contact lens related Acanthamœba keratitis. The British Journal of Ophthalmology 2000 ; 84 : 1103-8.
[30] Goldschmidt P, Degorge D, Benallaoua D, et al. New tool for the simultaneous detection of 10 different genotypes of Acanthamœba available from the american type culture collection. Br J Ophthalmol 2009 ; 93 : 1096-100.
[31] Yera H, Zamfir O, Bourcier T, et al. Comparison of PCR, microscopic examination and culture for the early diagnosis and characterization of Acanthamœba isolates from ocular infections. Eur J Clin Microbiol Infect Dis 2007 ; 26 : 221-4.
[32] Goldschmidt P, Yera H, Degorge S, et al. Quality assessment of the molecular tools used for the diagnosis of Acanthamœba. Jpn J Protozool 2007 ; 40.
[33] Goldschmidt P, Degorge S, Saint-Jean C, et al. Resistance of Acanthamœba to classic DNA extraction methods used for the diagnosis of corneal infections. British Journal of Ophthalmology 2008 ; 92 : 112-5.
[34] Goldschmidt P, Degorge S, Benallaoua D, et al. Rapid detection and simultaneous molecular profile characterization of Acanthamœba infections. Diagn Microbiol Infect Dis 2012 ; 74 : 137-41.
[35] Goldschmidt P, Degorge S, Merabet L, Chaumeil C. Enzymatic treatment of specimens before DNA extraction directly influences molecular detection of infectious agents. PLoS One 2014 ; 9 : e94886.
[36] Newman H, Gooding C. Viral ocular manifestations : a broad overview. Rev Med Virol 2013 ; 23 : 281-94.
[37] PCR used for the diagnosis of Herpesviruses and Acanthamœbal keratitis. British Journal of Ophthalmology 2006 ; 90 : 1354-6.
[38] Subasic D, Karamehic J. Optimisation of RT-PCR for detection of enteroviruses. Med Arh 2006 ; 60 : 217-8.
[39] Dubot-Pérès A, Tan CY, de Chesse R, et al. SYBR green real-time PCR for the detection of all enterovirus-A71 genogroups. PLoS One 2014 ; 9 : e89963.
[40] Dekeyser S, El Nady M, Diaz E, et al. Diagnosis of herpetic esophagitis in the immunocompetent subject by PCR (Herpès Consensus Générique-Argène). Report of six cases. Pathol Biol (Paris) 2009 ; 57 : 101-6.
[41] Dorsch JN. Neurologic syndromes of the head and neck. Prim Care 2014 ; 41 : 133-49.
[42] Franco E, Gabutti G, Bonanni P, et al. Herpes Zoster and its prevention in Italy. Scientific consensus statement. Ig Sanita Pubbl 2014 ; 70 : 111-27.
[43] Artornsombudh P, Sanpavat A, Tinnungwattana U, et al. Prevalence and clinicopathologic findings of conjunctival epithelial neoplasia in pterygia. Ophthalmology 2013 ; 120 : 1337-40.
[44] Di Girolamo N. Association of human papilloma virus with pterygia and ocular-surface squamous neoplasia. Eye (Lond) 2012 ; 26 : 202-11.
[45] Takamura Y, Kubo E, Tsuzuki S, Akagi Y. Detection of human papillomavirus in pterygium and conjunctival papilloma by hybrid capture II and PCR assays. Eye (Lond) 2008 ; 22 : 1442-5.
[46] Nemet AY, Vinker S, Kaiserman I. Associated morbidity of chalazia. Cornea 2011 ; 30 : 1376-81.
[47] Kaliki S, Arepalli S, Shields CL, et al. Conjunctival papilloma : features and outcomes based on age at initial examination. JAMA Ophthalmol 2013 ; 131 : 585-93.
[48] Verma V, Shen D, Sieving PC, Chan CC. The role of infectious agents in the etiology of ocular adnexal neoplasia. Surv Ophthalmol 2008 ; 53 : 312-31.
[49] Ohtomo K, Ueta T, Toyama T, Nagahara M. Predisposing factors for primary acquired nasolacrimal duct obstruction. Graefes Arch Clin Exp Ophthalmol 2013 ; 251 : 1835-9.
[50] Ali MJ, Joshi SD, Naik MN, Honavar SG. Clinical profile and management outcome of acute dacryocystitis : two decades of experience in a tertiary eye care center. Semin Ophthalmol 2013 ; 30.
[51] Mills DM, Bodman MG, Meyer DR, Morton AD 3rd. ASOPRS Dacryocystitis Study Group. The microbiologic spectrum of dacryocystitis : a national study of acute versus chronic infection. Ophthal Plast Reconstr Surg 2007 ; 23 : 302-6.
[52] Mohan ER, Kabra S, Udhay P, Madhavan HN. Intracanalicular antibiotics may obviate the need for surgical management of chronic suppurative canaliculitis. Indian J Ophthalmol 2008 ; 56 : 338-40.
[53] Hoshino A, Fujii T, Hibino S, et al. Acute infantile dacryoadenitis. J Pediatr 2014 ; 164 : 425.
[54] Goold LA, Madge SN, Au A, et al. Acute suppurative bacterial dacryoadenitis : a case series. Br J Ophthalmol 2013 ; 97 : 735-8.
[55] Fanella S, Singer A, Embree J. Presentation and management of pediatric orbital cellulitis. Can J Infect Dis Med Microbiol 2011 ; 22 : 97-100.
[56] Mouriaux F, Rysanek B, Babin E, Cattoir V. Orbital cellulitis. J Fr Ophtalmol 2012 ; 35 : 52-7.
[57] Peña MT, Preciado D, Orestes M, Choi S. Orbital complications of acute sinusitis : changes in the post-pneumococcal vaccine era. JAMA Otolaryngol Head Neck Surg 2013 ; 139 : 223-7.
[58] Connolly DJ. Paediatric post-septal and pre-septal cellulitis : 10 years’ experience at a tertiary-level children’s hospital. Br J Radiol 2014 ; 87 : 20130503.
[59] Jackson WB. Blepharitis : current strategies for diagnosis and management. Can J Ophthalmol 2008 ; 43 : 170-9.
[60] Groden LR, Murphy B, Rodnite J, Genvert GI. Lid flora in blepharitis. Cornea 1991 ; 10 : 50-3.
[61] Scheinfeld N, Berk T. A review of the diagnosis and treatment of rosacea. Postgrad Med 2010 ; 122 : 139-43.
[62] Baldwin HE. Diagnosis and treatment of rosacea : state of the art. J Drugs Dermatol 2012 ; 11 : 725-30.
[63] Webster G, Schaller M. Ocular rosacea : a dermatologic perspective. J Am Acad Dermatol. 2013 ; 69 : S42-3.
[64] Becherel PA, Chosidow O. Ectoparasitose cutanée. La Revue du Praticien 2002 ; 52 : 79-84.
[65] Champion RH, Burton JL, Burns DA, et al. Textbook of dermatology. Boston : Blackwell ; 1998, chap. 33.
[66] Rivera N, Molina P, Torres A. Measurement of the index of infection by Demodex spp in patients with chronic blepharitis and in patients without other ocular diseases. Rev Chilena Infectol 2013 ; 30 : 494-501.
[67] Liang L, Ding X, Tseng SC. High prevalence of demodex brevis infestation in chalazia. Am J Ophthalmol 2014 ; 157 : 342-8.
[68] Pahuja S, Puranik C, Jelliti B, et al. Parasitic infections of the external eye. Ocul Immunol Inflamm 2013 ; 21 : 292-9.
[69] Poux de tête et pédiculose du cuir chevelu. La Revue Prescrire 2000 ; 21 : 761-70.
[70] Prise en charge de la gale dans les établissements de soins pour personnes âgées. La Lettre de l’Infectiologue 2000 ; 8 : 351-7.
[71] Verallo O, Fragiotta S, Carnevale C, et al. Subconjunctival Loiasis : case reports and review of cases described in Italy. Clin Ter 2013 ; 164 : e127-31.
[72] Petithory JC, Ardoin F, Ash LR, et al. Microscopic diagnosis of blood parasites following a cytoconcentration technique. Am J Trop Med Hyg 1997 ; 57 : 78-83.
[73] Holmes D. Loa loa : neglected neurology and nematodes. Lancet Neurol 2013 ; 12 : 631-2.
[74] Altcheh J, Nallar M, Conca M, et al. Toxocariasis : clinical and laboratory features in 54 patients. An Pediatr (Barc) 2003 ; 58 : 425-31.
[75] Magnaval JF, Glickman LT. Toxocarose : actualités diagnostiques et thérapeutiques. La Lettre de l’Infectiologue 2006 ; 21 : 73-82.
[76] Arevalo JF, Espinoza JV, Arevalo FA. Ocular toxocariasis. J Pediatr Ophthalmol Strabismus 2013 ; 50 : 76-86.
[77] Ahn SJ, Woo SJ, Hyon JY, Park KH. Cataract formation associated with ocular toxocariasis. J Cataract Refract Surg 2013 ; 39 : 830-5.
[78] Gentil K, Pearlman E. Gamma interferon and interleukin-1 receptor 1 regulate neutrophil recruitment to the corneal stroma in a murine model of Onchocerca volvulus keratitis. Infect Immun 2009 ; 77 : 1606-12.
[79] Pearlman E, Hall LR, Higgins AW, et al. The role of eosinophils and neutrophils in helminth-induced keratitis. Invest Ophthalmol Vis Sci 1998 ; 39 : 1176-82.
[80] Aubry P, Touze JE. Cas cliniques en médecine tropicale. La Duraulie édit. ; mars 1990, p. 59-60.
[81] Francis H, Awadzi K, Ottesen EA. The Mazzotti reaction following treatment of onchocerciasis with diethylcarbamazine : clinical severity as a function of infection intensity. Am J Trop Med Hyg 1985 ; 34 : 529-36.
[82] Taylor MJ, Hoerauf A, Bockarie M. Lymphatic filariasis and onchocerciasis. Lancet 2010 ; 376 : 1175-85.
[83] Faresjö M. A useful guide for analysis of immune markers by fluorochrome (Luminex) technique. Methods Mol Biol 2014 ; 1172 : 87-96.
[84] Anderson S, Wakeley P, Wibberley G, et al. Development and evaluation of a Luminex multiplex serology assay to detect antibodies to bovine herpes virus 1, parainfluenza 3 virus, bovine viral diarrhoea virus, and bovine respiratory syncytial virus, with comparison to existing ELISA detection methods. J Immunol Methods 2011 ; 366 : 79-88.
[85] Navidad JF, Griswold DJ, Gradus MS, Bhattacharyya S. Evaluation of Luminex xTAG gastrointestinal pathogen analyte-specific reagents for high-throughput, simultaneous detection of bacteria, viruses, and parasites of clinical and public health importance. J Clin Microbiol 2013 ; 51 : 3018-24.
[86] Wessels E, Rusman LG, van Bussel MJ, Claas EC. Added value of multiplex Luminex Gastrointestinal Pathogen Panel (xTAG® GPP) testing in the diagnosis of infectious gastroenteritis. Clin Microbiol Infect 2014 ; 20 : O182-7.
[87] Coyle PK, Sibony PA. Viral antibodies in normal tears. Invest Ophthalmol Vis Sci 1988 ; 29 : 1552-8.
[88] Goldman H, Witmer R. Antibodies in the aqueous humor. Ophthalmologica 1954 ; 127 : 323-30.
[89] Errera MH, Goldschmidt P, Batellier L, et al. Findings in detection of Herpesviridae by polymerase chain reaction and intraocular antibody production in a case series of anterior uveitis. Ocul Immunol Inflamm 2013 ; 21 : 61-8.
Afssaps. Collyres et autres topiques antibiotiques dans les infections oculaires superficielles. Juillet 2004. En ligne : http://www.infectiologie.com/site/medias/_documents/consensus/2004-atb-locale-OPH-recos-afssaps.pdf
Afssaps. Prophylaxie des infections conjonctivales du nouveau-né. Novembre 2010. En ligne : http://nosobase.chu-lyon.fr/recommandations/afssaps/2010_InfectionsConjonctivales_AFSSAPS.pdf
Borderie VM, Gineys R, Goldschmidt P, et al. Association of anti-herpes simplex virus IgG in tears and serum with clinical presentation in patients with presumed herpetic simplex keratitis. Cornea 2012 ; 31 : 1251-6.
M. Randon, F. Brignole-Baudouin, C. Baudouin, A. Denoyer
Sur le plan ophtalmologique, l’infection à Demodex est associée à une blépharite symptomatique ou non, qui s’étend parfois à des troubles chroniques de la surface oculaire ou bien participe à la pathogenèse de la rosacée. Le Demodex folliculorum, de la sous-classe des acariens, vit en groupe autour de la racine des cils, alors que le Demodex brevis a tendance à vivre en solitaire dans les glandes sébacées ou les glandes de Meibomius. Le Demodex a été associé à diverses pathologies comme un dysfonctionnement des glandes de Meibomius, des blépharoconjonctivites chroniques, des néovascularisations cornéennes, des opacités cornéennes superficielles voire des cicatrices nodulaires. D’un point de vue diagnostique, l’épilation de deux cils ou plus par paupière, avec manchons périciliaires (huit cils ou plus pour les deux yeux), est la technique de référence. Des nouvelles méthodes d’imagerie in vivo pourraient à l’avenir permettre aussi d’optimiser le diagnostic et la prise en charge thérapeutique.
Le Demodex est un ectoparasite microscopique de la classe des arachnides et de la sous-classe des acariens qui vit au sein ou à proximité des follicules pileux des mammifères. Demodex vient du grec demos : graisse et dex : vers de bois. Environ 65 espèces de Demodex ont été recensées. Deux espèces ont l’homme pour hôte : Demodex folliculorum et Demodex brevis, connus pour être des acariens du bord palpébral. L’infection par Demodex est fréquente, souvent asymptomatique, et parfois responsable de certaines affections ophtalmologiques et cutanées.
Demodex folliculorum et Demodex brevis sont typiquement retrouvés chez l’humain. D. folliculorum a été décrit en 1842 par Simon [1]. Coston a rapporté une infection à Demodex chez 22 patients en 1961 [2]. D. brevis a été différencié de D. folliculurum en 1963 par Akbulatoya [3]. Ces deux espèces de Demodex appartiennent à la famille des Demodicidae de l’ordre des Trombidiformes de la sous-classe des Acari. Elles sont majoritairement trouvées sur la face, près du nez, sur les cils et sourcils, mais peuvent être trouvées partout sur le corps. Au niveau oculaire, le D. folliculorum est présent dans le follicule pileux ou ciliaire, alors que D. brevis vit dans les glandes sébacées du corps ciliaire (glandes de Zeiss) ou les glandes de Meibomius. Un seul follicule peut contenir jusqu’à 25 D. folliculurum. Le D. brevis a un caractère plus solitaire. Les adultes D. folliculorum dans le follicule sont parallèles au cil, la tête en bas, avec l’extrémité caudale (opisthosoma) dépassant légèrement de la surface cutanée. Les acariens immatures et les larves sont enchâssés plus profondément que les adultes.
Les acariens adultes mesurent entre 0,3 et 0,4 mm de long, à noter que D. brevis est légèrement plus court que D. folliculorum. Ils ont un corps allongé semi-transparent, constitué du prosome (céphalothorax) et de l’opisthosome (abdomen). La locomotion est assurée par huit pattes (podosomes) attachées au premier tiers antérieur du corps et chaque patte présente deux ou trois petites griffes. Les larves, nymphes et protonymphes, n’ont que trois paires de pattes. Les parasites peuvent quitter le follicule pileux et se déplacer lentement sur la peau à une vitesse de 8 à 16 mm par heure, surtout la nuit car ils sont photophobes [4].
Ils respirent via la trachée, les stigmata (petites ouvertures de la peau), l’intestin et la peau elle-même. Le corps est couvert d’écailles pour s’attacher au follicule pileux et l’acarien a une bouche en tête d’épingle pour manger les kératinocytes et le sébum qui s’accumulent dans le follicule pileux. Le pharynx, localisé derrière la bouche, agit comme une pompe pour aspirer la nourriture vers l’œsophage et l’estomac. L’estomac a une forme tubulaire avec de multiples diverticules s’étendant à tout l’abdomen. L’estomac et ses diverticules produisent des enzymes digestives et absorbent les nutriments. De façon singulière, cette espèce d’acarien ne possède pas d’anus. Leur abdomen devient de plus en plus gros, après la mort leur décomposition entraîne la libération des fèces.
L’examen en microscopie électronique a permis une meilleure description de cet acarien. D. folliculorum a un plus long corps et un gnathasoma (tête) doté d’une colonne supracoxale. La bouche a une ouverture ronde de 1 µm, une aiguille tranchante de 300 nm, pour déchirer et piquer. D. brevis possède un opisthosome plus court et un gnathasoma moins complexe [5]. Les femelles D. folliculorum sont plus larges et plus rondes que les mâles. Ces acariens sont sexués et la maturité sexuelle est atteinte au stade larvaire. La fécondation est interne. Les femelles sont territoriales, elles restent dans leurs follicules et attendent les mâles nomades qui se déplacent de follicule en follicule à la recherche de femelles. La reproduction a lieu à l’entrée du follicule dans l’obscurité. Le mâle dépose ses spermatozoïdes sous forme de spermatophore (capsule contenant les spermatozoïdes).
Après la fécondation, la femelle s’enfonce dans le follicule proche de l’ouverture de la glande sébacée et dépose ses œufs. Les larves apparaissent 3 à 4 jours après et deviennent adultes en environ 7 jours en passant par le stade de protonymphe et deutonymphe. Spickett a évalué à 14,5 jours la durée du cycle de vie (de l’œuf jusqu’au stade adulte), incluant 5 jours au stade adulte [1]. Les femelles peuvent vivre 5 jours en plus après la ponte [6].
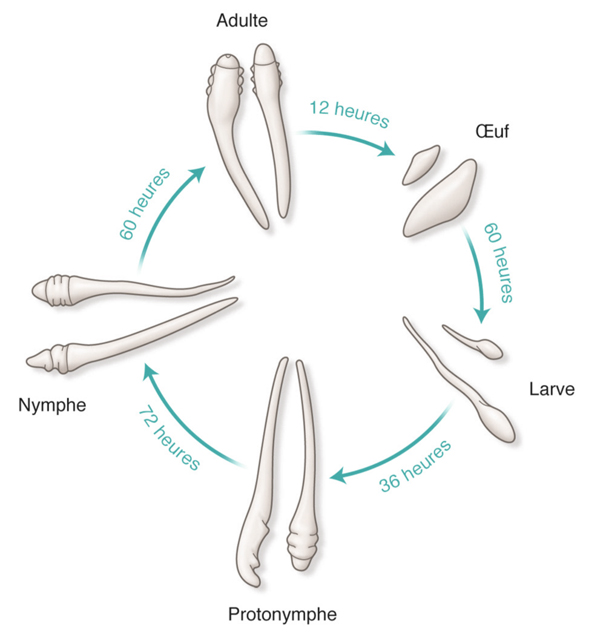
Fig. 2-76 Cycle de vie du Demodex.
Le Demodex est un ectoparasite pathogène. Des études comparatives suggèrent que la kératinisation, l’hyperplasie, la distension et l’agrégation mélanocytaire sont plus importantes si l’on retrouve une quantité importante de Demodex. Le caractère pathologique dépendrait donc de la concentration, expliquant la bonne tolérance de certains sujets porteurs mais asymptomatiques [7].
Tous les stades de Demodex consomment des cellules épithéliales en les perçant et en absorbant le cytoplasme. Ils produisent une distension et une hyperplasie épithéliale du follicule, augmentant la kératinisation et aboutissant à la formation d’un manchon périciliaire formé de kératine et de lipides. Ce manchon est observable à la lampe à fente (fig. 2-77 et 2-78). Celui-ci est plus fréquent lors d’une infection à D. folliculorum. L’hyperplasie épithéliale serait une réaction à l’effet abrasif des pattes des acariens. Bien que l’hyperplasie épithéliale dans le follicule soit fréquente, les modifications cutanées sont rares au-delà de l’espace périfolliculaire. L’accumulation de déchets produits par les acariens et notamment les Demodex morts peut affecter les follicules ou les glandes sébacées. Sur le plan histopathologique, ces acariens provoquent des modifications tissulaires, une inflammation, une hyperplasie épithéliale et une surcharge folliculaire [7]. Les rapports histologiques d’une section de follicules infectée par le Demodex relatent une distension et un épaississement de celui-ci [2]. Coston a montré que la moitié des follicules infectés présentait une infiltration lymphocytaire périfolliculaire [2]. L’infection du follicule ciliaire est responsable d’une dépilation plus facile. Elle affecte la formation et la croissance des cils qui deviennent plus cassants. La madarose est associée à une infection sévère.

Fig. 2-77 Blépharite antérieure avec collerettes périciliaires.

Fig. 2-78 Manchons cylindriques périciliaires.
Les Demodex sont impliqués dans l’apparition d’un syndrome sec oculaire. Lorsque les bouchons impliquent les glandes de Meibomius et la glande de Zeiss, une réduction de la couche lipidique du film lacrymal apparaît. Seul D. brevis peut subsister dans l’épithélium des glandes sébacées. L’effet de D. brevis sur la glande de Meibomius peut induire la formation de chalazions. Ces derniers sont des granulomes organisés, formés d’un cœur de cellules épithélioïdes et d’histiocytes, entourés par des fibroblastes, lymphocytes et plasmocytes. Ces cellules immunitaires encerclent des particules trop larges pour être éliminées par les macrophages. Des D. brevis ont été observés au centre de granulomes meibomiens [7].
L’infection par le Demodex peut accompagner des pathologies cutanées du nez, des joues ou du front. D. folliculorum est impliqué dans le Pityriasis folliculorum [8]. Cette pathologie cutanée se manifeste par un érythème diffus et affecte différentes régions. Squames, xérodermie et lésions de pseudo-rosacée sont aussi observées. La sécheresse cutanée décrit par Ayres est initiée lorsqu’un Demodex infecte un follicule et diminue le débit de sébum, ce qui conduit à une desquamation et à une xérodermie [9]. Le débit de sébum est réduit d’autant plus que le patient applique des crèmes sur la face. Les acariens prolifèrent avec ces additions d’huile, causant une augmentation de la population et aggravant la sécheresse cutanée. De nombreuses études préliminaires suggèrent une association entre cette infection parasitaire et la rosacée. Le Demodex est considéré par certains auteurs comme un agent pathogène important à la phase papulopustuleuse de la rosacée [10]. Le Demodex peut être trouvé chez des sujets sains, ce qui suggère que sa densité (supérieure à cinq Demodex par centimètre carré) est plus importante que sa présence. La prévalence de l’acarien a été étudiée sur des biopsies par trois auteurs avec des résultats contradictoires, mais des études récentes utilisant la technique de biopsie cutanée superficielle ont montré que la densité cutanée moyenne en Demodex est plus importante chez les patients porteurs de rosacée [11]. D’autres ont montré une corrélation entre l’infection à Demodex et l’acné, suggérant que ce parasite pourrait aggraver cette dermopathie [12].
Ces acariens sont aussi des vecteurs d’agents infectieux. La microscopie électronique de la surface des acariens a permis de montrer la présence de bactéries et de virus [7]. En effet, les Demodex peuvent transporter des streptocoques et des staphylocoques à leur surface. Des superantigènes produits par ces bactéries peuvent induire une rosacée [13]. Des bactéries comme le Bacillus oleronius présent à l’intérieur de l’acarien peuvent être responsables aussi d’une réaction inflammatoire. Cette bactérie est non motile, de coloration à Gram négatif. En utilisant les cils épilés de 38 patients souffrant de blépharite à Demodex, une culture a permis d’isoler cette bactérie chez 23 d’entre eux [14]. Ces bactéries sont sensibles à la ciprofloxacine, à la doxycycline, à la gentamycine et, souvent, à la clindamycine. Des anticorps sériques sont sécrétés contre deux protéines pro-inflammatoires du bacille de 62 kDa et 83 kDa. Il existe une corrélation forte entre la réaction immune sérique, l’infection oculaire à Demodex et l’acné rosacée [15]. Le bacille peut stimuler une réponse monocytaire chez les patients porteurs de rosacée [16] et les acariens morts dans les follicules ou les glandes peuvent relarguer le bacille à un seuil déclenchant une réponse inflammatoire [17]. Des phénomènes allergiques dans la paupière entretiennent les réactions inflammatoires. Des protéines inhérentes au Demodex peuvent déclencher une hypersensibilité de type retardé ou une réponse immune innée. En étudiant 92 cas de rosacée papulopustulaire appariés à 92 témoins, Georgala et al. ont montré la présence d’un intense infiltrat périfolliculaire composé de lymphocytes T à 90 % ou de lymphocytes CD4. Une augmentation des macrophages ou des cellules de Langerhans n’était retrouvée que chez les patients porteurs de Demodex [17].
De nombreux chercheurs ont tenté d’évaluer la prévalence du Demodex au niveau des cils. L’étude princeps de 1961 a évalué la prévalence à 95 % [9]. On retrouve une atteinte semblable chez toutes les ethnies, sans préférence de genre. L’infection est corrélée au nombre de glandes sébacées mais pas à la densité en follicules pileux. Post et Julin ont rapporté la présence du D. folliculorum chez 84 % d’une population âgée en moyenne de 61 ans et de 100 % chez les sujets de plus de 70 ans [18]. Les sujets âgés sont plus touchés par cette infection : environ un tiers des enfants et adolescents, la moitié des adultes et deux tiers des sujets âgés sont porteurs de ce parasite. En post mortem, le parasite est retrouvé chez 97 % des individus [2]. Liang et al. ont rapporté en 2010 que la démodécie oculaire pourrait être une cause de blépharoconjonctivite pédiatrique (enfants de 2,5 à 11 ans dans l’étude) [19]. Le faible taux de portage chez les enfants est sans doute en rapport avec une production moindre de sébum. Certains auteurs pensent que le Demodex est un parasite pathogène qu’il faut éliminer, d’autres considèrent ce parasite comme un saprophyte normal inoffensif car fréquent chez les sujets sains [6]. Les acariens sont transférés entre les hôtes par contact des poils, sourcils ou des glandes sébacées du nez.
Les facteurs de risque de la blépharite à Demodex sont principalement l’âge et la rosacée. Les autres facteurs modifiant le micro-environnement et favorisant la prolifération de l’acarien sont le phototype cutané clair (possible facteur confondant avec la rosacée), l’exposition solaire [20], la consommation d’alcool, le tabac, le stress, la consommation de boissons chaudes, l’alimentation épicée et les changements brutaux de température [21]. Une hygiène insuffisante est souvent en cause en raison de l’anatomie de la face, car les paupières ne sont pas aisément accessibles lors du lavage. L’immunodépression locale par l’instillation de corticoïdes ou par voie générale dans un contexte d’hémopathie ou d’infection à VIH (virus de l’immunodéficience humaine) favoriserait aussi cette infection [11].
L’ensemble des signes et symptômes en faveur d’une infection à Demodex sont résumés dans le tableau 2-9. En l’absence d’hygiène adéquate, l’inflammation palpébrale peut s’étendre à la conjonctive menant à une blépharoconjonctivite souvent réfractaire au traitement conventionnel. Le traitement de l’infection à Demodex permet de résoudre cette blépharoconjonctivite [22]. Cette pathologie connue chez l’adulte reste incertaine chez l’enfant. Une étude récente a étudié 12 enfants souffrant de conjonctivite réfractaire au traitement conventionnel. Ils présentaient une conjonctivite avec une rougeur bulbaire et des follicules sur la conjonctive tarsale ainsi qu’une infection à Demodex. Le traitement d’éradication a permis une résolution de l’inflammation de la surface oculaire [19]. Ces résultats suggèrent que la recherche de Demodex est également indiquée devant des blépharoconjonctivites chez l’enfant. L’inflammation conjonctivopalpébrale peut parfois s’étendre à la cornée. L’infection à Demodex peut menacer la vision en raison de vaisseaux superficiels, de lésions phlycténulaires, d’opacités superficielles et de taies nodulaires [22]. De manière intéressante, D. brevis est plus souvent associé avec des manifestations cornéennes, alors que normalement il est très peu retrouvé lors de l’épilation des cils. Des études complémentaires seront nécessaires pour savoir si une infection sévère à D. brevis peut être responsable de ces manifestations cornéennes.
Tableau 2-9 Symptômes et signes évocateurs d’une infection oculaire à Demodex.
Les symptômes peuvent être les suivants : épaississement palpébral, lichénification des paupières, madarose, trichiasis, dysfonction des glandes de Meibomius, baisse de l’acuité visuelle, rosacée, conjonctivite. L’examen à la lampe à fente révèle une collerette kératinisée autour de la base des cils, une distension folliculaire, un syndrome sec oculaire et des atteintes cornéennes comme une vascularisation superficielle, une infiltration marginale, des phlychténules, des opacités cornéennes superficielles et des cicatrices nodulaires. Le diagnostic est réalisé sur une forte suspicion clinique. Le manchon périciliaire (cylindrical dandruff) est pathognomonique d’une infection à Demodex (voir fig. 2-78) [23]. La visualisation du parasite à la lampe à fente à fort grossissement est rare en raison de la photophobie de l’acarien. Les diagnostics différentiels sont les autres causes de blépharite, le chalazion, le syndrome sec oculaire et l’orgelet.
Les cils des paupières inférieure et supérieure (deux à douze cils par œil) ne doivent pas être épilés au hasard, les cils possédant un manchon squameux ont une probabilité supérieure d’être infectés. Les cils sont placés séparément entre lame et lamelle, et immédiatement examinés au microscope à faible grossissement (× 25 à × 50) directement ou avec une goutte d’huile d’immersion ou de la méthycellulose à 2 % (fig. 2-79). Le résultat est rendu en nombre de Demodex par cil. Le Demodex d’aspect strié bouge vivement et se déplace d’environ 1 cm par heure [24]. Un ajout de fluorescéine (0,25 %) puis une attente de 20 minutes lors du montage entre lame et lamelle améliorent la détection et le comptage des acariens qui sont agglutinés dans le manchon squameux [25]. L’épilation permet de détecter essentiellement le D. folliculorum adulte car il est souvent attaché au cil. En revanche, D. brevis et les larves ne sont pas ou peu détectés par cette technique. La microscopie électronique n’est pas utilisée en pratique courante pour le diagnostic.

Fig. 2-79 D. folliculorum en microscopie optique après épilation.
La microscopie confocale in vivo, grâce à ses développements les plus modernes (HRT-RCM®, Heidelberg Engineering, Heidelberg, Allemagne), semble être un outil innovant dans la détection des acariens de manière non invasive et permet une évaluation histologique des glandes de Meibomius ainsi qu’une visualisation des follicules pileux (fig. 2-80 et 2-81).
Le Demodex joue un rôle important dans l’apparition de maladies de la surface oculaire, comme la blépharite, le dysfonctionnement des glandes de Meibomius, la conjonctivite, et de lésions cornéennes. L’infection oculaire est généralement associée à une infection systémique par le Demodex et à une rosacée oculaire. Des études sont nécessaires pour développer des méthodes diagnostiques plus sensibles et plus simples et des traitements plus efficaces et spécifiques.
[1] Spickett SG. A preliminary note on Demodex folliculorum Simon (1842), as a possible vector of leprosy. Leprosy Review 1961 ; 32 : 263-8.
[2] Morgan RJ, Coston TO. Demodex blepharitis. Southern Medical Journal 1964 ; 57 : 694-9.
[3] Akbulatova L. The pathogenic role of the mite Demodex and the clinical forms of demodicosis in man. Vestnik Dermatol Venerol 1966 ; 40 : 57-61.
[4] Zhou SH, Wang LL. Review on the biological research of human Demodex. Chinese Journal of Parasitology & Parasitic Diseases 2006 ; 24 : 379-81.
[5] Jing X, Shuling G, Ying L. Environmental scanning electron microscopy observation of the ultrastructure of Demodex. Microscopy Research and Technique 2005 ; 68 : 284-9.
[6] Rufli T, Mumcuoglu Y. The Hair follicle mites Demodex folliculorum and Demodex brevis : biology and medical importance. A review. Dermatologica 1981 ; 162 : 1-11.
[7] English FP, Nutting WB. Demodicosis of ophthalmic concern. Am J Ophthalmol 1981 ; 91 : 362-72.
[8] Karincaoglu Y, Bayram N, Aycan O, Esrefoglu M. The clinical importance of Demodex folliculorum presenting with nonspecific facial signs and symptoms. J Dermatol 2004 ; 31 : 618-26.
[9] Ayres S Jr, Ayres S 3rd. Demodectic eruptions (demodicidosis) in the human. 30 Years’ experience with 2 commonly unrecognized entities : Pityriasis folliculorum (Demodex) and Acne rosacea (Demodex Type). Archiv Dermatol 1961 ; 83 : 816-27.
[10] Casas C, Carle P, Morad L, et al. Quantification of Demodex folliculorum by PCR in rosacea and its relationship to skin innate immune activation. Exp Dermatol 2012 ; 21 : 906-10.
[11] Yamaoka T, Murota H, Tani M, Katayama I. Severe rosacea with prominent Demodex folliculorum in a patient with HIV. J Dermatol 2014 ; 41 : 195-6.
[12] Okyay P, Ertabaklar H, Savk E, Ertug S. Prevalence of Demodex folliculorum in young adults : relation with sociodemographic/hygienic factors and acne vulgaris. JEADV 2006 ; 20 : 474-6.
[13] Wolf R, Ophir J, Avigad J, et al. The hair follicle mites (Demodex spp.). Could they be vectors of pathogenic microorganisms ? Acta Derm Venereol 1988 ; 68 : 535-7.
[14] Szkaradkiewicz A, Chudzicka I, Karpinski TM, et al. Bacillus oleronius and Demodex mite infestation in patients with chronic blepharitis. Clin Microbiol Infection 2012 ; 18 : 1020-5.
[15] Li J, O’Reilly N, Sheha H, et al. Correlation between ocular Demodex infestation and serum immunoreactivity to Bacillus proteins in patients with facial rosacea. Ophthalmology 2010 ; 117 : 870-7.
[16] Lacey N, Delaney S, Kavanagh K, Powell FC. Mite-related bacterial antigens stimulate inflammatory cells in rosacea. Br J Dermatol 2007 ; 157 : 474-81.
[17] Georgala S, Katoulis AC, Kylafis GD, et al. Increased density of Demodex folliculorum and evidence of delayed hypersensitivity reaction in subjects with papulopustular rosacea. JEADV 2001 ; 15 : 441-4.
[18] Post CF, Juhlin E. Demodex folliculorum and blepharitis. Arch Dermatol 1963 ; 88 : 298-302.
[19] Liang L, Safran S, Gao Y, et al. Ocular Demodicosis as a potential cause of pediatric blepharoconjunctivitis. Cornea 2010 ; 29 : 1386-91.
[20] Kulac M, Ciftci I, Karaca S, Cetinkaya Z. Clinical importance of Demodex folliculorum in patients receiving phototherapy. Intern J Dermatol 2008 ; 47 : 72-7.
[21] Wilkin JK. Oral thermal-induced flushing in erythematotelangiectatic rosacea. J Invest Dermatol 1981 ; 76 : 15-8.
[22] Kheirkah A, Casas V, Li W, Raju VK, Tseng S. Corneal manifestations of ocular demodex infestation. Am J Ophthalmol 2007 ; 143 : 743-9.
[23] Gao Yy, Di Pascuale M, Wei L, et al. High prevalence of Demodex in eyelashes with cylindrical dandruff. Invest Ophthalmol Vis Sci 2005 ; 46 : 3089-94.
[24] Kamoun B, Fourati M, Feki J, et al. Blepharitis due to Demodex : myth or reality ? J Fr Ophtalmol 1999 ; 22 : 525-7.
[25] Kheikhah A, Blanco G, Casas V, Tseng S. Fluorescein dye improves microscopic evaluation and counting of Demodex in blepharitis with cylindrical dandruff. Cornea 2007 ; 26 : 697-700.
F. Brignole-Baudouin, C. Baudouin
Les empreintes conjonctivales offrent de manière peu invasive et quasiment indolore un tapis cellulaire propre à l’analyse des pathologies de la surface oculaire. Les cotations en cytologie standard sont très utiles pour détecter et mesurer le degré de sécheresse oculaire, mais aussi des phénomènes inflammatoires ou allergiques. De nouvelles techniques d’immunocytologie, de cytométrie en flux et de biologie moléculaire ont élargi le spectre d’utilisation des empreintes conjonctivales et en font de puissants outils d’analyse clinique et de recherche, permettant d’évaluer de nouvelles thérapeutiques et aussi de screener de nouveaux médiateurs impliqués dans la sécheresse oculaire.
Développée à la fin des années 1970 [1, 2], l’empreinte conjonctivale est maintenant une technique bien connue et adoptée par la plupart des grands centres d’ophtalmologie. Facilement reproductible, elle permet le recueil des cellules épithéliales conjonctivales d’une manière non ou très peu invasive, rapide et quasiment indolore, pour une analyse biologique des maladies de la surface oculaire. Grâce aux empreintes conjonctivales, les cellules les plus superficielles de l’épithélium conjonctival, c’est-à-dire les cellules qui desquament, sont recueillies. L’épithélium conjonctival se renouvelle par l’intermédiaire des couches basales profondes, et les couches les plus superficielles qui ont atteint leur stade de différenciation définitif sont progressivement évacuées dans les fluides lacrymaux. Les empreintes conjonctivales permettent le recueil des cellules localisées dans les couches superficielles de la conjonctive.
Le recueil des cellules est classiquement effectué à l’aide de filtres ou membranes de structure et de composition variées dépendant des applications ultérieures [3]. Les filtres sont appliqués sur la conjonctive bulbaire supérieure, une zone habituellement choisie pour sa protection par la paupière et la reproductibilité du prélèvement, qui évite une variabilité environnementale dans les zones exposées (fig. 2-82). Les filtres d’acétate de cellulose restent dévolus aux techniques de cytologie classique nécessitant une transparisation avant la lecture au microscope. Les filtres de polyéther sulfone ne pouvant être rendus transparents sont réservés aux techniques de microscopie confocale, de cytométrie en flux ou de biologie moléculaire. Ces filtres, non stériles, de tailles et de formes variées, les plus courants étant des demi-filtres de 13 mm de diamètre, sont appliqués sur la surface oculaire à l’aide d’une pince de préférence en plastique et à usage unique.
L’expérience du préleveur est nécessaire pour permettre une bonne reproductibilité du geste lors de l’application de la membrane sur l’œil, à la fois dans la pression exercée qui doit rester la plus légère possible et dans le temps d’application qui correspond généralement au temps de la simple application suivie du décollement. Il n’est pas nécessaire d’attendre et de laisser la membrane en place même quelques secondes avant de la décoller.
Il est possible de répéter facilement le prélèvement afin de recueillir davantage de cellules ou recueillir des cellules de différentes zones de la surface oculaire.
Le matériau privilégié pour réaliser l’empreinte conjonctivale destinée aux colorations classiques de cytologie favorisant la visibilité des mucocytes, comme le crésyl violet ou l’acide périodique de Schiff (periodic acid Schiff ou PAS), est composé d’esters de cellulose (GSWP01300, MF-Millipore®). Ces membranes offrent la possibilité, en fin de coloration, de les rendre transparentes sous l’effet du xylène ou du toluène afin de permettre l’analyse cytologique en microscopie classique. La zone de prélèvement dépend de la pathologie sous-jacente mais il est important de prélever les empreintes toujours au même endroit pour les études comparatives de groupes de patients et pour le suivi de ceux-ci.

Fig. 2-82 Technique classique de prélèvement sur la conjonctive bulbaire supérieure.
Diverses classifications ont été proposées permettant de coter les altérations cytologiques pour aider au diagnostic et permettre le suivi [4–6]. Trois types de populations cellulaires conjonctivales peuvent être observés sur des empreintes conjonctivales : les cellules épithéliales, les cellules à mucus et les cellules inflammatoires (fig. 2-83 à 2-85). Jusqu’à maintenant, les cellules épithéliales n’étaient considérées que comme la limite externe de la muqueuse conjonctivale, mais il a été très largement démontré qu’elles sont directement impliquées dans de nombreuses réactions biologiques, particulièrement dans les processus inflammatoires et apoptotiques [7–9]. Les cellules à mucus libèrent des mucines solubles dans le film lacrymal et de cette manière jouent un rôle de régulation et de défense important au niveau de la surface oculaire. La perte de cellules à mucus est la marque des syndromes secs [10], alors que la présence de cellules à mucus sur des empreintes obtenues à partir de la surface cornéenne est pathognomonique de la conjonctivalisation associée aux déficits en cellules souches limbiques [11]. La densité de cellules à mucus la plus importante est trouvée sur la conjonctive palpébrale nasale puis temporale, puis sur la conjonctive bulbaire près du fornix puis du limbe [2]. Cette dernière localisation est celle qui permet le mieux de voir la réduction des cellules à mucus importante à rechercher dans les sécheresses oculaires. Les cellules inflammatoires présentes dans les empreintes conjonctivales incluent : les polynucléaires neutrophiles, éosinophiles, essentiellement ; les cellules dendritiques connues pour leur forme caractéristique et leur propriété d’immunocompétence ; les cellules de Langerhans ; des populations de lymphocytes localisées dans l’épithélium ou migrant depuis le chorion sous-épithélial.
Les empreintes conjonctivales classiques permettent d’évaluer la densité des cellules à mucus et de coter la métaplasie squameuse, particulièrement dans l’œil sec, selon diverses classifications (encadrés 2-4 à 2-6).
Grade 0
• Cellules épithéliales petites et rondes avec un cytoplasme éosinophile
• Noyau de grande taille, basophile, avec un rapport nucléo/cytoplasmique (RNC) de 1/2
• Densité élevée de cellules à mucus (500 cellules/mm2) avec un cytoplasme intensément PAS positif
Grade 1
• Cellules épithéliales plus larges et polyédriques
• Noyaux de plus petite taille avec un RNC de 1/3
• Diminution de la densité des cellules à mucus (350–500 cellules/mm2) qui gardent une forme arrondie avec un cytoplasme intensément PAS positif
Grade 2
• Cellules épithéliales encore plus larges et polyédriques, parfois multinucléées avec un cytoplasme de coloration variable
• Petits noyaux avec un RNC entre 1/4 et 1/5
• Densité des cellules à mucus très diminuée (100–350 cellules/mm2), cellules à mucus plus petites et moins PAS positif
Grade 3
• Cellules épithéliales larges et polyédriques avec un cytoplasme basophile
• Petit noyau pycnotique parfois absent, RNC de 1/6
• Très peu de cellules à mucus (100 cellules/mm2)
Stade 0
• Épithélium conjonctival normal
• Rapport nucléo/cytoplasmique (RNC) : 1/1
• Densité moyenne de cellules à mucus qui sont dispersées parmi des cellules épithéliales uniformes
Stade 1
Perte débutante de cellules à mucus sans kératinisation :
• diminution de la densité des cellules à mucus
• augmentation modérée de la surface de quelques cellules épithéliales
• RNC de 1/2 à 1/3
Stade 2
Perte totale des cellules à mucus sans kératinisation :
• disparition des cellules à mucus
• toutes les cellules épithéliales sont modérément élargies, gonflées, squameuses, avec un cytoplasme de couleur bleu-vert jusqu’au rosâtre et un RNC à 1/4
Stade 3
Kératinisation débutante et minime :
• toutes les cellules épithéliales sont squameuses avec des changements chromatiques du cytoplasme qui prend une couleur rosâtre
• certaines cellules épithéliales contiennent des filaments de kératine visible
• RNC à 1/6, lié au gonflement du cytoplasme et à la condensation du noyau
Stade 4
Kératinisation modérée :
• larges cellules épithéliales métachromiques et squameuses
• davantage de cellules contiennent des filaments de kératine visible, des granules de kérato-hyaline et un noyau pycnotique
• RNC à 1/8
Stade 5
Kératinisation avancée :
• très nombreuses cellules kératinisées avec un cytoplasme modifié
• paquets de filaments de kératine dense dans lesquels le noyau est très pycnotique, lysé ou absent et parfois agrégé en débris kératinisés
Grade 0
• Cellules épithéliales petites, rondes avec un rapport nucléo/cytoplasmique (RNC) de 1/2
• Nombreuses cellules à mucus très colorées
Grade 1
• Cellules épithéliales plus larges avec un RNC diminué à 1/3
• Diminution de la densité des cellules à mucus mais qui restent très colorées par le PAS
Grade 2
• Cellules épithéliales plus larges, avec une diminution plus importante du RNC
• Diminution de la densité en cellules à mucus, avec souvent une diminution de la coloration
Grade 3
• Cellules épithéliales larges et irrégulières, noyau pycnotique
• Densité des cellules à mucus faible et coloration faible
L’identification de cellules épithéliales contenant une chromatine en forme de serpent ou snake-like chromatin (fig. 2-86) ou des inclusions intra-épithéliales, des cellules non épithéliales provenant des couches profondes de la conjonctive (lymphocytes, cellules dendritiques, éosinophiles) et mêmes d’autres micro-organismes, est possible. L’analyse de ces différentes populations cellulaires (taille, nombre, densité et modifications pathologiques) apporte des informations importantes concernant le statut de la surface oculaire. Les empreintes conjonctivales sont beaucoup plus accessibles et sont obtenues de manière moins agressive que les prélèvements cornéens et apportent indirectement des informations sur l’atteinte cornéoconjonctivale, notamment dans le domaine de l’œil sec, des pathologies limbiques et de l’inflammation chronique de la surface oculaire.

Fig. 2-83 Cytologie sur empreinte conjonctivale après coloration au crésyl violet.
Cellules épithéliales conjonctivales (flèches) et mucocytes (têtes de flèche).

Fig. 2-84 Cytologie sur empreinte conjonctivale : nombreux lymphocytes (flèches) s’infiltrant entre les cellules épithéliales.

Fig. 2-85 Cytologie sur empreinte conjonctivale : densité importante de mucocytes (flèches).

Fig. 2-86 Cytologie sur empreinte conjonctivale dans un cas de syndrome sec montrant de nombreuses cellules avec une chromatine en forme de serpent ou snake-like chromatin (flèches).
La quasi-totalité des yeux normaux ont des empreintes conjonctivales cotées grade 0 ou 1 selon la classification de Nelson [5], mais de très grandes variations peuvent être observées, en fonction de la localisation sur la cornée, du sexe, du cycle ovulatoire, de la prise de contraceptif, et même de l’heure du recueil des cellules [10]. L’âge peut aussi influencer les résultats des empreintes conjonctivales : le rapport nucléocytoplasmique diminue avec l’âge et des aspects de snake-like chromatin ont été retrouvés chez 39 % des sujets âgés [12]. Le comptage des cellules à mucus semble ne pas être influencé par l’âge, mais la répétition d’empreintes dans la même zone conjonctivale [13] et le port de lentilles de contact [14] augmentent la densité en cellules à mucus, suggérant que la stimulation des cellules à mucus intervient comme une réponse adaptative précoce à des microtraumatismes ou à des réactions inflammatoires.
Cependant, la plupart des études sur les désordres chroniques de la surface oculaire, comme les syndromes secs, les conjonctivites chroniques, la rosacée oculaire, l’utilisation au long cours de collyres antiglaucomateux ou le port prolongé de lentilles de contact, aboutissent toujours à une baisse importante et parfois une disparition des cellules à mucus [7, 15]. La perte des cellules à mucus et la métaplasie squameuse sont des signes non spécifiques de la kératoconjonctivite sèche (KCS). En plus de l’atteinte des cellules à mucus, les cellules épithéliales subissent des transformations importantes, comme un allongement cellulaire, un gonflement, une augmentation de la surface cytoplasmique entraînant une diminution du rapport nucléocytoplasmique de 1/1 à 1/8, une pycnose nucléaire ou l’apparition de snake-like chromatin [11, 16]. Dans le cas de l’étude des conjonctivites allergiques, l’empreinte peut identifier des éosinophiles très évocateurs de phénomènes allergiques (fig. 2-87). Dans certains cas sévères de kératoconjonctivites vernales, des acariens ou même des insectes ont pu être retrouvés, témoins probables de l’auto-inoculation par les mouvements de grattage (fig. 2-88 et 2-89). Il est dans ces cas très vraisemblable que ces parasites entretiennent et stimulent des réactions inflammatoires locales sévères. Rappelons simplement que l’allergie aux acariens est considérée comme une réaction essentiellement due à leurs déjections plus qu’à leur présence directe.

Fig. 2-87 Empreinte conjonctivale dans un cas d’allergie retrouvant de nombreux éosinophiles, petites cellules aux noyaux denses bilobés.

Fig. 2-88 Empreinte prise chez un enfant atteint de kératoconjonctivite vernale montrant la présence d’un acarien au sein des cellules épithéliales de la conjonctive.

Fig. 2-89 Cas similaire chez un autre enfant avec présence d’un insecte probablement inoculé lors des manœuvres de grattage.
L’exploitation de la technique classique de cytologie conjonctivale reste cependant limitée. Pour cette raison, de nouvelles procédures comme les techniques immunocytologiques ont été développées durant ces quinze dernières années. Au départ, la technique d’immunofluorescence ne pouvait pas être pratiquée directement sur les empreintes permettant le recueil des cellules. Ces cellules conjonctivales devaient être transférées sur un support transparent, entraînant un risque de perte ou d’altération cellulaires [11, 17]. L’utilisation de membranes transparentes dès leur mise en milieu liquide permet l’analyse en lumière blanche comme en fluorescence (Biopore Millicell® Millipore). Mais, aujourd’hui, l’utilisation d’un microscope confocal a rendu possible les techniques d’immunofluorescence directement sur ces empreintes (fig. 2-90) [11, 15]. Les techniques d’immunoperoxydase peuvent aussi être utilisées sur les empreintes avant de les rendre transparentes pour un examen microscopique [18]. Dans les deux cas, de nombreux marqueurs peuvent être utilisés pour identifier les cellules ou leur activation et analyser les épithéliums de surface à la recherche de réactions inflammatoires. Cependant, ces techniques d’immunocytologie ne permettent pas de quantifier de manière fiable les marqueurs d’activation. Ces analyses morphologiques peuvent donc être avantageusement complétées par des techniques de quantification en particulier par la cytométrie en flux.

Fig. 2-90 Immunomarquage en microscopie confocale (marquage vert du CD44, rouge des noyaux cellulaires), montrant des cellules dendritiformes au sein de l’épithélium conjonctival.
La cytométrie en flux a offert à la biologie cellulaire de nombreuses avancées depuis les années 1970. La technique consiste en l’illumination individuelle de cellules en suspension avec un faisceau laser de haute énergie et monochromatique. Les cellules ainsi illuminées réfléchissent le signal lumineux sur un angle étroit (autour de 10°) proportionnel à leur taille (dispersion en avant) et les autres signaux lumineux sur un angle large (autour de 90°) proportionnel à leur structure ou à leur densité intracellulaire (dispersion latérale). Des signaux colorés sont aussi émis, correspondant à l’autofluorescence ou à la fluorescence transmise quand les cellules ont été marquées avec un marqueur fluorescent comme les anticorps conjugués à la fluorescéine. La détection de très faibles concentrations de cellules, aussi faibles que 100 à 500 cellules/ml, ainsi que d’intensité faible de fluorescence, est possible. Au-delà de la caractérisation des cellules, la cytométrie en flux permet également l’exploration de leur fonction et une approche physiologique.
L’utilisation de la cytométrie en flux pour l’analyse des empreintes conjonctivales [19] a été développée pour obtenir une technique précise et reproductible permettant d’explorer les désordres de la surface oculaire et analyser l’efficacité ou la toxicité de certains médicaments topiques. Trois pathologies principales ont directement bénéficié de cette nouvelle technique : l’allergie, les syndromes secs et les atteintes toxiques [15, 20–22].
Les maladies de la surface oculaire sont associées à différents types d’altérations cellulaires : une perte de cellules à mucus ; des réactions métaplasiques induisant une exfoliation cellulaire progressive et une desquamation (fig. 2-91 et 2-92) ; une augmentation en parallèle du nombre de cellules inflammatoires, notamment les cellules dendritiques, associée à l’activation des cellules épithéliales sur un mode inflammatoire [19, 23, 24]. Les techniques de détection de l’apoptose cellulaire induite par des processus toxiques ou inflammatoires et actuellement accessibles à la technique de cytométrie en flux comprennent la diminution de la taille des cellules, l’expression de marqueurs cellulaires comme l’annexine-V et l’Apo 2.7, et la détermination du pic sub-G1 du cycle cellulaire [7, 20]. De plus, les phénomènes immuno-inflammatoires peuvent être reconnus grâce à des marqueurs caractéristiques comme l’expression des antigènes de classe II du complexe majeur d’histocompatibilité HLA-DR, l’amplification de molécules d’adhésion ou la présence de molécules appartenant à la famille des récepteurs au TNF-α (CD40, CD95/Fas) ou à celle des interleukines [9, 23]. Une étude a montré que cette technique peut permettre de discriminer les marqueurs des systèmes TH1 et TH2 par la présence des récepteurs aux chimiokines CCR5 et CCR4 respectivement, qui sont exprimés de manière très importante au niveau des cellules épithéliales dans le syndrome de Sjögren pour le CCR5 et dans la kératoconjonctivite vernale pour CCR4 [24]. Il semblerait que de tous ces marqueurs, l’expression de HLA-DR, normalement limitée aux cellules immunitaires mais surexprimée par les cellules épithéliales dans le cas d’une inflammation induite par le système immunitaire, soit le facteur le plus pertinent. Du fait de sa très grande sensibilité, dépendante de l’intensité des réactions inflammatoires, HLA-DR est actuellement un des meilleurs marqueurs d’inflammation au niveau de la surface oculaire.

Fig. 2-91 Kératoconjonctivite vernale responsable d’une dessiccation cornéenne centrale.

Fig. 2-92 Même cas qu’à la fig. 2-91 en empreinte cornéenne (marquage du cytosquelette à la phalloïdine) retrouvant l’épithélium cornéen anormal, desséché et desquamant dans le film lacrymal.
Cette lésion entraînera secondairement un ulcère vernal sévère.
Le prélèvement classique demande de l’expérience, notamment lors des phases d’application où il faut savoir doser le temps et la force d’application de la membrane. Cette dépendance à l’expérience du préleveur, hors pathologie du patient (allergie ou sécheresse, par exemple), peut être la cause de variations importantes du nombre de cellules recueillies. Il prend du temps, car il faut prédécouper les membranes en suivant une procédure rigoureuse mais relativement lourde (fig. 2-93) ; en outre, celles-ci ne sont généralement pas stériles. Un dispositif de recueil stérile et à usage unique vient d’être mis sur le marché (EyePrim®, OPIA Technologies, France : fig. 2-94). Il permet désormais de standardiser le mode de prélèvement, la membrane en polyéther sulfone stérile, préinstallée dans le dispositif, étant appliquée sur l’œil à l’aide d’un piston [25]. Ce dispositif permet de réaliser facilement le recueil, sans risque pour le patient, évitant l’utilisation de pinces et garantissant la stérilité de la membrane. Grâce à ces qualités, il est déjà utilisé pour des études cliniques. Les seules limitations de ce dispositif sont pour l’instant son coût et le fait qu’il n’existe que lié aux membranes de polyéther sulfone. Cependant, bien que ces membranes ne puissent être rendues transparentes par le toluène comme les membranes d’acétate de cellulose utilisées pour la cytologie standard, elles permettent l’analyse des anomalies cytologiques avec des microscopes classiques, même si elle est moins confortable.

Fig. 2-93 Ensemble des matériels nécessaires pour pratiquer une empreinte conjonctivale.
a. Ici, les filtres présentés sont en esters de cellulose destinés à l’examen cytologique standard. b. Une paire de gants. c. Un tube par patient pour le recueil des empreintes, contenant une solution de formol à 10 %. d. Une pince en plastique mousse stérile pour saisir les membranes et les appliquer sur la conjonctive. e. Un pot stérile pour conserver les membranes de chaque patient.

Fig. 2-94 Dispositif EyePrim® de prélèvement des empreintes conjonctivales.
Les techniques de biologie moléculaire appliquées aux empreintes conjonctivales offrent la possibilité d’analyser plusieurs transcrits simultanément sur une même empreinte, là où il fallait plusieurs recueils successifs pour enrichir le nombre de cellules recueillies pour la cytométrie en flux. Des membranes de nitrocellulose [26] ou de polyéther sulfone [27] ont été utilisées pour rechercher des cytokines pro-inflammatoires. Les membranes de polyéther sulfone permettent de recueillir 1 à 2 mg d’ARN total [27]. L’implication de l’IL-6 dans le syndrome sec auto-immun de Sjögren a été identifiée en priorité, mais de nombreuses autres cytokines ont été recherchées, comme IL-8, GRO-α, IL-1β, etc.
D’autres domaines de recherche importants concernent l’étude des mucines de la conjonctive [28, 29] ou les expressions géniques des enzymes anti-oxydantes [30, 31]. De même, des empreintes conjonctivales pratiquées chez des patients glaucomateux traités avec des analogues des prostaglandines ont permis de montrer en RT-PCR l’induction des MMP-1, 3, 9 et la réduction de leurs inhibiteurs TIMP (tissue inhibitors of metalloproteinase) 1 et 2 sous l’effet de ces molécules [32].
Récemment, les empreintes conjonctivales ont permis de mettre en évidence qu’un polymorphisme du gène THBS1 réduisant l’expression de la glycoprotéine TSP1 serait un facteur de prédisposition d’une kératoconjonctivite inflammatoire après chirurgie réfractive [33]. Enfin, une corrélation a été montrée entre les niveaux des ARN messagers et les profils d’expression de la protéine HLA-DR sur des empreintes conjonctivales recueillies à l’aide du nouveau dispositif EyePrim® [34]. Aujourd’hui, des méthodes de screening large de transcrits existent permettant d’analyser plusieurs centaines de gènes sur une seule empreinte et utilisant des techniques de microarray ou de nanostring [35].
Les empreintes conjonctivales en PCR offrent donc la possibilité d’étudier les transcrits de nombreux médiateurs ou récepteurs à grande échelle et d’envisager ainsi la possibilité de découvrir de nouveaux biomarqueurs pour les diagnostics des pathologies de la surface oculaire.
[1] Thatcher RW, Darougar S, Jones BR. Conjunctival impression cytology. Arch Ophthalmol 1977 ; 95 : 678-81.
[2] Egbert PR, Lauber S, Maurice D. A simple conjunctiva biopsy. Am J Ophthalmol 1977 ; 84 : 798-801.
[3] Singh R, Joseph A, Umapathy T, et al. Impression cytology of the ocular surface. Br J Ophthalmol 2005 ; 89 : 1655-9.
[4] Tseng SCG. Staging of conjunctival squamous metaplasia by impression cytology. Ophthalmology 1985 ; 92 : 728-33.
[5] Nelson JD. Impression cytology. Cornea 1988 ; 7 : 71-81.
[6] Adams AD, Dilly PN, Kirkness CM. Monitoring ocular disease by impression cytology. Eye 1988 ; 2 : 506-16.
[7] Brignole F, Becquet F, Pisella PJ, et al. Expression of Fas antigen (CD95) in the human conjunctival epithelium. Positive correlation with class II HLA DR expression in inflammatory conditions. Exp Eye Res 1998 ; 67 : 687-97.
[8] Baudouin C. The pathology of dry eye. Surv Ophthalmol 2001 ; 45 : S211-S220.
[9] Brignole-Baudouin F, Ott AC, Warnet JM, Baudouin C. Flow cytometry in conjunctival impression cytology : a new tool for exploring ocularsurface pathologies. Exp Eye Res 2004 ; 78 : 473-81.
[10] Puangsricharern V, Tseng SC. Cytologic evidence of corneal diseases with limbal stem cell deficiency. Ophthalmology 1995 ; 102 : 1476-85.
[11] Calonge M, Diebold Y, Saez V, et al. Impression cytology of the ocular surface : a review. Exp Eye Res 2004 ; 78 : 457-72.
[12] Bjerrum KB. Snake-like chromatin in conjunctival cells of normal elderly persons and of patients with primary Sjögren’s syndrome and other connective tissue diseases. Acta Ophthalmol Scand 1995 ; 73 : 33-6.
[13] Rolando M, Terragna F, Giordiano G, Calabria G. Conjunctival surface damage distribution in keratoconjunctivitis sicca : an impresion cytology study. Ophthalmologica 1990 ; 200 : 170-6.
[14] Connor CG, Campbell JB, Steel SA, Burke JH. The effects of daily wear contact lenses on goblet cell density. J Am Optom Assoc 1994 ; 65 : 792-4.
[15] Pisella PJ, Brignole F, Debbasch C, et al. Flow cytometric analysis of conjunctival epithelium in ocular rosacea and keratoconjunctivitis sicca. Ophthalmology 2000 ; 107 : 1841-9.
[16] Marner K. Snake-like appearance of nuclear chromatin in conjunctival epithelial cells from patients with keratoconjunctivitis sicca. Acta Ophthalmol (Copenh) 1980 ; 58 : 849-53.
[17] Baudouin C, Haouat N, Brignole-Baudouin F, et al. Immunopathological findings in conjunctival cells using immunofluorescence staining of impression cytology specimens. Br J Ophthalmol 1992 ; 76 : 545-9.
[18] Thiel MA, Bossart W, Bernauer W. Improved impression cytology techniques for the immunopathological diagnosis of superficial viral infections. Br J Ophthalmol 1997 ; 81 : 984-8.
[19] Baudouin C, Brignole F, Becquet F, et al. Flow cytometry in impression cytology specimens. A new method for evaluation of conjunctival inflammation. Invest Ophthalmol Vis Sci 1997 ; 38 : 1458-64.
[20] Brignole F, Pisella PJ, Goldschild M, et al. Flow cytometric analysis of inflammatory markers in conjunctival epithelial cells of patients with dry eyes. Invest Ophthalmol Vis Sci 2000 ; 41 : 1356-63.
[21] Baudouin C, Bourcier T, Brignole-Baudouin F, et al. Correlation between tear IgE levels and HLA DR expression by conjunctival cells in allergic and nonallergic chronic conjunctivitis. Graefes Arch Clin Exp Ophthalmol 2000 ; 238 : 900-4.
[22] Pisella PJ, Debbasch C, Hamard P, et al. Conjunctival proinflammatory and proapoptotic effects of latanoprost, preserved timolol and unpreserved timolol : an ex vivo and in vitro study. Invest Ophthalmol Vis Sci 2004 ; 45 : 1360-8.
[23] Baudouin C, Hamard P, Liang H, et al. Conjunctival epithelial cells from long-term treated glaucoma patients exhibit inflammatory cytokines. Ophthalmology 2004 ; 111 : 2186-92.
[24] Baudouin C, Liang H, Bremond-Gignac D, et al. CCR 4 and CCR 5 expression in conjunctival specimens as differential markers of TH1/TH2 in ocular surface disorders. J Allergy Clin Immunol 2005 ; 116 : 614-9.
[25] Roy P, Cimbolini N, Antonelli S, et al. Assessment of a new device for conjunctival impression. ARVO 2012 ; 261 : program number 1868.
[26] Jones DT, Monroy D, Ji Z, et al. Sjögren’s syndrome : cytokine and Epstein-Barr viral gene expression within the conjunctival epithelium. Invest Ophthalmol Vis Sci 1994 ; 35 : 3493-504.
[27] Narayanan S, Miller WL, McDermott AM. Conjunctival cytokine expression in symptomatic moderate dry eye subjects. Invest Ophthalmol Vis Sci 2006 ; 47 : 2445-50.
[28] Corrales RM, Calonge M, Herreras JM, et al. Levels of mucin gene expression in normal human conjunctival epithelium in vivo. Curr Eye Res 2003 ; 27 : 323-8.
[29] Corrales RM, Galarreta D, Herreras JM, et al. Conjunctival mucin mRNA expression in contact lens wear. Optom Vis Sci 2009 ; 86 : 1051-8.
[30] Bradley JL, Edwards CS, Fullard RJ. Adaptation of impression cytology to enable conjunctival surface cell transcriptome analysis. Curr Eye Res 2014 ; 39 : 31-41.
[31] Corrales RM, Galarreta D, Herreras J, et al. Antioxidant enzyme mRNA expression in conjunctival epithelium of healthy human subjects. Can J Ophthalmol 2011 ; 46 : 35-9.
[32] Lopilly Park HY, Kim JH, Lee KM, Park CK. Effect of prostaglandin analogues on tear proteomics and expression of cytokines and matrix metalloproteinases in the conjunctiva and cornea. Exp Eye Res 2012 ; 94 : 13-21.
[33] Contreras-Ruiz L, Ryan DS, Sia RK, et al. Polymorphism in THBS1 gene is associated with post-refractive surgery chronic ocular surface inflammation. Ophthalmology 2014 ; 121 : 1389-97.
[34] Kessal K, Riancho L, Brignole-Baudouin F, et al. Correlation between mRNA and protein expression profiles of HLA-DR in conjunctival impression cytology : using new device for collecting epithelial cells. ARVO 2014 ; 263.
[35] Stricker TP, Morales La Madrid A, Chlenski A, et al. Validation of a prognostic multi-gene signature in high-risk neuroblastoma using the high throughput digital NanoString nCounter• system. Mol Oncol 2014 ; 8 : 669-78.