Introduction : liste des étiologies
C. Creuzot-Garcher
L’œdème maculaire (OM) est un épaississement maculaire, résultat d’une accumulation de liquide dans la rétine autour de la fovéa. Il s’agit d’une affection non spécifique qui doit être considérée comme une réponse de la région maculaire à une modification de l’environnement. La baisse de vision est liée à l’altération fonctionnelle des cellules rétiniennes et aux événements mis en œuvre pour répondre à celle-ci. Les causes d’œdème maculaire sont multiples, la plupart d’entre elles s’accompagnent d’une rupture de la barrière hémato-rétinienne (BHR). L’atteinte préférentielle avec accumulation d’eau dans les couches plexiforme externe, nucléaire et plexiforme interne caractérise l’OM sur le plan histologique. Cette accumulation liquidienne peut se faire en intracellulaire et en extracellulaire et implique tout particulièrement les cellules de Müller. L’œdème intracellulaire sans altération des BHR s’accompagne d’un gonflement des cellules, lié à un trouble des transports ioniques avec augmentation du sodium (Na+) intracellulaire. L’œdème extracellulaire est secondaire à une rupture des BHR interne (localisée au niveau des jonctions serrées des cellules endothéliales des vaisseaux rétiniens) ou externe (jonctions entre les cellules de l’épithélium pigmentaire ou EP).
Les mouvements liquidiens répondent alors à la loi de Starling qui prend en compte la pression hydrostatique et la pression osmotique des différents secteurs. La perméabilité capillaire et la compliance du tissu rétinien sont les autres facteurs qui concourent à limiter l’accumulation de liquide dans l’espace extracellulaire. On comprend alors l’influence des facteurs systémiques dans l’apparition de l’OM, notamment dans l’œdème maculaire diabétique (OMD), ou de la pression osmotique dans les OM liés aux occlusions veineuses. Toutefois, ces mécanismes initiaux s’accompagnent d’une sécrétion de médiateurs inflammatoires à la fois réactionnels à la pathologie mais également dans le but de réparer les altérations tissulaires et de la BHR. L’endothélium des vaisseaux et l’EP deviennent alors cibles et acteurs d’une réaction où médiateurs de l’inflammation et facteurs de croissance conjuguent leurs effets. La complexité de ces processus physiopathologiques explique le grand nombre d’affections oculaires ou systémiques qui peuvent se compliquer d’OM (encadré 7-1
• Diabète
• Occlusion de la veine centrale de la rétine (OVCR)
• Occlusion de branche veineuse rétinienne (OBVR)
• Uvéite
• Œdèmes maculaires postchirurgicaux dont le syndrome d’Irvine-Gass
• Dégénérescence maculaire liée à l’âge (DMLA)
• Anomalies de l’interface vitréorétinien
• Purpura thrombopénique, toxémie gravidique et ischémie choroïdienne
• Macro-anévrisme
• Rétinopathie radique
• Angiomatose rétinienne
• Hémangiome choroïdien
• Mélanomes de la choroïde
• Métastases choroïdiennes
• Médicaments
• Hérédo-dégénérescences
• Télangiectasies maculaires
• Choriorétinites séreuses centrales et épithéliopathie rétinienne diffuse
• Maladie de Coats
). Pour modifier la présentation habituelle, on peut également essayer d’évoquer les étiologies en fonction de l’âge de présentation (tableau 7-1) ou de leur caractère uni- ou bilatéral (tableau 7-2).
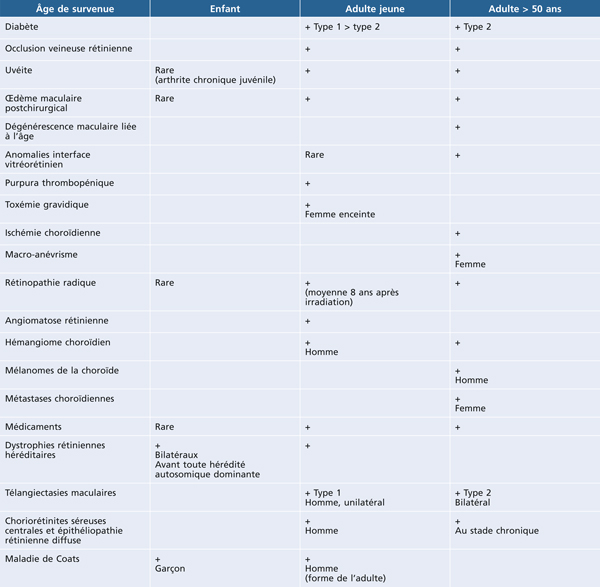
Tableau 7-1 Survenue des œdèmes maculaires en fonction de l’âge (tendance préférentielle).
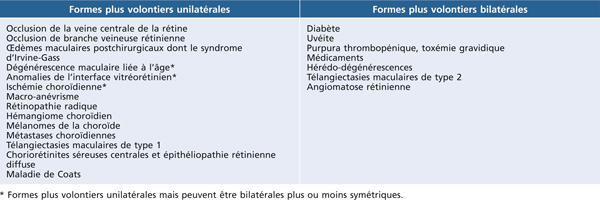
Tableau 7-2 Présentation (préférentielle) uni- ou bilatérale des œdèmes maculaires.
Les affections listées dans l’encadré 7-1 peuvent entraîner un OM lors de leur évolution. Il est difficile de donner une répartition des causes d’OM puisque celle-ci dépend bien entendu de la fréquence de la maladie en cause : un OM complique très fréquemment une rétinopathie radique mais la pathologie d’origine reste rare. En revanche, le retentissement économique de l’OMD sur la société est très lourd en raison du nombre élevé de patients diabétiques dans le monde. Par ailleurs, les prévalence et incidence rapportées actuellement sont susceptibles de se modifier sous l’effet des pratiques de dépistage, de prévention et de traitement. L’effet observé récemment sur la prévalence de la cécité, après l’apparition des anti-angiogéniques, peut également, à un certain niveau, se manifester dans les OM accessibles à un traitement. Toutes les informations ci-dessous seront détaillées dans les chapitres correspondants.
En 2014, la prévalence mondiale du diabète était estimée à 9 % chez les adultes âgés de 18 ans et plus, soit plus de 350 millions de personnes dans le monde. L’OMD représente ainsi la principale cause d’OM dans la pratique ophtalmologique. Cette complication oculaire sévère est le principal responsable de la baisse d’acuité visuelle chez le patient diabétique avec la rétinopathie diabétique proliférante. L’OMD représente, à lui seul, la première cause de cécité chez les sujets de moins de 50 ans. Son incidence est directement liée à la durée du diabète et au degré de rétinopathie diabétique (RD) : ainsi un patient diabétique de type 1 diagnostiqué avant 30 ans voit le risque d’OM passer de 0 % avant 5 ans à 29 % au bout de 20 ans ou plus. L’identification de zone de diffusion localisée à partir de micro-anévrismes (OM focal) est souvent associée à une atteinte diffuse à partir des capillaires rétiniens dilatés (fig. 7-1). Toutefois, cette distinction « focale » et « diffuse » n’est pas constamment retenue dans la littérature qui considère d’avantage l’épaississement rétinien de façon globale. La particularité de l’OMD est d’être très dépendant des facteurs systémiques (équilibre du diabète et tension artérielle essentiellement).
Les prévalences de l’OMD dans la littérature ont varié au cours des trente dernières années, tant en raison des critères différents retenus pour diagnostiquer l’OMD, qu’en raison de l’amélioration des méthodes de dépistage et de traitement de l’OMD et de la RD. La plupart des études s’appuient sur l’analyse des rétinophotographies en couleurs et l’arrivée des premières études reposant sur l’optical coherence tomography (OCT) va peut-être modifier ces données. La prévalence de l’œdème maculaire cliniquement significatif (OMCS) – soit un œdème maculaire présent dans les 500 µ centraux – est passée de 10 % en 1980 à 5 % dans les années 1990 puis environ 3 % dans les années 2000, alors que dans le même temps, on assiste à une augmentation très importante du nombre de patients diabétiques. Toutefois, cette décroissance rapportée dans les pays industrialisés cache une disparité selon le niveau socio-économique des patients mais probablement aussi d’autres facteurs encore méconnus, notamment génétiques.
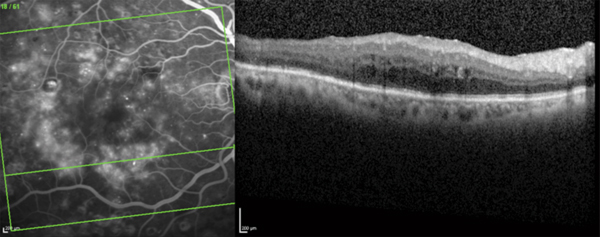
Fig. 7-1 Angiographie à la fluorescéine couplée à l’OCT montrant un OM en rapport avec une diffusion à partir de micro-anévrismes et des capillaires rétiniens chez un patient présentant une rétinopathie non proliférante modérée.
On dénombre dans le monde plus de 16 millions de patients souffrant d’occlusion veineuse rétinienne (OVR) avec 2,5 millions d’occlusions de la veine centrale de la rétine (OVCR) et 14 millions d’occlusions de branche veineuse rétinienne (OBVR). Les occlusions veineuses constituent donc la deuxième grande cause d’OM avec 40 000 nouveaux cas d’OVR et 26 000 cas d’OM liés à cette étiologie en France chaque année. Ces pathologies sont toutefois certainement sous-diagnostiquées quand elles sont limitées à l’atteinte d’une branche sans baisse de la vision. L’OM apparaîtrait dans 28 % des cas pour les OBVR et 39 % des cas pour les OVCR (fig. 7-2). Les OVR s’accompagnent d’une baisse d’acuité visuelle dans 12 % des cas avec 15 ans de suivi.
Une composante ischémique se surajoute parfois modifiant encore le pronostic. L’OM survient dans environ 30 % des OVCR non ischémiques. Le pronostic d’un OM survenant lors d’une OBVR est toutefois de meilleur pronostic avec un taux de résolution spontanée élevé (de l’ordre de 30 % environ). Il est probable que la modification des pratiques, avec un traitement de l’œdème souvent initié de façon plus précoce, s’accompagnera d’une diminution de la baisse d’acuité visuelle liée à l’OM des OVR dans les années à venir.
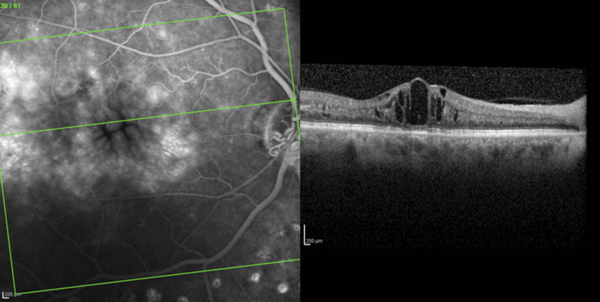
Fig. 7-2 Angiographie à la fluorescéine couplée à l’OCT montrant un OM cystoïde compliquant une OVCR.
Les uvéites constituent la cause d’OM dans laquelle l’inflammation joue un rôle central. Il s’agit d’une complication fréquente des uvéites qui peut persister même si l’affection générale est contrôlée. Les uvéites peuvent apparaître à tout âge de la vie mais touchent avant tout l’adulte jeune. Avec une prévalence de l’ordre de 38 cas pour 100 000 personnes, on peut estimer qu’environ 20 000 personnes sont porteuses d’une uvéite en France. Vingt-sept pour cent des patients vont présenter une baisse de vision liée à un OM mais cette complication est très variable selon la maladie d’origine : si l’OM peut compliquer toutes les uvéites, les principales causes d’OM sont les uvéites intermédiaires et postérieures, mais également certaines uvéites antérieures non granulomateuses associées au HLA-B27 (human leucocyte antigen B27).
On parle d’œdème postchirurgical entre 1 et 4 mois après chirurgie, l’œdème rentrant dans la catégorie chronique au-delà de 6 mois. La prévalence de l’OM postchirurgical varie de 0,2 à 50 % selon les modalités utilisées pour le mettre en évidence et le délai postchirurgical. Alors que l’examen biomicroscopique l’identifie dans 0,2 % des cas, l’angiographie montre un OM sans baisse de vision dans plus de 25 % des cas et les techniques d’OCT dans environ 5 % des cas (fig. 7-3). Avec le temps, ce taux diminue puisque seuls 3 % des patients présentent un OM angiographique à 12 mois postopératoires.
L’amélioration des techniques s’est sans aucun doute accompagnée d’une diminution de sa prévalence depuis les chirurgies en intracapsulaire. Sa fréquence réelle est largement sous-évaluée, car il ne s’accompagne d’aucune manifestation dans la plupart des cas. Seuls 1 % des patients ressentiraient une sensation de baisse visuelle. Environ 90 % des OM postchirurgicaux s’améliorent spontanément. En revanche, une complication peropératoire augmente fortement ce risque à 35 % en cas de rupture capsulaire par exemple. Enfin, la conjonction de deux situations favorisant l’OM (comme le diabète) augmente ce taux d’OM d’autant plus que l’état rétinien n’a pas été préalablement traité. Les pathologies chirurgicales rétiniennes peuvent également se compliquer d’OM avec survenue d’environ 10 % d’OM dans les suites de décollements de rétine soulevant la macula, ce chiffre étant assez stable dans le temps. La meilleure connaissance des facteurs de risque, comme le diabète, justifie les traitements préventifs (par injection intravitréenne par exemple) susceptibles de limiter cette complication.
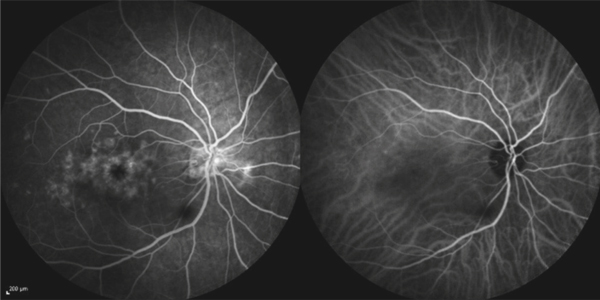
Fig. 7-3 Angiographie à la fluorescéine (à gauche) montrant un OM cystoïde associé à un œdème papillaire dans le cadre d’un syndrome d’Irvine-Gass. L’angiographie au vert d’indocyanine est normale (à droite).
Un œdème maculaire peut compliquer une dégénérescence maculaire liée à l’âge (DMLA) dans sa forme exsudative. Il survient généralement en association avec un décollement séreux rétinien d’autant plus qu’il a été prolongé et que la néovascularisation était rétrofovéolaire. L’apparition de la composante exsudative bien visible sur l’OCT est devenue synonyme de récidive. Toutefois, il faut distinguer les logettes intrarétiniennes, signe de récidive de la DMLA, des petits kystes involutionnels sans pronostic défavorable marquant simplement une forme de cicatrisation de la lésion néovasculaire (fig. 7-4).
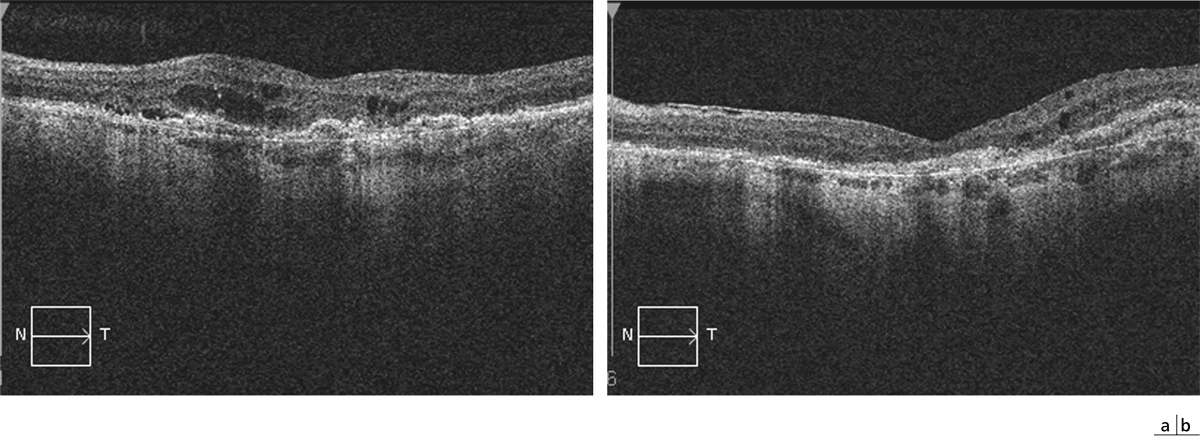
Fig. 7-4 Logettes intrarétiniennes chez un patient présentant une DMLA exsudative suivie dans le cadre d’un protocole « treat and extend ».
a. Logettes intrarétiniennes associées à un décollement sous-rétinien signant la récidive de l’exsudation. b. Aspect de petites logettes résiduelles sans signe de reprise évolutive.
Les membranes épirétiniennes induisent une rétraction superficielle de la rétine. L’OM est lié à plusieurs mécanismes intriqués associant une distorsion des vaisseaux rétiniens responsable de la fuite liquidienne, une altération du flux capillaire et une perte d’adhésion de la rétine sur l’EP limitant les capacités de ce dernier à pomper les fluides. Cette situation est encore plus marquée dans les aspects de traction vitréomaculaire, la survenue du décollement du vitré pouvant permettre la disparition de l’œdème. L’épaississement rétinien constant dans une membrane ou un syndrome de traction vitréomaculaire peut s’améliorer après ablation de la membrane épirétinienne (MER) et d’une éventuelle limitante interne rétractée, mais se compliquer secondairement d’un œdème maculaire postchirurgical. Cette complication est également plus marquée en cas de facteurs de risque lors des membranes secondaires par exemple.
En dehors des pathologies avec altération des vaisseaux mentionnés ci-dessus, différentes maladies avec atteintes vasculaires peuvent s’accompagner d’OM. Ces pathologies regroupent différentes étiologies cumulant, à des degrés divers, facteurs vasculaires systémiques et locaux, ischémie rétinienne et proliférations vasculaires. On y rassemble les étiologies comme le purpura thrombopénique, la toxémie gravidique et l’ischémie choroïdienne, les angiomatoses rétiniennes ainsi que les macro-anévrismes.
Les OM peuvent également survenir lors des pathologies tumorales que sont les hémangiomes choroïdiens, les mélanomes de la choroïde et les métastases. Ils compliquent soit la pathologie d’origine, soit les traitements employés pour les traiter dans le cadre de la rétinopathie radique. L’ischémie rétinienne associée est souvent responsable de leur sévérité.
On distingue les OM liés à des instillations locales et les OM liés à des traitements systémiques. Ces derniers sont souvent transitoires et cèdent à l’arrêt du traitement mais leur identification précoce est indispensable.
L’OM est une cause fréquente de baisse de vision chez le patient atteint de rétinopathie pigmentaire (RP) et l’apparition d’un OM maculaire bilatéral chez un patient jeune doit faire évoquer une RP débutante. Les télangiectasies maculaires de type 1 constituent une forme clinique d’OM unilatéral radicalement différente de l’atrophie maculaire finale rencontrée dans les télangiectasies de type 2 (fig. 7-5).
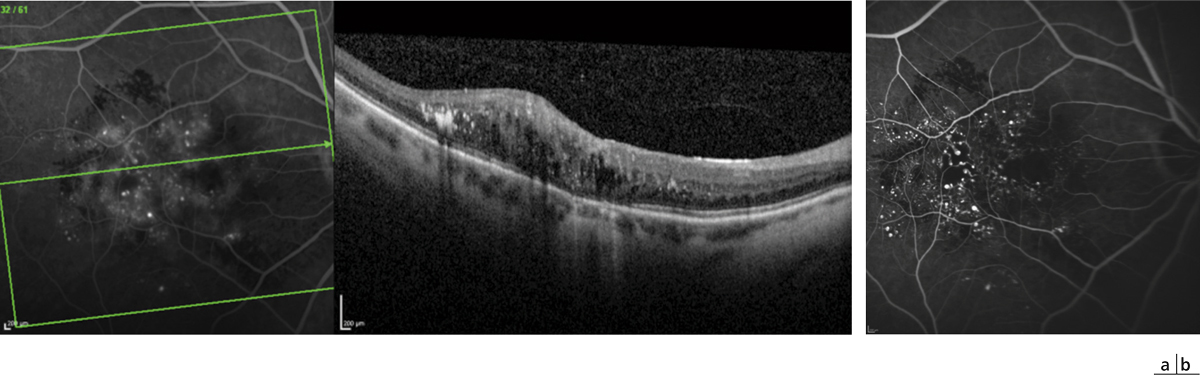
Fig. 7-5 a, b. Angiographie à la fluorescéine couplée à l’OCT montrant des dilatations anormales des capillaires périfovéolaires associées à un OM dans le cadre de télangiectasies maculaires de type 1.
Ces OM surviennent volontiers chez le sujet jeune et sont associés à des phénomènes exsudatifs variés (fig. 7-6).
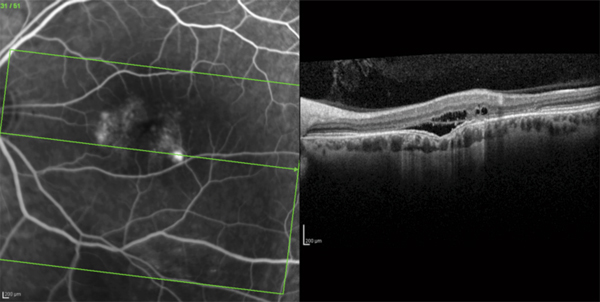
Fig. 7-6 Angiographie à la fluorescéine couplée à l’OCT retrouvant un OM avec diffusion de fluorescéine en regard d’un point de fuite dans le cadre d’une choriorétinopathie séreuse centrale.
Certaines situations s’accompagnent d’une véritable dilacération des couches rétiniennes en association avec un mécanisme tractionnel, de probables altérations de la circulation choroïdienne ou des anomalies héréditaires ou embryologiques. Ces affections ne s’accompagnent pas réellement d’atteinte de la BHR mais vont se traduire par un augmentation de l’épaisseur de la rétine et à ce titre sont à situer plutôt dans les limites de l’œdème. Ces situations regroupent :
les affections du myope fort comprenant le schisis du myope fort, les aspects de macula bombée et les dysversions papillaires ;
les anomalies héréditaires ou du développement regroupant le rétinoschisis lié à l’X et autres hérédo-dégénérescences et les fossettes colobomateuses de la papille ;
les œdèmes maculaires microkystiques : la finesse des explorations par OCT a permis la mise en évidence des pseudo-kystes maculaires dont on a longtemps pensé qu’ils étaient limités à la population des patients porteurs de neuropathie, mais dont on sait maintenant qu’ils sont très probablement non spécifiques d’une affection donnée sans que l’on connaisse réellement leur signification.